里程碑:FDA首次批准LNP递送的体内CRISPR基因编辑进行人体临床试验
以CRISPR-Cas9为代表的基因编辑技术,大大加速了基因治疗的发展,为许多原本无药可医的疑难疾病带来了巨大希望。
2023年3月2日,Intellia Therapeutics宣布,FDA批准了其治疗遗传性血管性水肿(HAE)的体内CRISPR疗法NTLA-2002的研究型新药(IND)申请。这也是首个获得FDA批准用于人体临床试验的LNP递送的体内CRISPR基因编辑疗法。
NTLA-2002,是一种体内CRISPR基因编辑候选疗法,通过脂质纳米颗粒(LNP)以mRNA形式递送CRISPR-Cas9基因编辑系统,靶向敲除KLKB1基因,以永久性降低血浆中激肽释放酶活性,从而防止遗传性血管性水肿(HAE)的发作。

Intellia Therapeutics是由CRISPR基因编辑技术奠基人、诺奖得主詹妮弗·杜德娜(Jennifer Doudna)创立的基因编辑治疗公司。

2021年6月26日,Intellia公司在国际顶尖医学期刊《新英格兰医学杂志》(NEJM)发表论文,报道了CRISPR基因编辑疗法NTLA-2001治疗转甲状腺素蛋白淀粉样变性(ATTR)的效果,这是世界首个公布的体内CRISPR基因编辑疗法的临床试验结果。
这项临床研究大大扩展了CRISPR基因编辑疗法的应用范围,直接注射LNP递送的CRISPR基因编辑组份即可在体内进行高效基因编辑,这为许多遗传疾病的治疗开辟了新的途径,被誉为“开启了医学新时代”。
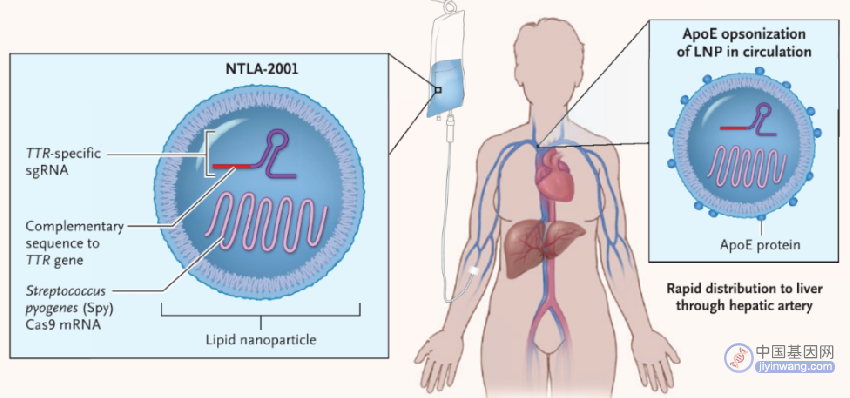
2022年6月,Intellia公布了NTLA-2001疗法的中期临床试验结果,结果显示在治疗后2个月至12个月的随访期,患者的血清转甲状腺素蛋白(TTR)水平持续保持下降。这也说明了LNP递送的CRISPR基因编辑可在体内产生长期治疗效果。
NTLA-2002,是Intellia公司开发的第二款体内CRISPR基因编辑疗法,旨在评估NTLA-2002在I型或II型遗传性血管性水肿(HAE)成人患者中的安全性、耐受性、药代动力学和药效学,包括测定治疗后血浆中激肽释放酶活性水平以及HAE发作率。其中1期临床试验为开放标签、单剂量递增设计,用于确定NTLA-2002的不同剂量水平,2期临床试验将进行随机、安慰剂对照的进一步评估。
遗传性血管性水肿(HAE)是一种罕见遗传性疾病,大约50000人中有1人患病。其特征是身体各个器官和组织中出现严重、反复和不可预测的炎症发作,让患者倍感痛苦、衰弱,甚至危及生命。目前的治疗选择通常是终身治疗,需要每周两次慢性静脉内给药或皮下注射给药,或每天口服给药。但即使长期用药,仍会发生突破性发作。而抑制激肽释放酶(kallikrein)是一种经过临床验证的预防遗传性血管性水肿(HAE)的策略。
NTLA-2002 的治疗原理是通过LNP递送CRISPR-Cas9基因编辑靶向肝脏细胞的KLKB1基因,从而抑制激肽释放酶(kallikrein)的产生,进而抑制缓激肽(bradykinin)的产生,而缓激肽的过度产生会导致遗传性血管性水肿(HAE)的发作。
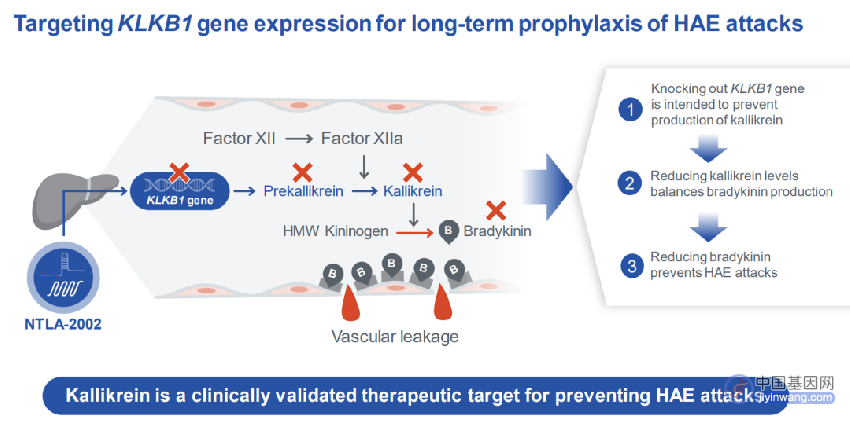
2022年11月12日,Intellia公布了NTLA-2002疗法在治疗遗传性血管水肿(HAE)的1/2期临床试验的中期数据。
这些临床数据来自接受 NTLA-2002 疗法的10名不同剂量的遗传性血管水肿(HAE)成年患者,结果显示,所有不同剂量(25mg、50mg、75mg)治疗的患者的致病性的激肽释放酶均显著下降,分别在第32周、第22天、第16周时下降64%、81%、92%。
此外,这些数据还显示,患者在接受单次治疗后遗传性血管水肿(HAE)的发作频率显著下降,25mg和75mg剂量组在治疗后第1周到第16周,发作频率平均分别下降了91%和78%(当时50mg剂量组尚未达到第16周的观察时间)。截至公布数据时,最早接受治疗的三名患者已有5.5-10.6个月没有再发作。在所有剂量组中,NTLA-2002 的耐受性普遍良好,大多数不良事件是轻微的。这些临床数据显示了NTLA-2002具有一次治疗、持续缓解的潜力。
Intellia总裁兼CEO John Leonard 博士说表示,FDA接受了NTLA-2002的IND申请以启动临床评估,使我们更接近于为遗传性血管性水肿(HAE)患者带来一种可能改变当前治疗范式的颠覆性疗法。NTLA-2002的IND获批标志着Intellia的一个重要里程碑,继续奠定Intellia因作为基因组编辑领域领导者的地位。很高兴能在美国推进NTLA-2002疗法的开发,目前,Intellia正在努力快速招募患者参加2期临床试验,期待着今年晚些时候公布这项研究的首批人体试验的更多数据。
Intellia研发管线
Intellia的研发管线分为体内CRISPR疗法和体外CRISPR疗法两大类。
目前,体内CRISPR疗法中有两项正在进行临床试验,分别是NTLA-2001(治疗转甲状腺素蛋白淀粉样变性)和NTLA-2002(治疗遗传性血管性水肿)。
另有NTLA-2003(治疗α1-抗胰蛋白酶缺乏性肝病)、NTLA-3001(治疗α1-抗胰蛋白酶缺乏性肺病)和一款治疗血友病B型的疗法正在IND申请,第一种为基因敲除型,后两种为基因插入型。
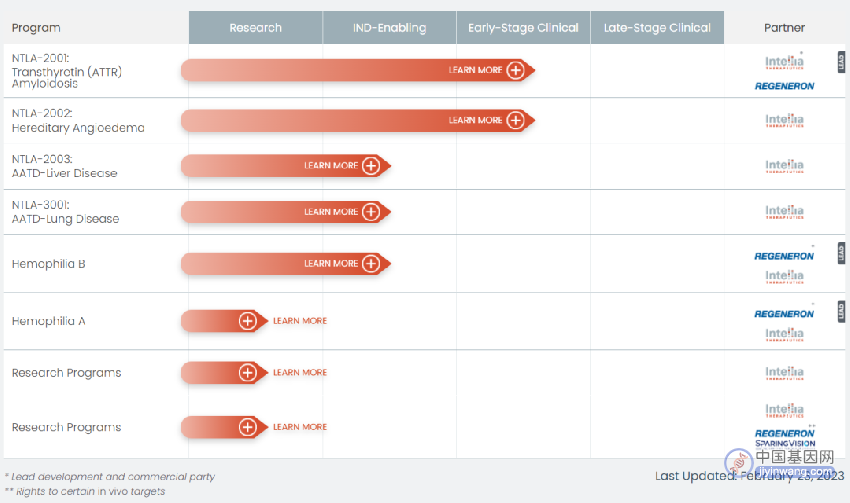
而体外CRISPR疗法中,与诺华合作开发的镰状细胞病疗法,以及独立开发的治疗急性髓细胞白血病的NTLA-5001,此前已开始临床试验,但在最新公布的研发管线中已删除。还有一款治疗CD30阳性淋巴瘤的通用型CAR-T疗法NTLA-6001正在IND申请。

参考资料:
https://www.intelliatx.com/
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。