2023年基因治疗药物回顾盘点,这些基因疗法获批上市!
现代医学与分子生物学的融合催生了基因治疗概念。基因治疗的历史可追溯到1970年代,科学家们首次在细胞中进行基因治疗科学实践。1980年代,随着基因工程技术的快速发展,基因治疗开始进入实验室阶段。1990年代,第一例基因治疗临床试验在美国开展。在随后的几十年里,不断有科学家们在基因治疗领域进行探索和研究,并逐渐取得了一些突破性的进展。
2017年,美国FDA批准了第一款基因疗法,该疗法用于治疗一种罕见的儿童遗传性疾病。此后,基因治疗领域进入了一个新的发展阶段,相继有更多的基因疗法获得批准并用于治疗不同类型的疾病。
基因治疗定义有广义和狭义之分,狭义的概念是指用具有正常功能的基因置换或增补患者体内有缺陷的基因,从而达到治疗的目的。广义的概念指把某些遗传物质转移到患者体内,使其在患者体内表达,最终达到治疗某种疾病的方法。

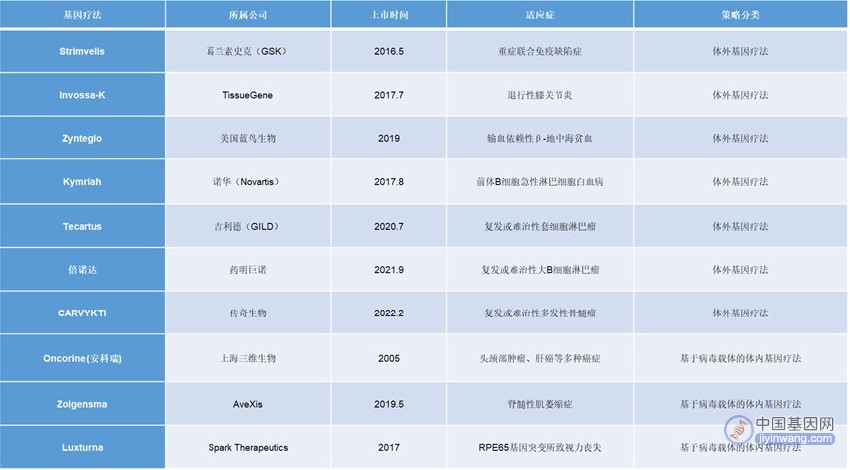
截至目前,全球累计共有54款广义上的基因治疗药物获批上市,其中体外基因疗法17款;基于病毒载体的体内基因疗法16款;小核酸药物19款;质粒药物2款。
在过去的2023年累计有6款基因治疗新药物获批上市。适应症包括四种罕见病以及两种非实体瘤。
因此,我们对2023年基因治疗药物进行盘点,与大家一起回顾过去一年中这些获批上市的药物,希望能够给大家带来更多的启示。
上市基因治疗药物盘点
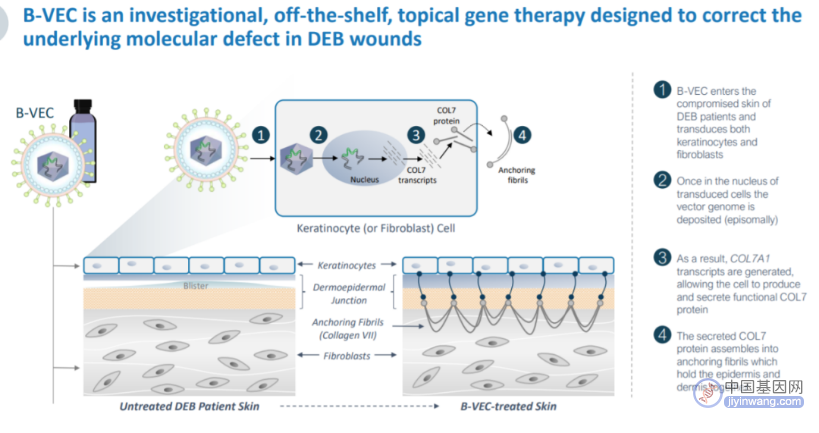
2023年5月,全球首款营养不良型大疱性表皮松解症基因治疗药物Vyjuvek (Beremagene Geperpavec)获批上市。它是Krystal Biotech开发的首个FDA批准的外用基因疗法,也是首款可重复给药的基因疗法。营养不良型大疱性表皮松解症(DEB)是一种罕见且严重的单基因遗传病,由编码VII型胶原蛋白(COL7)的COL7A1基因出现突变引起,使得皮肤缺少胶原蛋白,从而导致表皮与真皮分离。Vyjuvek采用了改造的I型单纯疱疹病毒(HSV-1)作为COL7A1的递送载体制备成可涂抹的外用药膏,让患者以一种更为简单、便捷方式来补充缺失的COL7A1基因的正常拷贝,以生成功能性COL7A1蛋白,针对导致疾病的根本机制进行治疗。
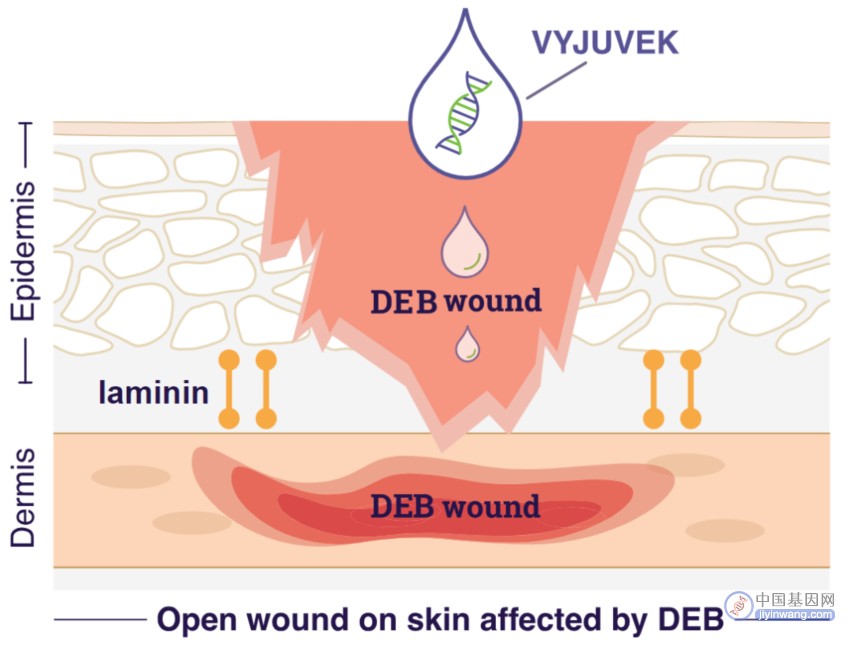
图片来源:Vyjuvek官网
2023年6月,全球首款杜氏肌营养不良症基因疗法药物Elevidys (Delandistrogene Moxeparvovec)获批上市。杜氏肌营养不良症(DMD) 是由X染色体上的抗肌萎缩蛋白基因突变引起的,导致缺乏或不产生抗肌萎缩蛋白。抗肌萎缩蛋白是一种保持肌肉细胞完整必不可少的蛋白质。Elevidys是Sarepta Therapeutics开发的一种基于腺相关病毒(AAV rh74)的基因疗法。它通过向肌细胞传递一种编码缩短版的抗肌萎缩蛋白的基因,即Elevidys微型抗肌萎缩蛋白,以弥补患者缺乏的正常抗肌萎缩蛋白,这解决了导致DMD的潜在遗传缺陷。该疗法旨在恢复因遗传性肌肉疾病的根源突变而丧失的功能。
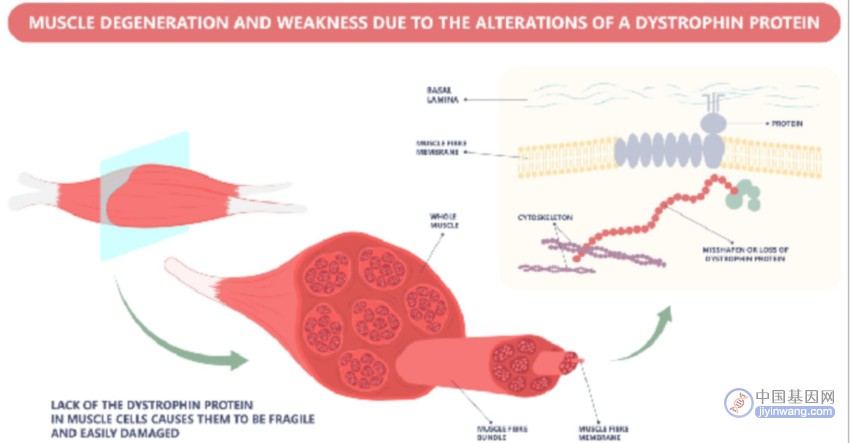
图片来源:Pepermpron/Shutterstock.com
2023年11月,全球首款利用CRISPR基因编辑技术治疗罕见血液疾病的基因治疗药物Casgevy (Exagamglogene Autotemcel)获批上市。Casgevy是Vertex Pharmaceuticals开发的一种自体、体外CRISPR/Cas9基因编辑的细胞疗法。通过对患者自身的造血干细胞在体外电转导入CRISPR/Cas9进行基因编辑,使得编辑后分化的红细胞能够产生高水平的胎儿血红蛋白(HbF)。HbF是携带氧气的血红蛋白,在胎儿发育期间天然存在,在出生后转变为成人形式的血红蛋白。Casgevy对HbF水平的升高能够减少或消除SCD患者的疼痛和血管闭塞性危象 (VOC),并缓解TDT患者的输血需求。
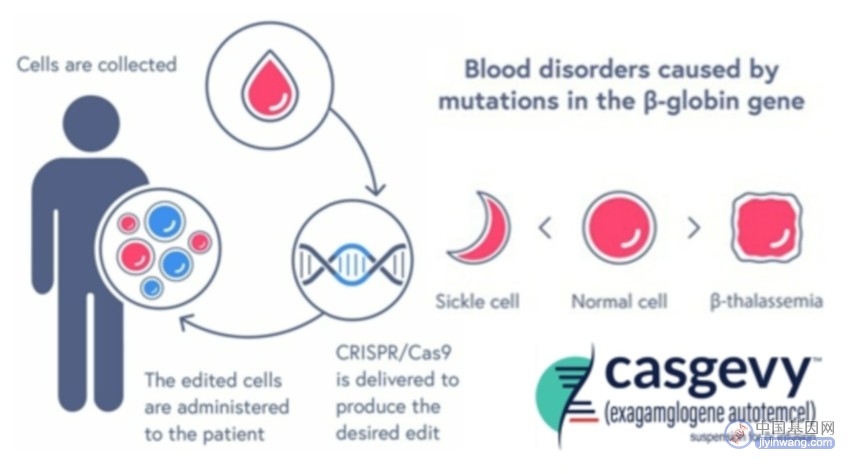
图片来源:CRISPR Therapeutics
2023年12月,一款治疗镰刀型细胞贫血病(SCD)的基因治疗药物Lyfgenia (lovotibeglogene autotemcel)获批上市。Lyfgenia是Bluebird Bio开发的一款基于慢病毒载体的细胞基因疗法,通过慢病毒载体将功能性β珠蛋白基因永久添加到患者自身的造血干细胞(HSC)中,可持久产生具有抗镰状细胞特性的血红蛋白(HbAT87Q型),HbAT87Q型与野生型 HbA 具有相似的氧结合能力,限制红细胞镰状化,并有可能减少血管闭塞事件 (VOE),这是一种一次性疗法,适用于12岁及以上的患者。
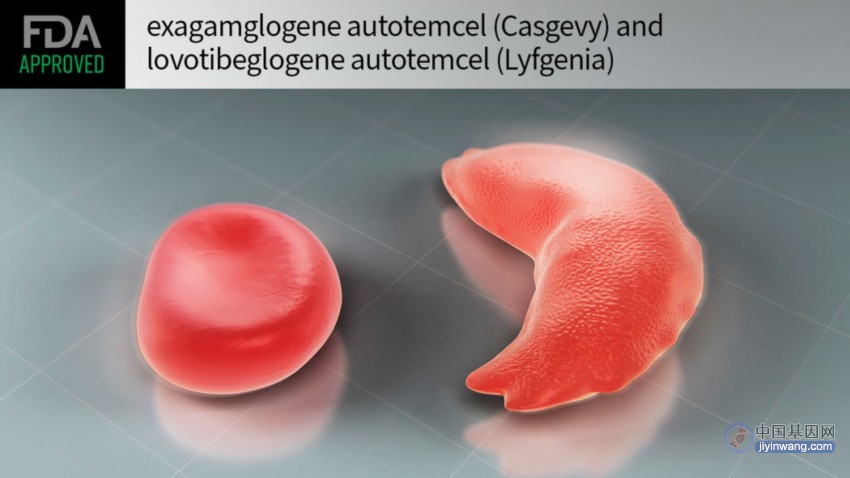
图片来源:Milestone Gene Therapies for Sickle Cell Disease Greenlit by FDA— Casgevy and Lyfgenia approved for one-time treatment of sickle cell disease
2023年,NMPA批准了2款细胞与基因治疗新药物在境内上市,分别是6月份获批的伊基奥仑赛注射液(商品名:福可苏)和11月份获批的纳基奥仑赛注射液(商品名:源瑞达)。福可苏是由驯鹿生物与信达生物共同开发的首款在中国获批的BCMA靶向CAR-T疗法,用于治疗既往经过至少3线治疗后进展的复发或难治性多发性骨髓瘤(r/r MM)成人患者。源瑞达是由合源生物开发的首款在中国获批的治疗白血病的CAR-T疗法,用于治疗成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。两款药物在关键性临床研究中展示出良好的安全性和积极的治疗效果。
总结与展望
基因治疗药物在2023年取得了令人瞩目的进展,共有6款新药获批上市,涵盖了多个领域的疾病治疗。这一系列的上市药物展现出了基因治疗在医学领域的巨大潜力,为许多患者带来了新的希望和治疗选择。从首次利用CRISPR基因编辑技术治疗罕见血液疾病的Casgevy,到用于治疗镰刀型细胞贫血病的Lyfgenia,再到外用治疗营养不良型大疱性表皮松解症的Vyjuvek,这些药物的上市标志着基因治疗领域迎来了新的突破。在这一年中,我国也有36款基于AAV载体的基因治疗药物IND申报获批,并且有3款药物进入了III期临床,未来也将进一步推动行业的发展。
基因治疗药物的不断涌现为更多疾病提供了治疗可能性,为医学界拓展了新的研究方向。随着技术的不断进步,我们可以期待基因治疗在更多疾病治疗中发挥重要作用,包括罕见病、遗传性疾病以及一些难以治愈的疾病。
此外,随着基因治疗技术的成熟和临床实践的积累,相信未来会有更多安全、有效的基因治疗药物问世。同时,我们也需要面对一些挑战。基因治疗药物的研发和上市需要投入大量的时间和资源,安全性、成本等问题也需要得到充分考虑。我们期待未来在这些方面取得更多的进展,以确保基因治疗药物能够更广泛地造福患者。
2023年是基因治疗领域取得重要进展的一年,展望未来,基因治疗药物的研发与应用将继续成为医学领域关注的焦点,为人类健康带来更多希望与可能。
希望在未来的日子里,基因治疗能够不断取得新的突破,为医学事业和社会健康做出更大的贡献。在龙年到来之际,让我们共同期待、共同创造一个更加美好的未来!
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。