艾滋病治愈的希望:CCR5Δ32/Δ32缺陷基因的造血干细胞移植
继2009年和2019年成功治愈 HIV-1的2名病例——“柏林患者”和“伦敦患者”之后,再次传来好消息,2023年2月20日发表在世界权威杂志《自然》上的一篇研究论文,再度激起了彻底治愈世纪绝症“艾滋病”的希望。

让我们通过论文来还原这第三例被治愈的艾滋病患者过程。
该名患者是一名 53 岁男性,于2008 年1月被诊断为HIV-1感染,B亚型,这是欧美流行的主要亚型,初始CD4 + T 细胞计数为964个细胞/μl,HIV-1血浆病毒载量为12,850 拷贝/ml,根据当时的美国治疗指南,没有启动抗病毒治疗。直到2010 年 10 月,开始进行抗病毒治疗,当时CD4 + T 细胞为503个细胞每微升和病毒载量为每毫升35,303个HIV-1 拷贝,治疗后血浆病毒载量持续受到抑制(图1a)。
但祸不单行,该患者于2011年1 月,被诊断为急性髓性白血病 (AML) M2,化疗后患者获得血液学完全缓解,但2012 年 9 月,患者急性髓性白血病复发,在接受新化疗方案方案后实现了第二次完全缓解。
2013年2月患者移植了带有CCR5Δ32/Δ32缺陷基因的造血干细胞。在接受了长达9年多的各项最敏感检测技术指标的监测后,同“柏林患者”和“伦敦患者”一样,奇迹再次出现。
不仅在治疗过程中,血液中的前病毒 HIV-1 DNA 和 HIV-1 RNA 检测不到(图1a ),同时,对外周血、淋巴和肠道组织中 HIV-1 病毒库的多次评估显示,血液中除在几个时间点有零星的 HIV-1 DNA 痕迹,第 51 个月的腹股沟淋巴结组织切片和第 77 个月的一些肠道活检组织切片中检测到了残留的 HIV-1 DNA 和 HIV-1 RNA(图 1b 外,大多数时候检测不到病毒存在,更重要的是,无论是通过重复的基于细胞培养的定量病毒生长测定还是通过完整的原病毒 DNA 测定,都无法在外周血单核细胞 (PBMC) 中检测到 HIV-1 p24、HIV-1 RNA 或 HIV-1 DNA。使用两种不同的人源化小鼠模型进行的体内生长阴性试验证实了测试样本中不存在具有复制能力的病毒。
通过综合评判和获得伦理委员会的批准,于 2018 年 11 月,患者在骨髓移植后 69 个月停止艾滋病的抗病毒治疗,在抗病毒治疗后收集的四份血浆样本中未检测到抗逆转录病毒药物存在(图1a),患者也没有任何艾滋病的临床或实验室体征。停止治疗48个月后,也没有出现血浆 HIV-1 RNA 的反弹(图1a)。
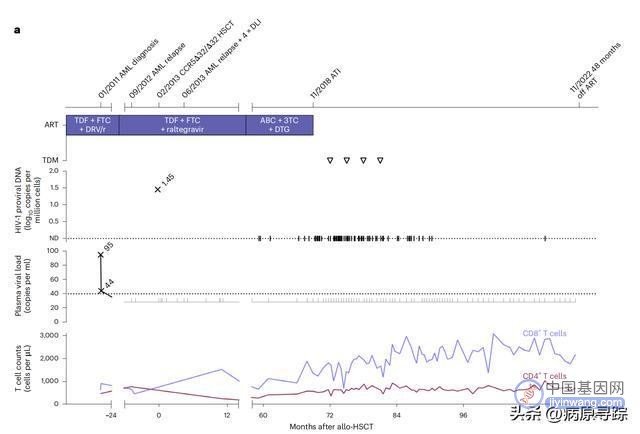
图 1:抗病毒中断前后的临床过程和 HIV-1 病毒库 a,临床事件、ART 方案、HIV-1 血浆病毒载量、来自 PBMC 的原病毒载量
以及 CD4 +和 CD8 +计数。三角形表示 停止治疗后 3、6、9 和 12 个月治疗药物监测 (TDM) 的阴性结果。ABC,阿巴卡韦;ND,检测不到。
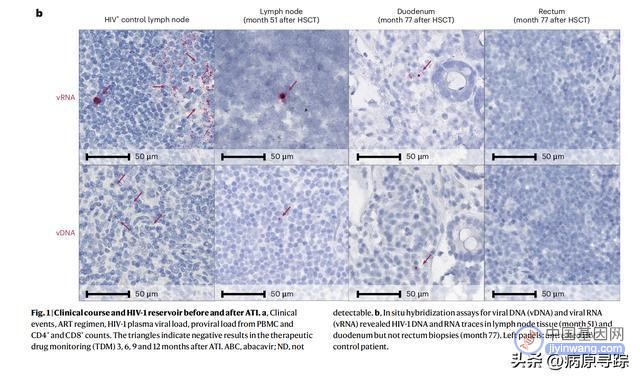
图 1:抗病毒中断前后的临床过程和 HIV-1 病毒库 b,病毒 DNA (vDNA) 和病毒 RNA (vRNA) 的原位杂交分析揭示了淋巴结组织(第 51 个月)和十二指肠中的 HIV-1 DNA 和 RNA 痕迹,但直肠活检(第 77 个月)中没有。左图:未经治疗的 HIV +对照患者。
另一方面,在停止抗病毒治疗后,患者外周血NK 细胞和细胞毒性CD8 + T 细胞的活化水平与正常人的基本一样(图2a、b),在骨髓移植后第39个月,通过细胞内细胞因子染色,在 HIV-1 Gag、Pol 和 Nef 的重叠肽库的刺激下,检测到 HIV-1特异性 CD8 + T 细胞,并且在停止治疗后没有增加(图2c ),HIV-1 特异性抗体反应的免疫印迹分析与细胞 HIV-1 反应性的逐渐丧失相平行:抗 gp120 和抗 gp160 抗体显示出最长的持久性(图 2d),在骨髓移植后第39个月,外周血 HIV-1 特异性抗体水平低于 PLWH 的临界值,与正常人相当。因为病毒特异性反应的维持依赖于慢性感染中的抗原刺激, 极度微弱和减弱的 HIV-1 特异性 T 细胞反应和特异性抗体水平的降低表明,能够产生抗原的 HIV-1 储存库已被骨髓移植程序和/或移植物抗HIV效应极度耗尽 。
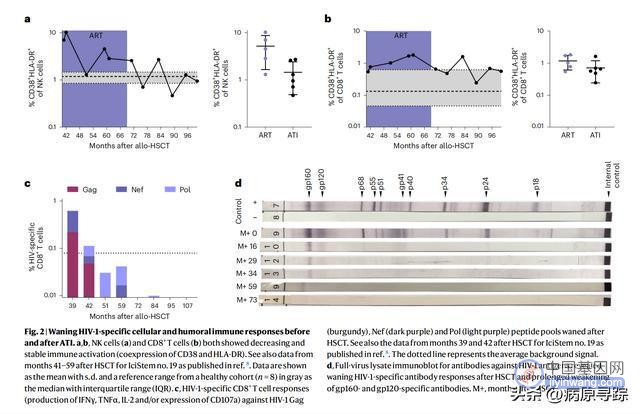
图 2:ATI 前后 HIV-1 特异性细胞和体液免疫反应减弱
a , b , NK 细胞 ( a ) 和 CD8 + T 细胞 ( b ) 均表现出降低和稳定的免疫激活(CD38 和 HLA-DR 的共表达),数据显示为 sd 的平均值和来自健康队列 ( n = 8) 的参考范围,以灰色显示为带四分位距 (IQR) 的中位数。c、HIV-1特异性CD8 +HSCT 后,针对 HIV-1 Gag(深的紫红色)、Nef(深紫色)和 Pol(浅紫色)肽库的 T 细胞反应(IFNγ、TNFα、IL-2 的产生和/或 CD107a 的表达)减弱。虚线代表平均背景信号。d,针对 HIV-1 抗原的抗体的全病毒裂解物免疫印迹显示造血干细胞移植后 HIV-1 特异性抗体反应减弱以及 gp160 和 gp120 特异性抗体的长期减弱。
该研究结果的意义在于,在已经发表的两名被治愈的艾滋病患者基础上,通过对这名艾滋病全并急性髓性白血病患者,进行同种异体CCR5Δ32/Δ32 造血干细胞移植后9年多的跟踪监测。从免疫学和病毒学相关性的方面进行了深入研究。分析治疗中断四年后,没有病毒反弹,也没有HIV-1抗原持续存在的免疫学相关性,这是CCR5Δ32/Δ32造血干细胞移植后 HIV-1 治愈的有力证据,也再一次科学证明 CCR5Δ32/Δ32 造血干细胞移植是可以治愈艾滋病的。
参考文献
1.Björn-Erik Ole Jensen.et al.In-depth virological and immunological characterization of HIV-1 cure after CCR5Δ32/Δ32 allogeneic hematopoietic stem cell transplantation.Nature published online:20 february 2023.
2. Hütter, G. et al. Long-term control of HIV by CCR5 delta32/delta32 stem-cell transplantation. N. Engl. J. Med. 360, 692–698(2009).
3. Gupta, R. K. et al. HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem-cell transplantation. Nature 568, 244–248(2019).
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。