基因治疗曲折发展历史:基因治疗的时代来了吗?
在精准医疗时代,个体化诊疗将成为未来趋势,不同患者,对于疾病的耐受程度、治疗的敏感性和不良反应等各不相同。测序技术对患者突变基因进行检测,结合基因编辑技术可精准修复突变基因,给某些疾病带来彻底治愈的可能。可以预见,在不久将来基因治疗将真正成为一种常规的安全的治疗方法,为维护人类健康做出重要贡献。
先来感受一下基因治疗的曲折发展历史
简史:基因治疗
1972年:弗里德曼(Friedmann) 和卢布林(Roblin)在《科学》杂志上发表了一篇题为《人类遗传病的基因治疗?》的论文,,引用了Rogers(1970)的观点,提出外源性的好的DNA可以用来代替那些有遗传缺陷的人的坏的DNA。
1984年:设计了一个逆转录病毒载体系统,可以有效地将外源基因插入到哺乳动物染色体。
1990年:9月14日,在William French Anderson的指导下,美国国家卫生研究院(NIH)首次进行基因治疗临床研究。1990年,利用逆转录病毒载体将腺苷脱氨酶(ADA)基因转移到两名严重的免疫缺陷(ADA- SCID)患儿的T细胞中。治疗后,患儿血液中T细胞数量开始正常。基因治疗结束后的2年内,整合的病毒载体和ADA基因在患儿的T细胞中持续发挥作用。虽然存在许多不确定因素,但研究人员认为基因治疗是一种安全、有效的治疗方法,可用于某些严重免疫缺陷疾病的治疗。
1992-1993年:提出了癌症的基因治疗。利用表达反义IGF-I RNA的载体治疗多形性胶质母细胞瘤(是一种恶性脑肿瘤)。
1999年:美国FDA暂停了多项基因治疗的临床试验。Jesse Gelsinger是第一位在基因治疗的临床试验中死亡的患者。他患有鸟氨酸氨甲酰转移酶缺乏症,这是一种与X基因有关的肝脏疾病。Jesse Gelsinger当时18岁,注射病毒载体4天后,全身出现大规模严重免疫反应,致使各器官衰竭而死亡。
截至2000年,全世界大约有4000名患者参与了500多个基因治疗的临床试验项目,其中77%来自美国,69%是针对癌症治疗。整个基因治疗行业呈现出一片欣欣向荣的局面。Jesse Gelsinger的死亡对逐步走向正轨的基因治疗无疑是当头棒喝。关于基因治疗,社会舆论、资本投入、学术研究也因此走入一个寒冬。
2000年:法国巴黎内克尔医院Alain Fisher领导的研究组报道了两例针对重症联合免疫缺陷症患者的基因治疗初步成功,然而,3年后,有两例年轻患者出现了类似血癌的症状。
2003年:1月,FDA暂时中止了所有用逆转录病毒来基因改造血液干细胞的临床试验;经过3个月严格审核权衡后,又允许基因治疗临床试验继续进行。同年10月,中国批准了基因治疗药物“今又生”上市,成为世界上第一个国家批准的基因治疗药物,这是一个腺病毒介导的P53病毒载体,用于晚期鼻咽癌配合放疗的联合治疗,但它的批准上市一直存在争议,临床应用也很有限,2008年被吊销生成许可。
2011年:Neovasculgen在俄罗斯注册,成为治疗外周动脉疾病的第一类基因治疗药物。
2012年:荷兰UniQure公司的Glybera通过欧盟审批,这个项目采用腺相关病毒作为载体,用于治疗脂蛋白脂肪酶缺乏引起的严重肌肉疾病,它的获批上市开启了基因治疗的新时代。2014年:FDA授予美国圣地亚哥医药公司Celladon针对心衰的基因治疗药物MYDICAR,这是FDA首次认定的基因疗法。2015年:AMGEN公司的溶瘤病毒药物T-Vec分别在美国和欧洲获得批准上市,这是基于单纯疱疹病毒载体的黑色素瘤的基因疗法,成为第一个被批准的非单基因遗传疾病的基因疗法。
2016年:逆转录病毒载体衍生的基因治疗药物 Strimvelis 被欧洲药品管理局( EMA) 批准用于治疗儿童腺苷脱氨酶缺乏的重度联合免疫缺陷症(ADA-SCID)。Strimvelis 由意大利 San Raffaele Tel- ethon 研究所与葛兰素史克(GSK) 公司联合开发,通过病毒载体将正常基因整合到患者造血干细胞,成功治愈 18 名患者。
2017年:美国FDA批准了第一项基因治疗-CAR-T疗法(Kymriah) ,用于治疗急性淋巴细胞白血病、弥漫性大B细胞淋巴瘤。

腺相关病毒AAV
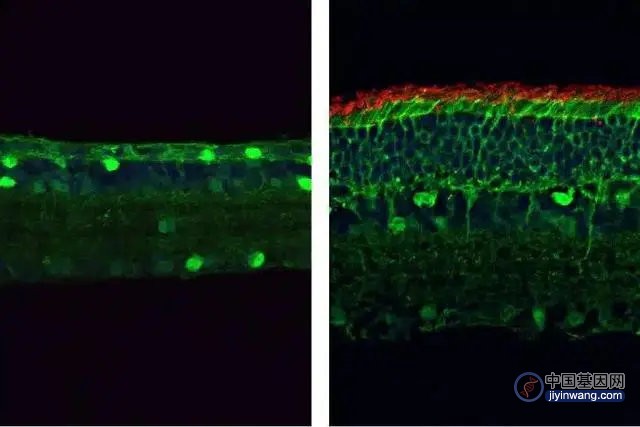
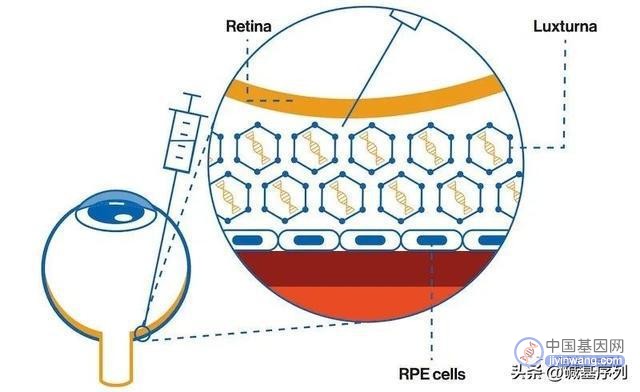
2018年:Spark公司利用腺相关病毒AAV作为载体将一种基因(RPE65)导入RPE65基因突变相关视网膜营养不良(一种罕见疾病)的患者的眼组织中,使其重获光明。
什么是基因治疗
我们都知道基因是我们遗传物质的基本功能单位。很多疾病都与基因缺陷有关,比如肿瘤、遗传病、某些高血压、某些心脏病等等。这类疾病尤其是遗传病的传统治疗手段主要通过不断用药对症状进行短暂控制,但无法在基因水平上根治疾病,因此亟待寻求一种新的治疗模式。
美国食品药物管理局( FDA) 对基因治疗( gene therapy) 的定义是“通过 各种手段修复缺陷基因,以实现减缓或者治愈疾病目的的技术”。也就是说,基因治疗主要指运用基因工程技术将“正常基因”导入细胞,以纠正或补偿因基因缺陷而引起的功能缺陷,从而治疗疾病。
1.怎么把“正常基因”导入呢?
在基因治疗过程中,我们需要将具有治疗作用的基因导入生物细胞中。因此根据治疗的方式和对象,我们需要选择一个合适的运输工具叫载体,它携带具有治疗作用的基因。目前常用的载体主要可以分为病毒类和非病毒类。
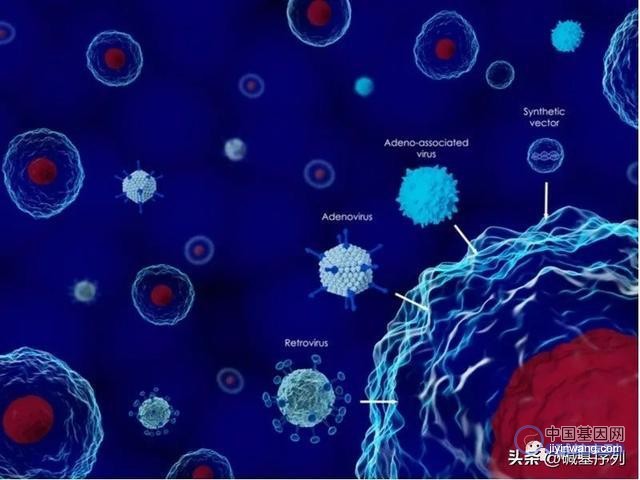
病毒载体:由于病毒对人体细胞的感染能力较强,我们改造病毒载体,除了病毒本身的致病作用,保留病毒在体内的复制功能。比如腺相关病毒( Adeno-associated virus,AAV) 、慢病毒 ( Lentivirus,LV) 、腺病毒( Adenovirus,AV) 以及逆转录病毒( Retrovirus,RV)
非病毒载体:脂质体、分子偶联受体以及其他新型材料如纳米技术材料等,相对病毒载体,其制备简单、无免疫原性、操作简单等。
2.“正常基因”导入哪些细胞呢?
精子、卵子或受精卵等生殖细胞,但是在伦理学方面受到较大的争议,所以在应用方面的限制较多。其他应用较多的细胞如成熟血细胞、脐带血造血干细胞、皮肤细胞、肝脏细胞、神经细胞、肌细胞、视网膜细胞等。
3.基因编辑技术是基因治疗的未来?
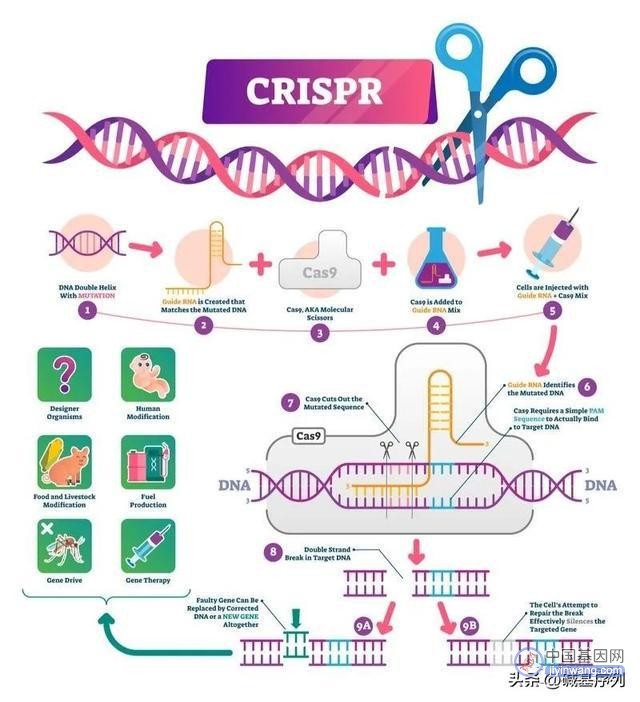
基因编辑是一种允许科学家改变生物体DNA的技术。这种生物技术,也被称为基因组编辑或DNA编辑,可以精准地在人类基因的某个位置进行添加、移除或改变等操作。其优点是更加精准和特异。但是目前也存在安全风险。
基因治疗哪些疾病
很多疾病的治疗处于临床实验阶段。比如血液系统单基因遗传病如血友病、地中海贫血、镰刀细胞性贫血等和其他系统遗传性疾病,如眼部疾病、免疫缺陷性疾病等。肿瘤疾病如神经胶质 瘤、肝癌、结肠癌、于头 颈部鳞癌、肺癌、鼻咽癌、黑色素瘤等。此外还有感染性疾病,神经系统性疾病、心血管系统疾病以及自身免疫性疾病。
疾病 基因 基因治疗公司
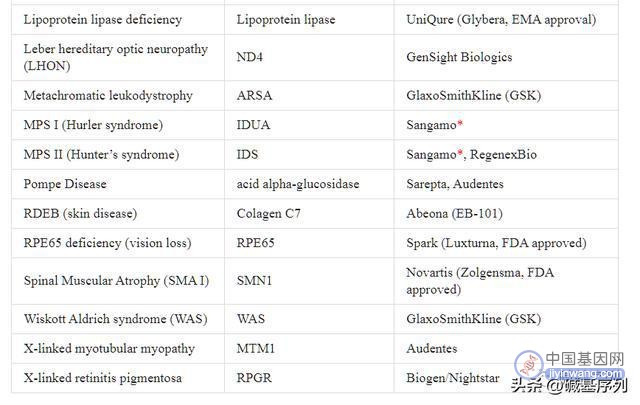
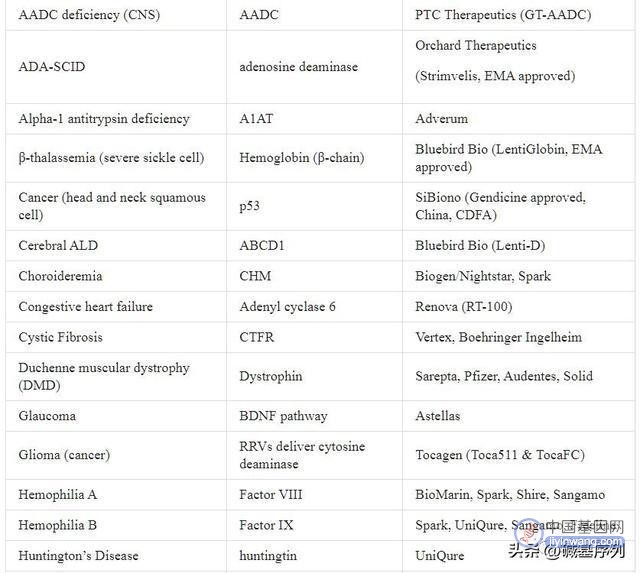
人没了,钱还在,悲催的是人在,钱没了,基因治疗费用如何,总之,相当的贵。
Zolgensma是一种治疗脊髓性肌萎缩症的基因疗法,于2019年获得美国FDA批准。诺华已经将这种疗法的价格定在每位患者210万美元(折合人民币多少??)。
Spark公司以每只眼睛425K美元的价格出售Luxturna(用于治疗视网膜营养不良的眼科疾病)。Luxturna基因疗法于2017年底获得批准。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。