双CRISPR-Cas3系统诱导多外显子跳跃,有望基因治疗大多数DMD患者

杜氏肌营养不良(DMD)是一种发病率相对较高的单基因疾病,由X染色体上编码肌营养不良蛋白(Dystrophin)的基因突变,导致无法产生足够的抗肌萎缩蛋白,患者的肌肉组织逐渐被脂肪和纤维化组织取代,大约每5000名新生男婴中就有1人患病。
近年来,已有几款治疗DMD的反义寡核苷酸(ASO)药物获批上市,通过外显子跳跃达到治疗目的,但这些药物只能覆盖少数特定突变位点的DMD患者。
2023年8月24日,日本京都大学的 Akitsu Hotta 团队在 Cell Press 旗下期刊 Stem Cell Reports 上发表了题为:Dual CRISPR-Cas3 system for inducing multi-exon skipping in DMD patient-derived iPSCs 的研究论文。
该研究开发了一种双重CRISPR-Cas3系统进行多外显子跳跃(MES),能够诱导杜氏肌营养不良(DMD)患者来源的诱导多能干细胞的肌营养不良蛋白(Dystrophin)基因外显子45-55区域的大片段缺失(~340kb),产生截短但仍有功能的肌营养不良蛋白,该方法能够覆盖60%以上的DMD患者。此外,该研究未发现明显的脱靶缺失。
这项研究表明,双CRISPR-Cas3系统是一种很有前景的工具,可通过多外显子跳跃(MES)诱导大片段基因组缺失,启发了治疗DMD和其他需要大量删除基因片段的遗传疾病的新方法。

由于影响肌营养不良蛋白基因的突变模式存在显著差异,因此,跳过或删除一小部分片段只适用于有限的DMD患者。例如,最常见的外显子51、53和45的单外显子跳跃分别适用于13%、8%和8%的DMD患者。
多外显子跳跃(MES)广泛适用于多种DMD突变模式。通过靶向肌营养不良蛋白基因的突变热点,研究人员估计外显子45-55的MES,能使60%以上的DMD患者受益。然而,很少有技术可以诱导如此大片段的基因删除,以覆盖分布在几百个碱基上的目标外显子。
为了克服这一障碍,研究团队使用CRISPR-Cas3在各种DMD突变模式的肌营养不良蛋白45-55外显子区域诱导了多达340kb的缺失。因为使用单个CRISPR RNA基本难以删除超过100bp,所以研团队在目标基因组区域内使用了一对CRISPR RNA。
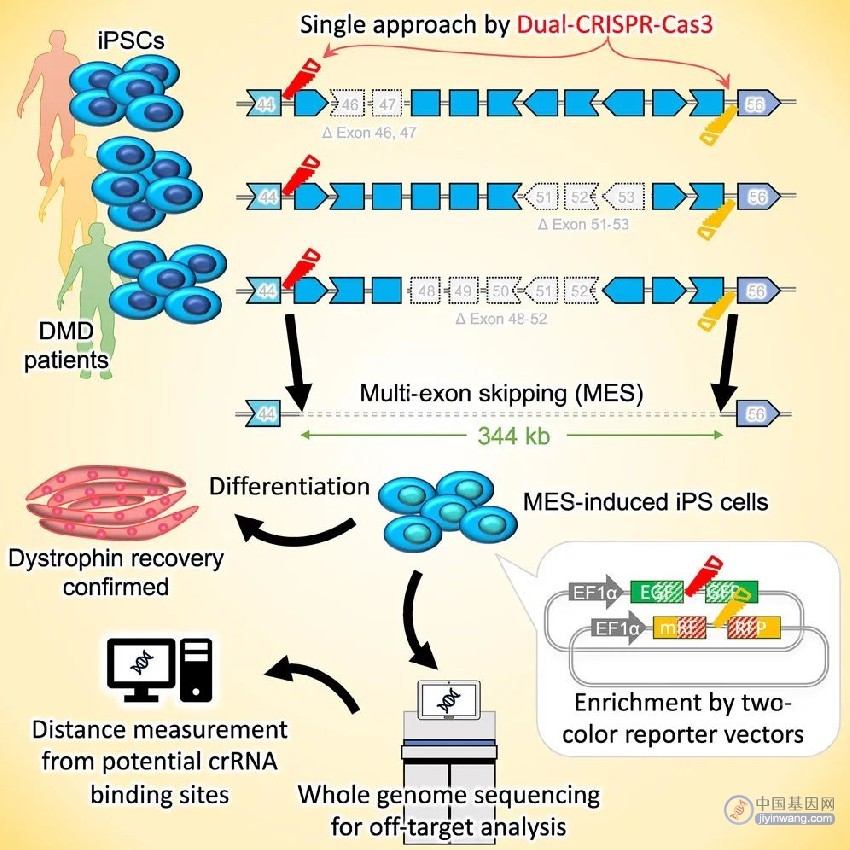
研究团队指出了这种双CRISPR RNA系统的潜在局限性。首先,删除模式存在变异,其精确起点和终点无法完全控制。当需要大量但精确删除时,这可能是一个缺点。其次,该研究没有证明肌营养不良蛋白功能的恢复情况。第三,还需要开发其他方法来提高Cas3系统的整体基因组编辑效率。
论文通讯作者 Akitsu Hotta 表示,双CRISPR-Cas3是一种很有前途的工具,可以通过多外显子跳跃诱导来实现基因删减。一旦能够将双CRISPR-Cas3系统安全有效地递送到体内骨骼肌组织中,就有望应用于未来的基因治疗。此外,诱导数百个DNA碱基缺失技术本身在基础研究中也具有广泛的适用性。希望这项研究能够启发治疗DMD和其他需要大量删除基因片段的遗传疾病的新方法。
论文链接:
https://www.cell.com/stem-cell-reports/fulltext/S2213-6711(23)00295-3
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。