基因工程改造细菌,让它们组成自杀小队,激活免疫系统对抗癌症
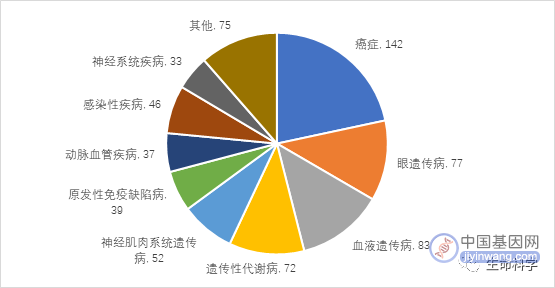
越来越多的研究表明,细菌是肿瘤微环境的一部分,肿瘤中特殊的低pH、坏死和免疫排斥等环境,能够支持一些细菌的生长,同时阻止免疫系统清除这些细菌。
这使得科学家们开始思考,是否可以通过基因工程改造这些细菌,让他们来发挥癌症治疗作用。
近日,哥伦比亚大学的研究人员在 Science 子刊 Science Advances 上发表了题为:Chemokines expressed by engineered bacteria recruit and orchestrate antitumor immunity 的研究论文。
该研究将癌症免疫学与基因工程相结合,将大肠杆菌改造成了靶向肿瘤的“细菌自杀小队”,这一小队由表达趋化因子CXCL16和CCL20的基因工程大肠杆菌组成,它们能够激活和招募先天性抗肿瘤免疫反应(由树突状细胞介导)和适应性抗肿瘤免疫反应(由T细胞介导),从而发挥更好、更安全的癌症免疫治疗效果。这项研究标志着利用非致病性细菌来对抗癌症的努力向前迈进了一大步。

肿瘤能够利用多种机制主动排斥参与抗肿瘤免疫的免疫细胞。而目前克服这些肿瘤排斥信号的策略仍然十分有限,也就难以针对性进行治疗。
近年来,合成生物学技术的进步,让我们可以通过基因工程改造细胞或其他微生物进行肿瘤局部药物递送。之前有研究人员在细菌中构建了一种同步裂解回路(Synchronized Lysis Circuit,SLC),这些细菌能够在肿瘤内定植,并在之后裂解,从而在肿瘤局部释放治疗药物,发挥癌症治疗作用。
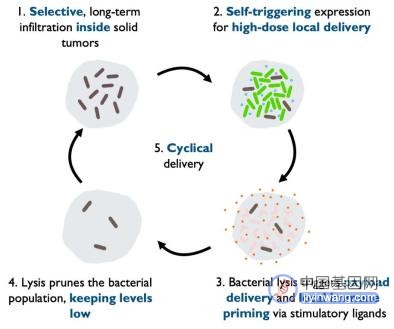
SLC工作原理
在这项最新研究中,研究团队将作为益生菌的大肠杆菌与同步裂解回路(SLC)相结合,设计了可在肿瘤内释放趋化因子(Chemokines)的基因工程大肠杆菌,以吸引适应性免疫细胞进入肿瘤中。
不同的趋化因子能够吸引不同类型的免疫细胞,并刺激它们做出特定反应。趋化因子CXCL16能够招募具有淋巴外归巢潜力的活化T细胞,CXCL16及其受体CXCR6在产生抗肿瘤免疫中起着关键作用,是一种有潜力的癌症治疗靶点。然而,目前还没有能够特异性地将CXCL16递送到肿瘤微环境以招募活化T细胞的方法。
在这项最新研究中,研究团队设计了表达人类趋化因子CXCL16激活突变体(hCXCL16K42A)的大肠杆菌,这一基因工程大肠杆菌在注射到小鼠体内后,会在肿瘤内定植,当在肿瘤内达到一定数量后,就会触发同步裂解回路(SLC),导致自身裂解,释放其中的内容物。进而招募CD8+T细胞,能够在多个肿瘤小鼠模型中激活抗肿瘤免疫反应。
为了进一步增强治疗效果,研究团队构建了表达另一种趋化因子CCL20的大肠杆菌,这一趋化因子能够激活常规1型树突状细胞,这些被激活的树突状细胞能够“吃掉”肿瘤细胞,并将这些肿瘤细胞的抗原呈递给T细胞,T细胞能够更好地识别出肿瘤细胞,从而发挥更好的肿瘤杀伤作用。
将表达两种趋化因子hCXCL16K42A和CCL20的基因工程大肠杆菌联合使用,可以招募参与肿瘤免疫反应启动和反应阶段的先天性免疫细胞(常规1型树突状细胞)和适应性免疫细胞(CD8+T细胞),从而增强整体抗肿瘤免疫反应,增强治疗效果。
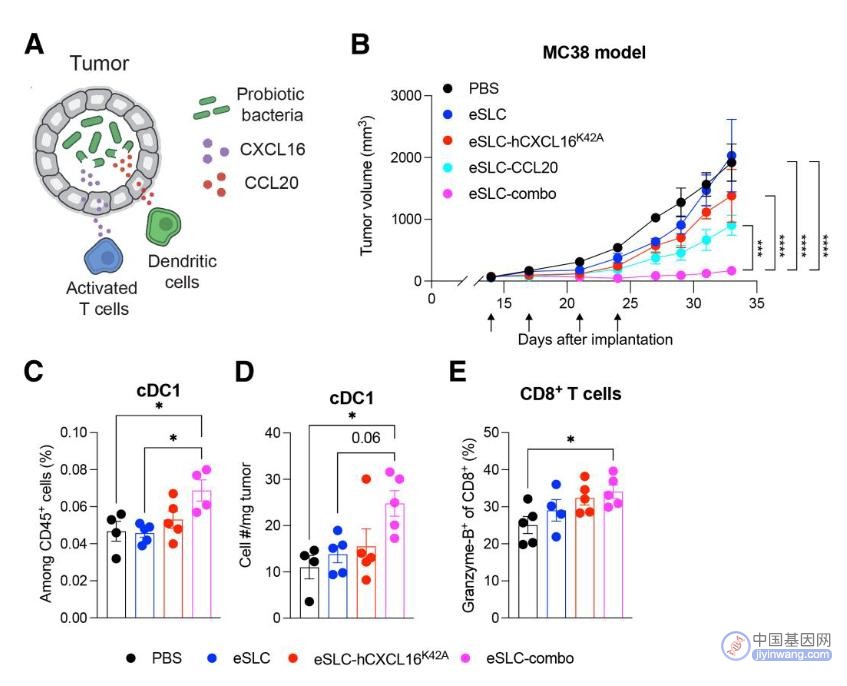
在癌症小鼠模型中,直接向肿瘤部位注射这些基因工程大肠杆菌,能够在注射部位肿瘤以及没有注射的远端肿瘤诱导强大的抗肿瘤免疫反应,此外,通过静脉注射同样有效。由于这些细菌只在肿瘤环境中定植,而且只有达到足够数量才会在肿瘤内裂解,因此,健康器官和组织中并没有检测到这些细菌的定植。
总的来说,该研究设计了表达趋化因子的大肠杆菌来激活和招募先天性抗肿瘤免疫反应和适应性抗肿瘤免疫反应,提供了一种癌症免疫治疗新策略。
研究团队表示,将继续对这一系统修补和优化,为后续临床试验奠定基础。研究团队也将这种方法申请了专利,并授权给了GenCirq公司进行后续商业化开发。

论文链接:
https://www.science.org/doi/10.1126/sciadv.adc9436
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。