2023年,10多款细胞和基因疗法有望获批上市!
美国FDA在几年前曾预计,“到2025年,FDA每年将批准10-20款细胞和基因疗法。”麦肯锡近期的一份报告则基于管线进展做出更大胆的预测:“仅在2024年,预计将有多达21种细胞疗法和多达31种基因疗法获得FDA批准。”
这些预言能否实现?“这只是即将到来的浪潮的第一波。”美国再生医学联盟(Alliance for Regenerative Medicine,ARM)首席执行官Timothy Hunt先生在年初发表的一则观点文章对此十分乐观。近5年来,获得FDA批准的细胞和基因疗法数量持续增长,2022年也是全球细胞和基因疗法获批总数创纪录的一年。当前这一领域还有超过2000项临床试验正在开展,其中超过100项已迈入3期。根据公开信息,在可预见的2023年,就有多达16款全新的细胞或基因疗法有望在全球首次获批。
与此同时,推动细胞和基因疗法成为主流的治疗方式,行业也仍有诸多挑战仍需解决。通向下一代细胞与基因疗法之路,哪些前沿突破有望引领风向?

在即将播出的“2023年药明康德全球论坛线上版”中,细胞和基因疗法领域多家新锐公司的CEO共话这一领域的治疗范式更迭,探讨使其更精准、更有效、更安全的变革性技术。这些嘉宾所在的公司均在近期获得早期高额融资,致力于打造多种独特的创新技术来开发下一代细胞和基因疗法。长按扫描文末二维码,即可申请观看。
2023年全球16款细胞或基因疗法有望获批或迎来重要监管进展
根据已公开信息及ARM预测信息,至2023年末,全球范围内将有16款细胞或基因疗法有望首次获批上市或迎来重要监管进展:
从疗法类型来看,包括7款基因疗法、1款基因编辑疗法、3款CAR-T细胞疗法、1款 TCR-T细胞疗法、2款干细胞疗法、1款TIL疗法和1款同种异体细胞疗法。
在适应症方面,这些候选基因疗法 中一半针对血液系统遗传疾病,CAR-T疗法则集中在血液肿瘤领域。
就监管进展而言,目前1款疗法已在日本获批,5款疗法已公开明确PDUFA日期或EMA审评结果预期公布时间,2款疗法 的 上市申请已 被 欧 美监管机构接受 ,3款CAR-T疗法的 上 市申请 已获得中国国家药监局(NMPA)受理并被纳入优先审评,还有5款疗法 已 向欧美监管 机构 递 交上市申请或明确推进上市计划。
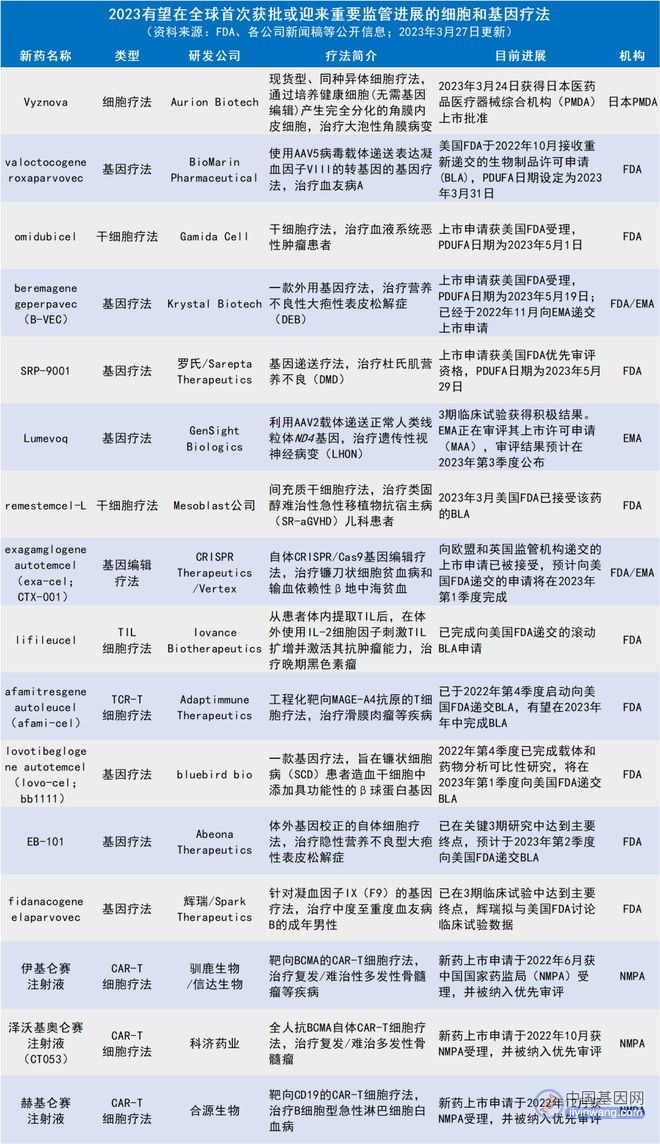
▲2023有望在全球首次获批或迎来重要监管进展的细胞和基因疗法
下一代细胞和基因疗法有哪些特征?
在管线蓬勃发展之际,开拓者已将目光投向更尖端的技术,以推动进一步释放细胞和基因疗法的潜力。
旨在“一次治疗、永久治愈”,疗效持久性是一款疗法必经的考验。事实上,自然界的基因调控核心机制中,就蕴含持久治疗的奥义。表观遗传学可谓基因表达的“天然守门员”,通过DNA的甲基化修饰来改变染色质,可以在不改变DNA序列的情况下控制基因表达并驱动细胞功能的持久变化。Chroma Medicine公司的目标正是高效模拟这一天然系统,并建立模块化的灵活平台,来精确、持久地控制基因表达。这一平台技术有潜力应用于多种疾病中,无论是否需要同时沉默、激活或靶向多个基因。相比当前通过切割DNA来间接调控基因表达的方法,模拟表观遗传学的技术得以避免激活不可预测的DNA修复途径,以及可能产生的免疫原性截断或突变蛋白。
精准性也是备受关注的疗法更迭方向。先导编辑(prime editing)无疑是精准编辑技术中的翘楚之一。先导编辑采用“搜索-替换”策略,从而大幅减少编辑位点副产物和脱靶效应,也不会导致DNA断裂。除此之外,这一策略可以在人类基因组中的几乎任何位置进行不同的序列编辑,可以纠正所有12种类型的单碱基对点突变,可应用于多种细胞和器官类型,理论上可以解决约90%的已知致病突变。由基因编辑领域先驱刘如谦博士于2021年联合创建的Prime Medicine公司,就以“先导编辑”为核心技术,致力于塑造基因疗法的未来,为患者带来终生获益。
在细胞疗法中,针对CAR结构的全新改造和设计,也有望让CAR-T更准确区分癌细胞和健康细胞。相比普通的CAR只向T细胞插入单个转基因、使用一种蛋白质来识别癌细胞,一些科学家试图让免疫细胞像计算机一样“智能”,识别并判断肿瘤的多个特征。ArsenalBio公司就致力于开发这样的多功能CAR-T细胞药物。一方面,在不依靠病毒载体的情况下,通过精准的CRISPR基因编辑将更大型的DNA片段精确插入到免疫细胞的基因组中,这些大型DNA片段就像广泛的“软件”指令集,让免疫细胞有效靶向实体瘤和血液癌症;同时,结合逻辑门控(使CAR-T只在复杂的情况下才被精准激活)改善肿瘤靶向功能。
药物递送仍然是一个绕不开的重大挑战。尤其是随着基因编辑工具的发展,递送的重要性愈发凸显。将疗法更有针对性地递送到目标组织或细胞,非病毒递送系统是一个趋势。Capstan Therapeutics是该领域的新秀之一,致力于通过mRNA递送技术来变革细胞疗法。其专有的靶向脂质纳米颗粒(tLNP)技术能够介导细胞种类特异性的吸收,通过设计疾病特异性的mRNA并将其递送到体内细胞中,可以实现在体内递送CAR至特定免疫细胞并生成CAR-T细胞,从而消灭疾病细胞,这项技术获得多家大型药企的投资。此外,此平台亦可通过递送mRNA编码的基因编辑系统至致病细胞中,借由编辑细胞内DNA来治疗遗传性疾病。
凭借独特技术来解决当前初代疗法所普遍面临的挑战,上述多家新锐公司的CEO均出席2023年药明康德全球论坛并深入探讨多样化的解决方案。
创变不息
说回FDA对于细胞和基因疗法的预测,行业正在大步迈向这一目标。而更令人振奋的是,科学将不断实现自我跨越,技术将持续向前飞跃,为这股浪潮注入源源不断的动力。
即刻报名,聆听产业先锋的洞见,共同畅想细胞和基因疗法的广阔天地!2023药明康德全球论坛汇聚30多位行业大咖,以“BOLD”为主题,还有多场专题将探讨成药性、RNA疗法等行业关注的重要议题。
致力于汇聚智慧、推动合作、加速为患者带来突破,药明康德全球论坛在过去十年中已经成为把脉行业发展的风向标。2023年将是充满挑战和机遇的一年,我们向勇敢创新者们致以敬意,相信行业领袖与先锋的前瞻观点,将为我们指明前行的方向。

▲本次论坛实行“邀请批准制”,不收取任何参会费用。为满足全球不同地区的观看需求,将分设中英版本及多个适宜的播出时间。长按识别上方二维码申请观看。完整议程请见下图。
参考资料:
[1] Statement from FDA Commissioner Scott Gottlieb, M.D. and Peter Marks, M.D., Ph.D., Director of the Center for Biologics Evaluation and Research on new policies to advance development of safe and effective cell and gene therapies. Retrieved March 22, 2023 from https://www.fda.gov/news-events/press-announcements/statement-fda-commissioner-scott-gottlieb-md-and-peter-marks-md-phd-director-center-biologics
[2] Eight imperatives for launching cell and gene therapies. Retrieved March 22, 2023 from https://www.mckinsey.com/industries/life-sciences/our-insights/eight-imperatives-for-launching-cell-and-gene-therapies
[3] The Cell And Gene Therapy Sector In 2023: A Wave Is Coming – Are We Ready?. Retrieved March 22, 2023 from https://invivo.pharmaintelligence.informa.com/IV146781/The-Cell-And-Gene-Therapy-Sector-In-2023-A-Wave-Is-Coming--Are-We-Ready
[4] ASGCT Clinical Trials Finder. Retrieved March 24, 2023 from https://asgct.careboxhealth.com/
[5] Approved Cellular and Gene Therapy Products. Retrieved March 22, 2023 from https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。