肿瘤的体内基因免疫治疗,体内免疫细胞治疗的工程化
癌症不仅来源于基因突变,同时也与患者免疫系统功能下降息息相关。免疫检查点抑制剂(ICIs),溶瘤病毒(OVs)和嵌合抗原受体(CAR) -T细胞等肿瘤免疫疗法在近10年来蓬勃发展,与此同时,核酸药物也在成药性方面实现了巨大突破,如RNAi和mRNA药物的获批和临床使用。基于前述二者的开发经验,基因免疫疗法应运而生。基因免疫疗法是指通过递送外源基因或调节内源基因表达,直接在体内调控免疫反应来对抗癌症的治疗方法。针对人体免疫系统,可以使用病毒载体和mRNA来递送治疗基因,如CARs,帮助免疫细胞重新锁定肿瘤细胞(图1)。针对肿瘤细胞,则可使用OVs或纳米颗粒包裹的mRNA来递送免疫调节基因,或是使用RNAi下调肿瘤免疫抑制因子的表达(图1)。
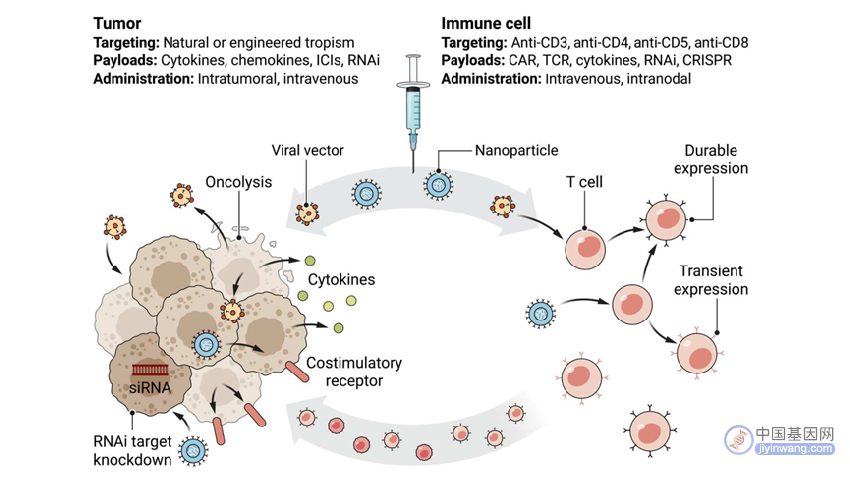
图1. 体内基因免疫疗法:工程化免疫细胞或调节肿瘤细胞的免疫特性
免疫治疗在本质上可以分为分子疗法或细胞疗法。分子免疫疗法主要是针对CTLA-4、PD-1/ PD-L1、LAG-3的免疫检查点抑制剂,如获得2018年诺贝尔医药奖的CTLA-4阻断抗体伊匹单抗。而目前的研究重点正在转向细胞免疫疗法和精确医学方法,即在体外以某种形式向免疫细胞中导入转基因从而操作免疫细胞的特性或行为 (图2)。然而,体外操作需要专业的设备和训练有素的人员,并且涉及到繁琐的质控、运输等配套措施,并且对生产条件的精确控制有着非常严格的要求,一些研究指出,为了驱动细胞的扩增所进行的长时间体外培养过程和激活步骤,也会导致免疫细胞的逐步分化并降低细胞产品的功能效应。因此,直接在体内进行治疗细胞的工程化改造,可能有利于产生分化程度较低而功能更强的细胞产品。
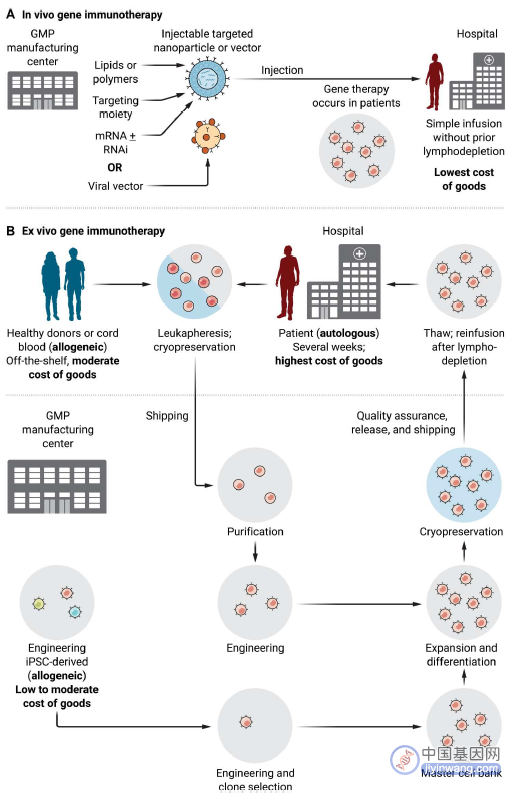
图2. 免疫细胞疗法的体内和体外工作流程的比较
01
体内免疫细胞治疗的工程化
1.1 免疫细胞工程化的目标
免疫细胞工程化的主要重点包括重定向抗原特异性,表型重编程,减轻转移细胞和受体免疫系统之间的对抗性相互作用。治疗癌症的一个主要挑战是缺乏免疫细胞对抗癌细胞。此外,癌症的一个主要免疫逃避途径是下调主要组织相容性复合体(MHC)的表达,这是T 细胞的 TCR 识别抗原所必需的。增加内源性免疫细胞参与抗肿瘤的有效方法就是以不依赖于 MHC 的方式赋予它们特异性识别肿瘤抗原的新受体,如嵌合抗原受体(CARs)。
细胞免疫治疗还面临的挑战在于慢性激活信号转导或肿瘤介导的抗炎重编程,导致的免疫细胞终末分化和功能衰退。因此,一种策略是调节支持促炎表型的细胞因子,维持 T 细胞的记忆表型和干性。
目前免疫细胞疗法使用的细胞是患者体内的,然而,使用异体细胞作为工作细胞可能前景更加光明。一些免疫细胞,如NK细胞,或许更适合这种方法。因为它们在对抗性移植物和宿主反应 (如移植物抗宿主病) 中的作用有限,而且它们在 KIR 错配环境中具有更大的活性。利用基因编辑技术减少移植物和宿主的之间不利的相互作用,并不一定与体内的工程化方法相关,但可以作为简化细胞疗法的流程,并通过启用异体基因转移帮助扩大细胞免疫治疗对更多潜在患者的可及性。与此同时,目前在体内对免疫细胞进行功能性重编程的方法,主要是利用靶向病毒载体进行基因的永久编辑或靶向型纳米粒进行基因的瞬时干扰 (图1)。
1.2 靶向型病毒载体
抗原特异性重定向 T 细胞的体外方法依赖于水泡性口炎病毒 (VSV) G 蛋白的假型慢病毒 (LV) 或 γ-逆转录病毒来转导 CAR、TCR 或类似的外源性受体。体内方法是利用工程化病毒在体内进行转导。在慢病毒系统中,可以通过副粘病毒或阿尔法病毒的假病毒化来实现体内转导,因为它们的受体结合和膜融合域是分离的,可将受体结合部分替换为指定的靶向配体。Buchholz 团队是率先证明这一点的研究小组之一,他们使用 CD8 靶向的 LV,使用 CD8α 链引导 LVs 进入 T 细胞,递送识别黑素瘤抗原酪氨酸酶的 TCR。针对 CD4 和 CD8 T 细胞亚群开发靶向性 LV 的进一步工作,也证明了在体内形成 CD19-CAR-T 的可能性。通过系统性注射 CD8-LVs,Buchholz 团队能够在移植了人外周血单个核细胞的小鼠中,检测到特异性的人 CD8+ CAR-T 细胞,并有效消除异种移植的 CD19+ Raji 癌细胞。此外,使用 CD19+ Nalm6 白血病模型,他们证明了体内转导的 CAR+ 细胞可以取得有效的肿瘤控制。值得注意的是,CAR+ 细胞群体除了 T 细胞外,还包括 NK 细胞和 NKT 细胞,而这些细胞也可能带来与这些细胞类型功能相关的治疗效益。在这些研究中,从血液、脾脏和骨髓中获得的 CD8+ T 细胞 CAR 阳性率可达 15%以上,尽管这与体外临床前转导效率相比而言是很低的,但与患者细胞中的临床转导效率相比则是较高的。
1.3 具有靶向性的生物材料
纳米颗粒(NPs)是指直径小于 1 μm、由有机分子或金属元素及其化合物构成的微小颗粒。NPs 可以作为 mRNA、RNAi 或基因组编辑组分等成分的递送载体,以一种瞬时性或永久性的方式参与体内治疗过程 (图1)。脂质 NPs (LNPs) 可以作为多种核酸的多功能载体。Rurik 等人通过在 LNP连接上靶向 CD5 的分子组分设计了靶向型 LNP (tLNPs),然后成功用编码成纤维细胞激活蛋白 (FAP) 靶向 CAR (FAP-CAR) 的 mRNA 转导了内源性 T 细胞。然而,tLNPs 的一个潜在限制是表达峰值相对较早且表达时间较短。对于心脏纤维化这种疾病模型而言,tLNP 的瞬时表达特征可能是有效且可取的,而用于治疗癌症仍面临着更多的挑战。考虑到 tLNP 的模块化特性,tLNPs 可以用于递送肿瘤特异性的 CARs,从而作为一种潜在的“现货型”短程癌症基因免疫疗法,并且具有多次给药的能力。聚合物 NPs 已被证明可递送抗原特异性受体 mRNA 或 DNA 编码的基因组整合机器,分别用于在体内产生瞬时性的或永久性的抗原特异性 T 细胞。
02
肿瘤的治疗性基因调节
1993年,G. J. Nabel 等人开展了人类历史上首次癌症体内基因治疗试验,他们利用脂质体 DNA 将人类白细胞抗原 (HLA) -B7 引入到 HLA-B7 阴性的黑色素瘤患者的病变组织中。然而免疫疗法只需实现细胞质递送而不需要核递送。由于将核酸递送到肿瘤的不同治疗方法的出现和进展,对武装OVs的临床研究比对 RNAi 的更为活跃,反过来,对 RNAi 的临床研究也多于对 mRNA 的临床研究 (图3A)。
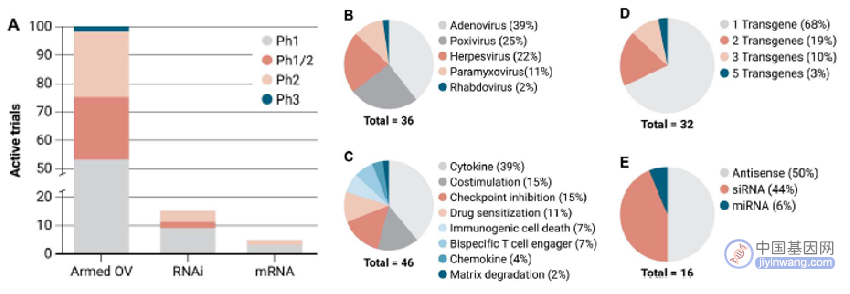
图3. 肿瘤靶向型基因免疫治疗策略的临床概况
2.1 溶瘤病毒(Oncolytic viruses)
癌症可强行启动细胞周期并使细胞凋亡失效,因此细胞成为了病毒的理想宿主,癌细胞被病毒感染的机率也大大增强。自19世纪80年代以来,已经有人观察到与病毒感染相关的自发的肿瘤消退。最近有报告称,严重急性呼吸综合征冠状病毒 2型(SARS-Cov-2)感染导致的癌症患者病情缓解 (59例)。
病毒感染的抗肿瘤作用主要是由宿主的免疫反应驱动的,包括病毒和肿瘤特异性成分。肿瘤细胞的病毒感染导致免疫原性细胞死亡,释放损伤和病原体相关的分子模式 (分别为 DAMPs 和 PAMPs),刺激宿主的模式识别受体。这些信号通路的激活会导致促炎细胞因子和趋化因子的产生。因此,病毒感染可以刺激免疫细胞的进入和树突状细胞(DCs)的成熟,从而诱导免疫反应,以应对死亡细胞中存在的内源性 (如肿瘤相关) 或外源性 (如病毒) 的抗原。显然,后者参与了被病毒感染的肿瘤的清除,但只有前者可以介导未感染的远端转移位点的异位效应。OV 领域一直致力于利用病毒的抗肿瘤特性,同时通过基因工程化控制病毒对肿瘤的限制性复制或转基因表达,从而最大限度地降低抗肿瘤病毒对健康组织的损伤风险。尽管大多数 OV 在肿瘤中都保留着复制能力,但非复制性 OV 如 aglatimagene besadenovec (CAN-2409) 也在研发之中,其使用单纯疱疹病毒胸苷激酶实现基因介导的细胞毒性免疫治疗。
2.2 OV 疗法的现状和挑战
目前,已经有一种 OV 疗法(Oncorine)在中国获批,但在美国和欧洲只有一种表达粒细胞-巨噬细胞集落刺激因子 (GM-CSF) 的武装型 OV talimogene laherparepvec (IMLYGIC) 获批。此外,在正在进行的50 个 OV 临床试验中,其中 36个 (72%) 至少添加了一种免疫调节性转基因,这表明 OVs 的首选用途是基因免疫治疗。目前有超过 100个 OVs 的临床试验正在进行中 (图3A):这些 OVs 必须具有额外的转基因编码能力和遗传稳定性,其中 31种 (86%) 使用来自腺病毒、痘病毒或疱疹病毒家族的遗传稳定的 DNA 病毒,其余 5种 (14%) 则使用遗传稳定的 RNA 病毒 (图3B)。细胞因子,包括 GM-CSF,IL-2, IL-7, IL-12, IFN 和 TNF-α,以及这些细胞因子的各种组合,是最常见的 OV 货物。而共刺激分子如 CD40L、ICIs 和药物增敏剂,则占了 OVs 临床试验的 10% 以上 (图3C)。另外,不常见的选择包括双特异性 T 细胞接合物和用于降解肿瘤的细胞外基质的酶类。总之,三分之一以上的 OVs 表达一个以上的转基因 (图3D)。
OVs 方向面临的挑战包括患者内部和患者之间在病毒进入受体或激活肿瘤特异性启动子所需因子的表达上的可变性,以及中和抗体和先天免疫反应的作用。如果固有免疫反应,如 IFN 信号或 NK 细胞反应过快,那么 OVs 的潜在治疗效益可能会被减弱。虽然模式识别受体途径和 NK 细胞的抑制剂改善和延长了 OV 复制,但有效诱导适应性免疫仍然需要固有免疫途径的激活。因此,OVs 面临的一个重要挑战是在逃逸固有免疫系统和刺激固有免疫系统找到一个最佳的平衡。
2.3 OV的进展
最近的一项研究表明,OV 编码的 RNAi 可以抑制染色质重塑因子腺嘌呤-胸腺嘧啶-富含相互作用结构域的蛋白1A (ARID1A),而该蛋白参与了细胞固有的抗病毒途径。由于 OV 编码的 RNAi 分子可以天然地进入到 OV 从宿主肿瘤细胞中芽出产生的胞外囊泡中,这些囊泡就可将 RNAi 分子转移到邻近的细胞中,通常增强了肿瘤对病毒感染的许可性。此外,在 EZH2 增强剂存在的情况下,ARID1A 敲低使肿瘤细胞对合成致死的敏感性增加。最后,为了提高抗肿瘤免疫能力,另一种策略是给 OVs 装备个性化的新抗原表位,从而受益于 OVs 所赋予的免疫原性和肿瘤微环境修饰,并通过异源使用 OV 平台来避免中和抗体的阻断并扩展病毒的趋向性。总之,这些新方面可能会让 OVs 成为基因免疫治疗的基石之一。
2.4 肿瘤导向的 mRNA 基因免疫治疗
相对于 OVs, mRNA 基因免疫治疗具有明显的优势,但其依赖于 NPs 进行传递,目前只有 5项活跃的临床研究 (图3A),并且迄今为止尚无临床试验数据发表。基于 mRNA 的治疗,可以避免人体内部的中和抗体干扰,而且其在肿瘤微环境的非转化细胞中调节基因表达方面具有相当好的灵活性。最近的研究表明,mRNA 平台发挥效用的一个重要方面,是细胞因子和共刺激分子的瘤内传递,而其中 IL-12 和 OX40 配体 (OX40L) 则是最受重视的候选分子。最近的多项研究显示,使用 LNP 封装的 IL-12 mRNA 在各种肿瘤模型中都取得了良好的抗肿瘤效果,这促使临床试验将其作为单一疗法、与 ICI 联合使用,或作为几种 mRNA 混合物的一部分 (NCT03946800 和 NCT03871348)。其他正在探索的 mRNA 技术的有效载荷组合包括 IL-23、IL-36γ 和 OX40L,它们在临床试验中作为单一治疗和联合治疗 (NCT03739931),在临床前研究中显示了疗效;单链 IL-12、IFN-α、GM-CSF 和 IL-15-sushi-结构域作为单一疗法或联合疗法(NCT03871348);和 OX40L、CD80 和 CD86 的结合,也显示出一定的临床前治疗前景,但目前还没有进行临床研究。
2.5 RNA干扰(RNAi)
2.5.1 RNAi 的形式和作用机制
RNAi 是使用非编码核酸在转录后水平上调节基因表达的一种分子生物学机制,siRNA 和 shRNA 则是利用细胞内源性 microRNA (miRNA) 机制的两种技术。细胞内的双链 RNA 特异性核糖核酸内切酶 (DICER) 会处理它们,并与 RNA 诱导沉默复合体 (RISC) 和 Argonaute 2 结合进而介导 mRNA 的翻译抑制。miRNAs 可以通过其“种子序列”同时调节多个基因的表达:对于完美匹配的 mRNA 则会被降解;对于不完美匹配的 mRNA,则会隔离 mRNA 并阻碍其翻译。双功能 shRNA 可以利用 miRNA 的切割和隔离依赖通路,导致对靶蛋白表达的影响更快速和更持久,同时比 miRNA 更具有靶向性。反义寡核苷酸 (ASOs) 是被发现的第一种不同于 miRNA 途径的 RNAi 形式。
2.5.2 RNAi 相关癌症疗法
到目前为止,美国和欧洲监管机构已经批准了 6种适合全身给药的 ASOs和 4种 siRNA 疗法,用于治疗各种罕见疾病。相比之下,尽管目前有 33种用于治疗癌症的 RNAi 候选药物进入临床试验,但均未达到 3期阶段,并且其中15种已终止临床试验,其中有11种(包括 5个ASOs和 6个siRNA) 因缺乏疗效而遭放弃;其他 4项研究因未披露的原因而被暂停或放弃,包括一种双功能 shRNA,一种抗 miR 疗法,以及负载肿瘤抗原的树突状细胞候选细胞和靶向免疫蛋白酶体或 PD-L1 和 PD-L2 的 siRNA。在仍处于活跃状态的 18种RNAi药物中,9个靶向肿瘤驱动因子、致癌信号通路或凋亡抵抗途径和 9个靶向因子具有主要或至少显著的免疫抑制作用。免疫治疗性 RNAi 候选药物正在 16个临床试验中进行研究(图3A),其中 8个(50%) 是 ASO 疗法,7个 (44%) 是 siRNA 候选药物,1个(6%) 是 miRNA 候选药物(图3E),反映了这些 RNAi 平台的相对成熟度。
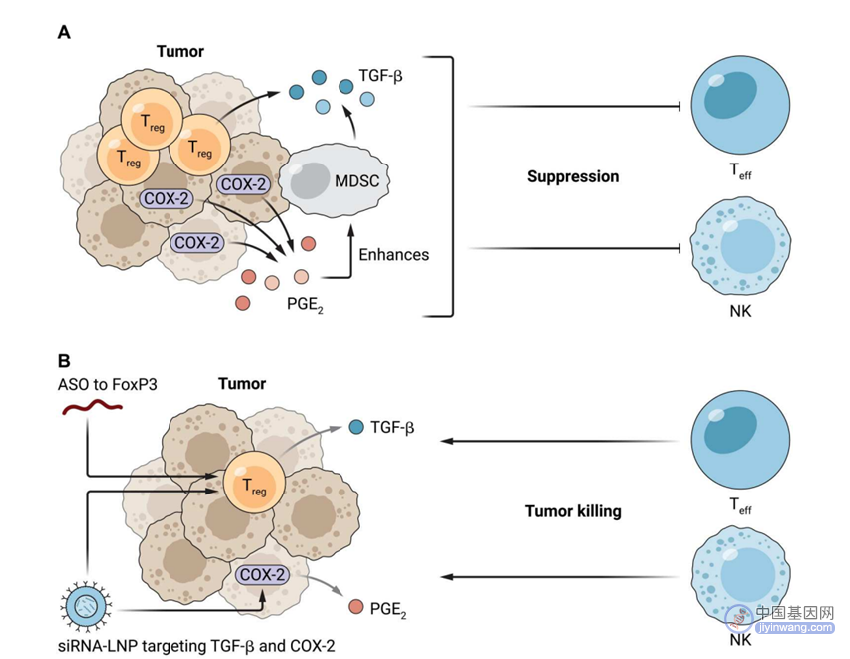
图4. 免疫治疗性RNAi可作用于多种细胞类型,对肿瘤微环境进行有利的修饰
2.5.3 改进 RNAi
与将 RNA递送到到免疫细胞相比,使用 NPs 将 RNA 递送到实体肿瘤面临明显挑战碍。幸运的是,实体肿瘤血管系统的改变导致的渗透性改变和留存效应,增强了ASOs 和 NPs 中封装的 RNA 载荷的传递。包含可电离脂质的 NPs 在肿瘤通过 Warburg 代谢产生的酸性微环境中会带上电荷,赋予NPs更高的细胞穿透潜能。此外,通过控制 NP 的大小、形状和电荷,并通过聚乙二醇 (PEG) 分子或肿瘤受体配体的表面修饰,可以合理设计 RNA-NP 配方,以达到低免疫原性、最佳 PK 和靶向递送的目的。因为一些 NP 修饰,如聚乙二醇化,可以提高血清半衰期,但降低穿透性,最近的 NPs 被设计成允许肿瘤微环境中过表达的 MMP 从聚乙二醇化的 NPs 中分离 PEG,并暴露其细胞穿透肽,从而增强肿瘤细胞的递送。
03
展望
对于肿瘤的基因免疫治疗,将 RNAi、mRNA 和基因编辑技术,与免疫细胞及靶向递送技术进行结合,有望实现最佳安全性和疗效。这将使我们可以武装多种免疫细胞 (如 T 细胞、NK 细胞、NKT 细胞和巨噬细胞) 来对抗患者体内的癌细胞,同时也可以帮助我们改造肿瘤微环境以促进工程化免疫细胞浸润。此外,OVs的研究与优化,也扩展了其肿瘤嗜性和靶向性,有助于在治疗持久性与免疫刺激之间保持平衡,以帮助机体更好的对抗肿瘤细胞。
参考文献:Mai et al., Sci. Transl. Med. 14, eabo3603 (2022) 9 November 2022
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。