EV装载mRNA蛋白质替代疗法:全新递送方法打开基因疗法大门
思珀生物是一家致力于研究细胞外囊泡装载mRNA蛋白质疗法的新的生物技术公司,与其合作的研究人员开发了一种新型信使RNA(mRNA)递送系统,用于光老化皮肤中的胶原蛋白补充疗法,这是第一个被证明这种能力的药物治疗方式。近日,思珀生物创始人Andrew Lee博士和李利博士的团队在国际学术期刊Nature子刊Nature Biomedical Engineering(影响因子:29.2)发表了题为《真皮内递送细胞外囊泡包裹的mRNA用于胶原替代治疗》(Intradermally delivered mRNA-encapsulating extracellular vesicles for collagen-replacement therapy)的文章。文章中所应用的这种新的递送系统,具有能够帮助mRNA和基因疗法克服目前面临的多种障碍的潜质。
30岁后,由于相关基因表达随着年龄的增长而下调,人体皮肤每年都会有约1%的胶原蛋白流失。衰老导致的胶原蛋白流失无可替代,脸、手、脖子和其他身体部位就这样形成了衰老所直接导致的皱纹。近些年来,胶原蛋白相关产品在相关衰老领域得到了广泛应用,也诞生了多个爆款产品。胶原蛋白的高效递送和长期稳定表达对于其功效有着至关重要的作用,相关的技术突破对于进一步缓解衰老意义巨大。
文章中显示,为解决皮肤中因衰老带来的胶原蛋白流失,相关团队开创了崭新的基于非病毒载体技术且可重复给药的基因治疗平台,使用细胞外囊泡(EV) 将编码胶原蛋白的mRNA 递送到皮肤细胞中,mRNA在细胞中可编码表达出相应的蛋白,从而发挥作用。这种细胞衍生的mRNA疗法,能够使皮肤细胞上调天然胶原蛋白的表达,弥补因衰老/光老化而造成的胶原蛋白流失,大大改善皱纹等衰老症状。
实际上,这一“梦幻般”的技术已接近现实,Andrew Lee博士,李利博士和倪佳博士所在的思珀生物正在完善此基因疗法,有望在胶原蛋白流失患者身上实现首个临床应用。
据介绍,思珀生物系全球第一家专注于开发细胞衍生的mRNA创新疗法与相关递送工具的公司。公司基于自主创新研发及与全球领先医疗机构及高等院校的合作,开发了非合成的、可量产且具有临床价值导向的细胞衍生的mRNA疗法,为下一代基因治疗方法提供了新的可能方向。目前,公司针对衰老相关胶原蛋白损伤的创新研发管线COL1A1-EV mRNA已获得了首个人体临床试验的伦理批件,有望于2023年夏天开始首批受试者的给药。思珀生物也将成为全球范围内首家在人体内测试可重复给药的非病毒基因治疗产品的生物医药企业。
创新基因治疗手段“逆转老化”
思珀生物“细胞衍生的RNA疗法”基于替代人体内与衰老相关的蛋白质损失的原理,将编码这些随着衰老而下调的蛋白质的 mRNA 输送到细胞内,通过人体自身的细胞来弥补因衰老/光老化而造成的损失。
这也决定了mRNA药物需要进入细胞质内才能发挥作用,如何将mRNA高效且特异性地递送至细胞内成为疗法生效的关键。
对此,思珀生物创造性地选择了细胞外囊泡(EV)作为mRNA递送的“运输工具”。细胞外囊泡作为一种自然存在的细胞间信使系统,存在于所有组织和生物体液中,可以将蛋白、核酸等活性成分有针对性地释放到各种组织。
更值得一提的是,基于具备自主知识产权的细胞衍生mRNA技术平台,思珀生物可通过细胞直接生产出包裹在细胞外囊泡中的mRNA药物,相关药物也表现出更为可靠的安全性、更强的溶酶体逃逸能力和更出色的生物膜透过性。该技术具有广泛的实用性,适用于绝大部分基因(无论基因大小),且经过思珀生物改造的细胞外囊泡具有高度的组织特异性靶向能力,可靶向给药至特定器官,提供了一种天然、安全、高效的创新基因疗法。
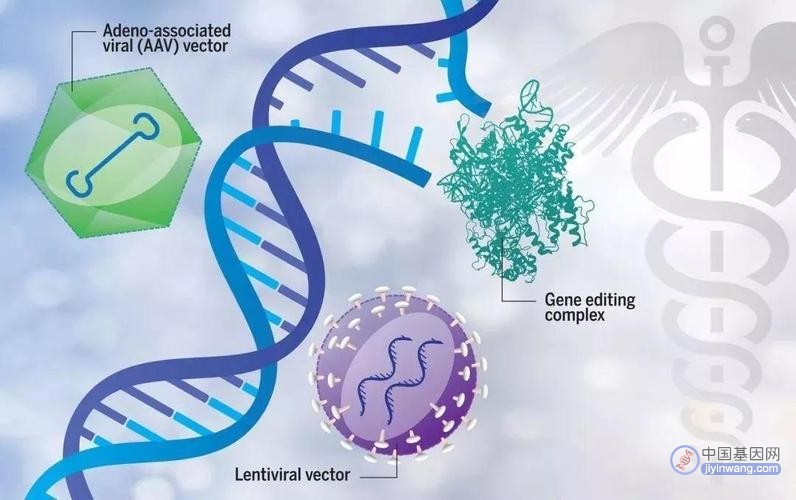
反观以腺相关病毒(AAV)为主的病毒类载体递送目标基因的相对常见的基因疗法,则在免疫原性、毒性或基因整合层面存在较为显著的风险,这也导致过去数年间相关药物临床试验多以失败告终。另外,由于AAV体积过小,人体约 80% 的基因序列都无法成功装载进入,导致其使用范围十分局限。更为棘手的是,由于抗AAV中和抗体的存在,患者在再次接受相同AAV载体递送的药物治疗时会产生免疫反应,因此无法重复给药。
相比之下,“细胞衍生的mRNA疗法”不使用病毒成分,在免疫原性和毒性领域具有先天优势,更不会如AAV一样引起强烈的免疫反应,因此可以实现多次给药。细胞外囊泡能容纳更大的装载物(cargo),足以承载核苷酸长度达到14K的核酸序列,适用范围更广。
即便与目前使用范围较广的LNP递送技术相比,“细胞衍生的mRNA疗法”采用了生物来源的递送工具,比起化学合成的LNP,在安全性和肝外靶向精准度方面占据优势。以思珀生物公布的临床前试验数据为例,与其他递送载体相比,采用EV递送mRNA时的炎症反应、皮肤红肿等局部反应更轻,mRNA的翻译效率更高。
同样据临床前研究数据显示,在裸鼠的光老化模型上,注射COL1A1-EV mRNA后即可观察到小鼠真皮中的胶原蛋白表达明显增加,背部皱纹显著改善,皱纹面积明显减少。定期在有皱纹的皮肤中注射一次,即能够产生大量的胶原蛋白,单次给药后抗皱效果最长能维持70天,而每 2-3 个月定期注射可维持更长时间。更值得一提的是,该疗法是通过补充mRNA使自体细胞表达出天然的产物并将其分布到皮肤中从而实现蛋白替代。这种经机体自然调节而发生的过程,避免了注射后胶原蛋白位移、变形、肿胀等风险。
前沿技术在消费级市场上的应用,也为思珀生物“细胞衍生的mRNA疗法”带来了颇为可观的发展前景。
据弗若斯特沙利文数据显示,2021年全球非手术类医疗美容市场规模达到320亿美元,在中国则达到了近千亿人民币。其中,以肉毒素,玻尿酸和胶原蛋白等几个品种为主的产品终端市场规模,就接近非手术类医疗美容的50%。全球医美巨头艾尔建的肉毒素产品保妥适,2021年全球净收入(非终端)为22.23亿美元;对于高端玻尿酸产品乔雅登,这一数字则是15.35亿美元。再生胶原蛋白类产品和竞争激烈的玻尿酸类产品,以及市场集中度较高的肉毒素类产品相比仍处于起步阶段,但随着国内玩家在重组胶原蛋白方面的技术突破,再生胶原类产品渗透率得以快速增长。在此背景下,思珀生物拥有更高安全性和更出色治疗效果的“细胞衍生的mRNA疗法”,无疑有望开拓出百亿级的蓝海市场。
引领下一代基因治疗方向
前沿技术的转化应用,离不开团队,资金和管线。
思珀生物就汇聚了具备丰富纳米药物递送载体开发经验、细胞及基因治疗开发与合作经验、创新药开发及产业化全流程经验的完备团队。公司已经组建了25人的团队,分别负责CMC,质量,临床样品生产及临床研究管理。思珀生物联合创始人Andrew Lee博士专精于细胞与基因治疗领域,发表了超过50篇文章并主导了多个细胞治疗从研究到临床;另一位创始人李利博士在纳米级工程和脂质颗粒制剂方面有着超过30年的经验,发表了超过400篇文章和30项以上专利。公司总经理倪佳博士,则在工业界拥有14年以上的药物研发经验,主导开发7个以上的新药IND,其中就包括中国第一个PROTAC药物,具有领导药物从研发到上市全过程的经验。

思珀生物官网
充满想象空间的管线应用前景,也让思珀生物成功获得了资本的青睐。2021年,公司就完成了由IDG资本、尚珹资本和盛大投资共同领投的A轮融资。而凭借这笔资金,思珀生物2000平米的第一期GMP标准生产设施已经在2022年建成并投入运营。据介绍,该GMP标准生产设施可满足1-3期临床生产需求,也让思珀生物拥有了世界范围内首条细胞衍生mRNA基因疗法生产线。公司的临床开发管线随后也已获得 IRB 批准,将于 2023 年开始进行首次人体临床试验。
思珀生物对COL1A1-EV mRNA的安全性和有效性充满信心,后续计划在中美澳三地申报IND,从基因治疗的角度为广阔的抗衰老市场带来崭新可能。
实际上,“细胞衍生的mRNA疗法”应用范围绝不仅仅只局限于抗衰老领域。细胞衍生的 mRNA 递送代表了一种新的通用基因治疗方式,它的潜在功能还包括治疗因人体蛋白质的缺失或损伤导致的疾病。很多罕见遗传性疾病都是由于基因/蛋白质的缺失或者表达不足造成的。例如,通过递送相应的mRNA可以形成抗肌萎缩蛋白(dystrophin),从而治疗杜氏肌营养不良症;通过递送VII型胶原蛋白mRNA可以治疗大疱性表皮松懈症等罕见病;也可以在肿瘤治疗中得到更多应用。
思珀生物将从皮肤开始,通过基因疗法来替代因衰老或光老化导致流失的胶原蛋白,此后将以罕见病作为首批适应症和主攻方向。在这一过程中,思珀生物也希望成长为下一代非病毒基因治疗的引领者,为更多临床未解决难题带来新的可能性。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。