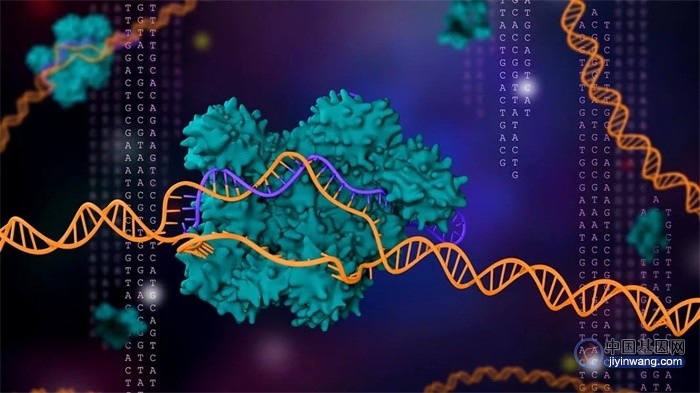
站在基因疗法的风口上:是阿拉丁神灯,还是潘多拉魔盒?
自从 1953 年发现了 DNA 的双螺旋结构,我们对遗传学的认识达到了分子的层面。从基因层面治疗疾病,一直是科学家们的梦想。经历了上个世纪 90 年代的狂热和低谷,人类终于在 2012 年迎来了第一个获批上市的基因疗法药物 Glybera。从此,人类打开了基因疗法的大门。
从小分子、蛋白药物、核酸类药物再到基因疗法,各类药物是如何发挥作用的?他们有什么区别和特点?
为什么基因疗法如此强大却又充满争议?人类第一次有能力改写遗传密码,这是阿拉丁神灯,还是潘多拉魔盒?
本篇文章中,我们从药物发展简史和各类药物与人体的相互作用出发,去理解基因疗法的基础、现状与未来。
本文将就如下问题逐一展开:
1 药物发展简史:从小分子到基因疗法
1.1 各类药物以相应学科为基础
1.2 不同药物的尺寸和复杂性
2 各类药物的作用机制
2.1 「中心法则」和两大生物学过程
2.2 不同的药物作用在不同的「靶点」上
3 基因疗法有多强大?
3.1 SMA——群雄逐鹿,各显神通
3.2 从罕见病到常见病、从治疗到预防、从健康到增强
一样,进入正文前,分享三个结论:
药物研发经历了从小分子、蛋白药物到核酸类药物,到今天已经开启了基因疗法时代。
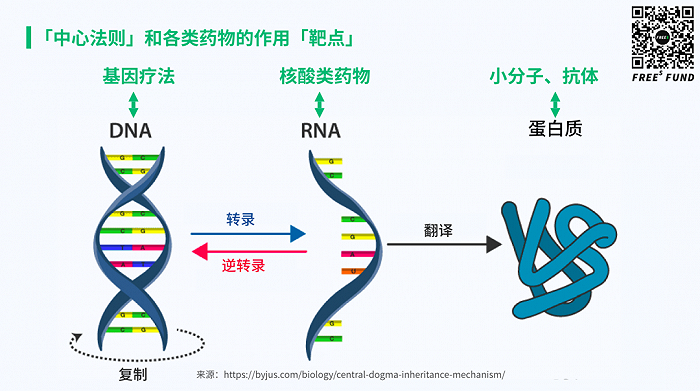
小分子和短肽、抗体类药物作用的「靶点」是蛋白质,调节蛋白的功能;核酸类药物作用的「靶点」是mRNA,调节蛋白的表达;基因疗法药物作用的「靶点」是DNA,不仅可以改变蛋白的表达,甚至还能够可遗传地修改蛋白的编码序列。
基因疗法从因果关系强的罕见病做起,将会逐步拓展到多因素常见病的治疗和管理中。
希望能提供新的思考角度。峰瑞资本在持续关注基因治疗领域的创新,期待与创业团队、从业者与行业专家交流探讨。
01、生命科学的探索与生物技术的发展,使得开发越来越复杂的药物成为现实
▍化学、分子生物学、遗传学的发展,与各种药物的相继登场
化学和小分子药
2019 年 6 月份,考古人员在帕米尔高原(Pamir Mountain)一处距今 2500 多年的古墓遺址中发现高浓度四氢大麻酚残留物。四氢大麻酚是大麻中最主要的精神活性物质,可以让人产生愉悦感和忘记痛苦,这是人类最早吸食大麻的直接证据。
除了大麻,在几千年漫长的与疾病抗争的过程中,人们发现许多植物都具有某些特定的功效,比如金鸡纳树皮可以治疗疟疾,柳树皮可以治疗感冒发烧。这些都是「小」分子药的雏形。随着自然科学的兴起,18 世纪末,人们已经可以把树皮中的一些成分分离出来,起到更好的效果。直到 19 世纪初,人们对物质的认识发展到分子和原子层面,于是化学这门学科就诞生了,也开启了小分子药物时代。
分子生物学和大分子药(抗体)、核酸类药物
18 世纪末,爱德华·琴纳给儿童接种牛痘预防天花,免疫学作为一个学科正式诞生。1890 年,Behring 和北里用白喉外毒素免疫动物时发现了抗体。1953 年 DNA 双螺旋结构让人们对生命的理解达到分子层面。直到 20 世纪 70 年代,随着电子显微镜和基因重组技术的成熟,分子生物学获得了极大的促进和发展。1975 年,Kohler 和 Milstein 发明了杂交瘤技术,使得治疗性单克隆抗体的发现规模化,到 1997 年第一个单克隆抗体获批,大分子药(抗体)时代随之到来。随着反义寡核苷酸和 RNA 干扰技术的诞生,核酸类药物也登上了历史舞台。
遗传学和基因疗法
从 1868 年瑞士医生米歇尔首先发现核酸,到 20 世纪 50 年代初威尔金斯和富兰克林采用 X-射线衍射技术分析 DNA 晶体,以及沃森和克里克发现了 DNA 双螺旋结构并提出分子生物学「中心法则」,再到 20 世纪七八十年代基因重组工程技术得到发展和病毒载体出现,人类对基因的认识和研究不断加深,基因治疗的技术体系初步具备。
1972 年,美国著名生物学家西奥多·弗里德曼等人在《科学》杂志上发表了一篇具有划时代意义的前瞻性评论《基因治疗能否用于人类遗传病?》,提出了基因治疗是否可以用于人类疾病治疗的问题。
从 1990 年首例基因疗法的临床试验治疗重症联合免疫缺陷病(SCID)开始,到 1999 年 18 岁美国男孩杰西·格尔辛格参与美国宾夕法尼亚大学基因治疗项目因多器官衰竭死亡,基因治疗的「希望肥皂泡」破裂,从此进入最黑暗和最艰难的一段时期。
经过 20 多年的不断探索,基因治疗终于迎来了第二个春天。2012 年,荷兰UniQure 公司的Glybera由欧盟审批通过,采用腺相关病毒(AAV)作为载体治疗脂蛋白脂肪酶缺乏引起的严重肌肉疾病。作为第一个正式获批的基因治疗药物,Glybera 的成功开启了基因治疗的新时代。
▍不同药物的尺寸和复杂性——与交通工具的类比
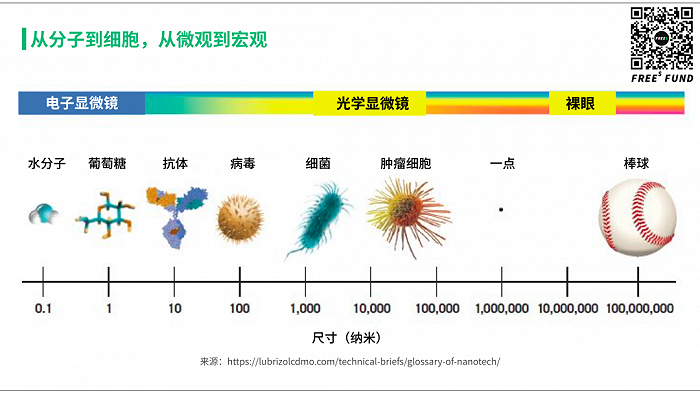
把分子到细胞按照尺寸大小排个序,最左边的是小分子,大概在几个纳米这个范围。大分子药物的尺寸比小分子大了 1-2 个数量级,达到 20纳米左右。基因疗法目前使用最广泛的是腺相关病毒,大概和抗体的尺寸相当。其他类型的病毒载体一般都会更大一些,达到 100 纳米左右。跟我们人体的真核细胞相比,还是小 2-3 个数量级。这还都是在微观层面,需要借助显微镜才能观察和研究。而到了肉眼可见的层面,比如我们能看到的一个点,就又比细胞大了约 100 倍。

让我们再用交通工具来作类比,试着理解不同药物的特点。小分子药就像自行车,它的制造和生产是最容易的。短肽类和小核酸类药物就像汽车,重量增加了不少,也复杂了不少。大分子药(抗体)就像飞机,而基因疗法使用的病毒载体就像火箭。
一般来说,越小的东西,它本身的复杂程度越低,这个容易理解。但在作用机制上和功能上,却会有不同的情况。
首先,每一种药物都有自己的适用场景,继续拿交通工具举例子,比如我们要去亲戚家串个门,骑个自行车估计是最方便快捷的,当然开车也行如果停车不是很麻烦的话,但是不可能坐飞机火箭吧。
其次,各类药物的作用机制不同,灵活性也不一样。比如,我们骑个自行车出去办事儿,可能有好几个目的地,可以很灵活的安排调整,真不想去了或者突然下雨了,回家就是了。但飞机、火箭目的地非常明确,一旦出发不能改变,除非返航迫降,那都是很大的事件了。
最后,结构上相对简单的小分子,安全性上却比不上抗体和基因疗法。比如我们都觉得坐飞机飞在天上不安全,实际上事故率飞机是最低的,是最安全的,自行车反倒可能是最不安全的。
做这个类比是想说,每种药物都有自己的特点和用武之地,不会因为出现了大分子抗体药和现在的基因疗法,小分子药就没有价值了或者可以被取代了。基因疗法虽然很热,但也无法取代抗体药或小分子药,只是作为一种新的治疗手段,确实可以解决小分子和抗体药物都很难解决的问题,就像只有火箭能把我们送出地球,去探索更为广阔的宇宙空间。这也是我们下面要讨论的问题。
02、从「中心法则」和生命两大过程,来理解不同药物的作用机制
▍「中心法则」和两大生物学过程

要理解这个问题,我们先来重温一下现代生物学基础——「中心法则」。「中心法则」是佛朗西斯·克里克 1958 年时就提出的,1970 年他写了一篇文章,发表在《自然》杂志上。这个文章的核心就是一句话,「分子生物学的中心法则旨在详细说明连串信息的逐字传送。它指出遗传信息不能由蛋白质转移到蛋白质或核酸之中。」这句话非常拗口,其实就是在回答遗传信息是如何传递的这个问题。
克里克解释说,对于生物体中三类主要生物大分子:DNA、RNA 和蛋白质,有 9 种可能的传递顺序。法则将这些顺序分为三类,3 个一般性的传递(通常发生在大多数细胞中),3 个特殊传递(会发生,但只在一些特定条件下发生),3 个未知传递(可能不会发生)。

把这些复杂的关系,总结成下面的图,就是现在我们都很熟悉的中心法则。它诠释了生命的基础特征之一——遗传。这是生命能够稳定存在的基础。
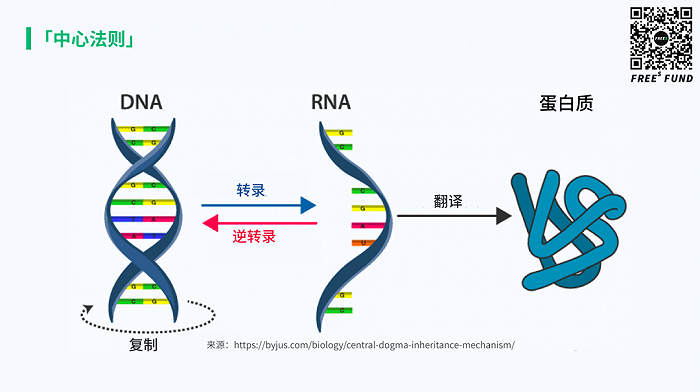
生命实际上是非常复杂的。遗传信息经过翻译和修饰支撑起了生命体内形形色色的生物学过程,这里我们重点介绍其中两个重要的过程:信号转导和新陈代谢。
信号转导要解决生命与外界、生命自身的信号调控问题。从受精卵开始那一刻起,它怎么分化,怎么发育,如何感知和应对外界刺激、如何自我保护,以及到高等动物中出现了记忆、情感,再到衰老,都涉及到信号转导和调节。经过几亿年的进化,自然界创造出相当复杂却又十分精准的调控体系,让生命得以呈现出今天的状态、让人类得以成为一个物种。
代谢解决的是生命体与环境之间的物质和能量交换问题。生命是一个开放体系,它要维持正常运转,就需要不断地摄取物质、排出废物,就需要解决能量的产生、存储和使用等问题。
大家可能看到了一些比较简单的结构或者节点,它们都是小分子。因为我们生命的物质基础就是小分子,包括最简单的氧气、二氧化碳再到糖类、氨基酸和脂类。这些物质之间的转化,涉及到大量的酶(一类能催化化学反应的蛋白质)。这些酶和小分子之间的作用机制,就是我们平常说的生物化学的主要研究内容。
▍不同的药物作用在不同的「靶点」上
第一个问题,疾病的产生。有些疾病的原因是相对单一的,比如单基因遗传病;有些疾病的原因是相对复杂的,比如肿瘤或者代谢类疾病。
第二个问题,药物的目的就是来修正这些问题和缺陷,前提是对正常生命活动的干扰尽量小,否则可能出现副作用。如果药物带来的收益,抵不上它引起的副作用,专业领域我们会说它的治疗窗口不够,通俗一点可以认为这个药物得不偿失、没有太多价值。
以蛋白质为「靶点」的小分子、短肽和大分子抗体药
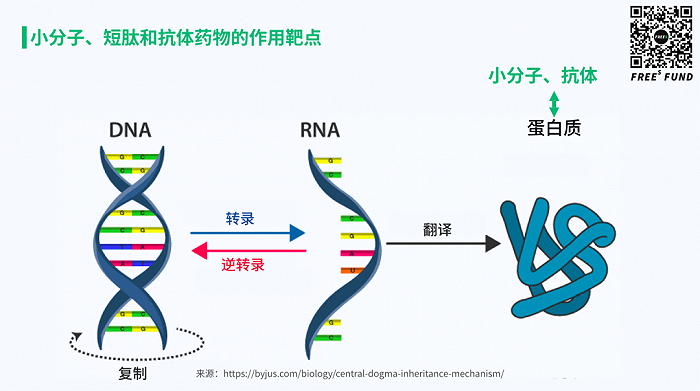
小分子、短肽和大分子抗体药一般情况下,都是通过蛋白质起作用的。于是我们说,这类药物的「靶点」是蛋白质。前面提到的信号转导和代谢这两大功能,主要是由蛋白质参与完成的。所以可以概括地说,小分子、短肽和大分子抗体药是通过影响蛋白质的功能,去干预信号转导或者代谢等过程,从而实现治疗疾病的目的。我们习惯上把这些统称为靶向药。
虽然都是以蛋白质为靶点,那小分子和短肽/抗体药有什么区别呢?
第一、由于小分子可以自由穿过细胞膜,小分子作用的靶点可以在细胞内,但是抗体和短肽主要作用在细胞膜上的蛋白或者细胞外蛋白。
第二、小分子的作用靶点主要是蛋白,这些蛋白在正常生命活动中,通常也会涉及到跟体内天然存在的小分子之间的相互作用,比如代谢相关蛋白和小分子代谢物、GPCR 和小分子信号分子、激酶和小分子辅因子等。而抗体的作用靶点,通常涉及到配体-受体相互作用,也就是大家常听到的蛋白-蛋白相互作用。
从这两类药物的起源来考虑,就不难理解它们之间的差异了。最早有药物活性的小分子,比如前面提到的四氢大麻酚、奎宁、阿司匹林,本来就是一些物种的代谢产物。这些分子由蛋白质合成出来,去结合其他蛋白(可以是其他物种的)而起作用,使得该物种在进化上获得了一些优势。只是恰好在人体内,我们发现了它们的一些治疗作用和治疗窗口,因而被发展成药物。
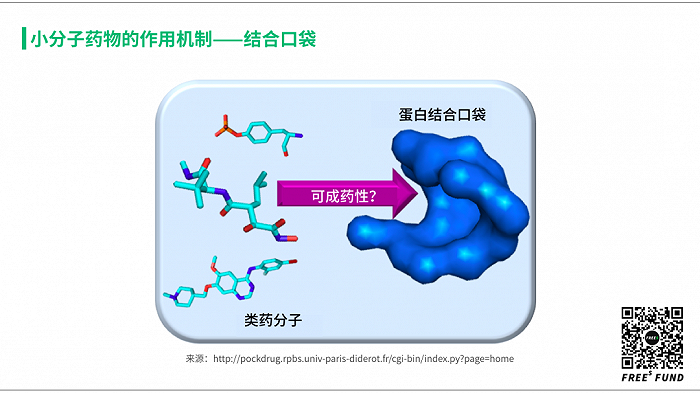
前面提到抗体是人体免疫系统抵抗外来侵犯的武器,也是身体自我检查和纠错的机制。因为蛋白是暴露在细胞表面(包括细菌和病毒表面),最能够区分敌我和正常/异常的标志,所以就被免疫系统使用,通过抗体来识别和区分自体的、正常的蛋白,和那些入侵的、异常的蛋白,区分「自我」和「非我」。所以,抗体药物的主要靶点是膜蛋白和细胞外蛋白,主要识别模式是所谓的蛋白蛋白相互作用,又称为「表位识别」。这是整个免疫学的基础,也是抗体药的基础。
人体内,大概一共 1 万 9 千多种蛋白,目前发现大约 5000 多种蛋白(约占1/4)跟疾病相关。这其中目前已经获批的药物针对的靶点大概有近 700 种,潜在的可成药靶点大概有 1200 多种,另外还有 3 千多种疾病相关蛋白被称为「不可成药」。
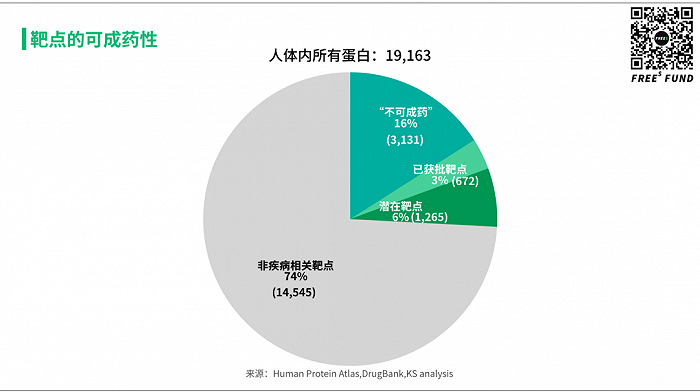
这些蛋白主要是在细胞内,无法用抗体去作用;也没有已知的天然存在小分子跟它们有相互作用,这使得小分子药的开发也变得很困难。当然,「不可成药」这个定义加了引号,也就意味着只能说现在还未成药。随着小分子和抗体领域技术手段的提升,我们有越来越多的手段和工具去干预这些靶点,希望这个定义被推翻,或者至少「不可成药」靶点数量越来越少。
以 RNA 为靶点的核酸类药物
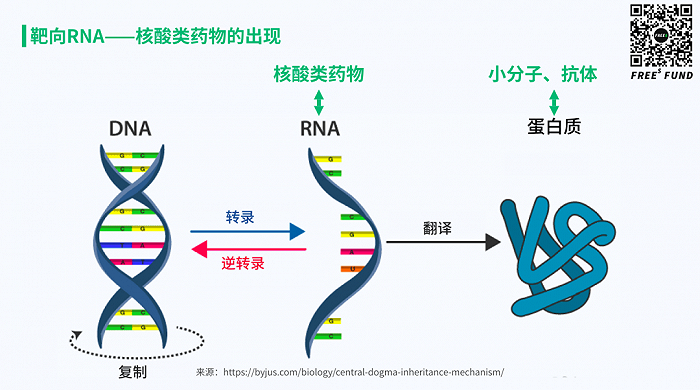
让我们回到这个「中心法则」,前面讨论的小分子和抗体类药物的作用靶点是蛋白质,那么针对 RNA 的药物我们把它称为核酸类药物。这类药物之所以成为可能,是因为两个底层技术的突破,一个是 1978 年 Zamecnik 和 Stephenson 发现了寡义核苷酸,另一个是 1998 年 Fire 和 Mello 发现了所谓的 RNA 干扰。
有趣的是,ASO 第一篇文章发表 20 年之后,1998 年,第一个 ASO 药物获批;同样,RNA 干扰技术发现 20 年之后的 2018 年,第一个 RNAi 药物获批。大概经过 20 年时间,一个技术从发现到成功应用于临床,使得我们第一次能够把对生命的调节系统化扩展到 RNA 这个层面。
我们说小分子和抗体药物跟蛋白质结合以后,会影响蛋白的某些功能,比如信号转导或者催化活性,从而起到治疗作用。但是,这种功能上的调节,通常不会直接引起蛋白本身浓度的变化(实际情况复杂且存在特例,这里高度概括),而 RNA 药物的作用机制恰恰就是蛋白的表达量(或表达形式)本身。
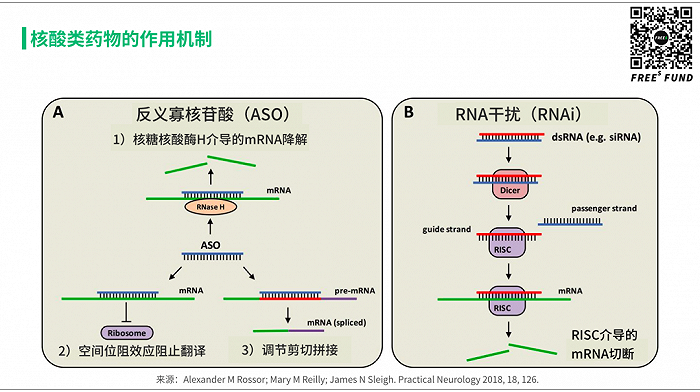
简单来说,无论是单链的DNA或RNA(ASO),还是双链的dsRNA(RNAi),它们与靶向的 mRNA 结合之后,将 mRNA 直接降解掉,或者阻碍其翻译成蛋白,或者影响其拼接而表达不同形式的蛋白。无论如何,蛋白的表达量(或者表达形式)被改变了,这就是核酸类药物的作用机制。
从核酸类药物的发展史来看,两家代表性公司都在这个领域经历了多次起起伏伏,可以说经历了至少两轮 Hype Cycle。
第一次是 RNA 靶向技术本身在人体内的验证,第二次是递送手段的突破,使得临床上找到了更好的治疗窗口。特别是最近几个重量级药物获批,使基于这类平台技术的新药开发公司受到产业和投资界的追捧。有兴趣的读者可以去阅读相关报道和综述文章。
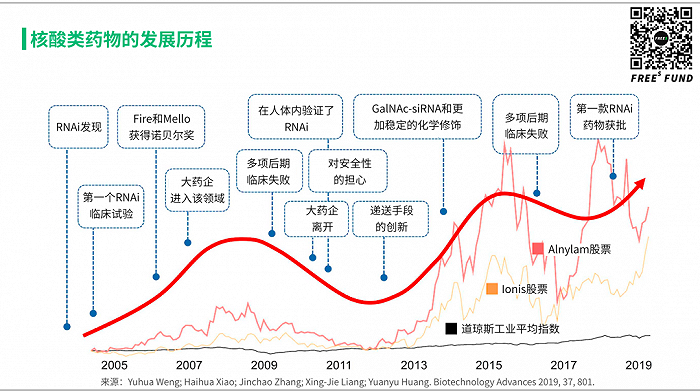
这里,我们还是回到各种药物手段的特点和区别,通过对比来理解核酸类药物的前景和局限。
前面说过,第一个 ASO 药物,是 1998 年获批的 Fomiversen,作为巨细胞病毒(CMV)视网膜炎的二线治疗药物。但由于高活性抗逆转录病毒疗法的发展,巨细胞病毒病例数量急剧下降,该药物在欧洲及美国分别于 2002 年及 2006 年退市。
这样的结果并不奇怪,因为本来抗病毒就是小分子最擅长的领域。但这并不妨碍核酸类药物在抗病毒领域的持续探索,无论是在 2003 年的非典,还是这次新冠,都有科学家在研究通过这项技术抑制病毒,这是后话。
另一个有名的 RNAi 药物,Bevasiranib,靶向 VEGF 的 mRNA,用于治疗老年性黄斑变性(AMD)。2008 年完成了三期临床试验,却在 2009 年停止开发。
为什么会这样?因为 VEGF 是个生长因子,它和受体 VEGFR 结合促进血管生成,而阻断这个作用最适合的药物手段是抗体。2006 年,Genentech 的 Lucentis 成功获批,迅速成为金标准,Bevasiranib 只能黯然离场。
2018 年对于核酸类药物都是极其重要的一年,FDA 先后批准了两款针对遗传性转甲状腺素蛋白淀粉样变性(hATTR)的核酸类药物。一个是 Ionis 公司开发的 ASO 药物 Tegsedi,另一个是 Alnylam 公司研制的 Onpattro,而后者是获批上市的第一款 RNAi 药物。
hATTR 是一种罕见的进展性、系统性、致死性遗传性神经疾病,是由于 TTR 淀粉样蛋白异常形成和聚集并沉积在全身多个器官和组织所导致的。
Tegsedi 和 Onpattro 的治疗都可以大大降低 TTR 蛋白水平,并使患者在神经病变和生活质量方面获得实质性改善。预期这两款药物会在定价、使用便利性、真实世界疗效和包括营销方面激烈对决,但无论结果如何,它们的成功获批无疑给行业带来了巨大的热情和希望,因为这才是核酸类药物最擅长的应用场景。
从能解决的问题上来说,核酸类药物有着不同于小分子和抗体药物的特长。但是从药物研发的角度来说,核酸类药物要冲破重重阻碍,才能真正发挥作用,这比小分子和抗体要复杂很多。
首先,不像小分子和抗体,核酸类药物在血液中不仅稳定性很差,还有免疫原性等问题。
其次,核酸类药物表面带有许多负电荷,没有穿过细胞膜的能力,但它的作用靶点是 mRNA,也就是必须要进入细胞质内才能发挥作用。因此,核酸类药物的细胞内递送是个巨大挑战。
最后,核酸类药物的大规模生产和质控比抗体药物复杂,比小分子药物复杂得多,这也限制了其大规模研发和探索。这也就解释了为什么核酸类药物的发展,经历了多次 Hype Cycle,才达到今天这样的水平。
以 mRNA 为药物的新风口
经历了这次新冠疫情,想必大家都对 mRNA 疫苗和 Moderna 公司不再陌生。作为美国生物医药领域 IPO 市值最高的独角兽公司,Moderna 公司的发迹史充满传奇,非常有趣,建议大家去读一读。前面提到的开发核酸类药物的公司,以 mRNA 作为靶点,然而近些年涌现出来的包括 Moderna 在内的一些公司,选择把 mRNA 本身作为药物来治疗疾病。
Moderna 公司其实已经在开发针对 CMV 和流感病毒的 mRNA 疫苗,只是这次突如其来的疫情,引发了人们对这个方向的极大关注,尽管其实到目前为止还没有一款 mRNA 疫苗真正获批用于传染病预防。针对此次新冠,Moderna 公司更是跳过了临床前的动物实验验证,直接开始将疫苗应用于人体。我们暂且不评论这么做的伦理问题和疫苗最终是否有效,对于 Moderna 公司来说,这是一次商业上的成功,对整个 mRNA 领域来说,这也是一次难得的促进和宣传。
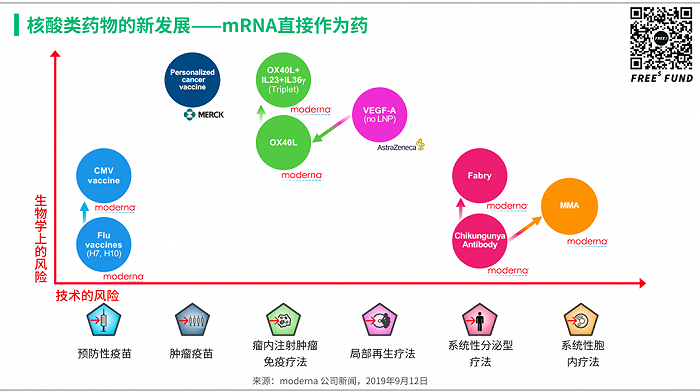
关于 Moderna 公司产品管线,这里我们多说两句。请看这张图,来自于公司去年的一次投资人关系会议上的宣讲材料。这个产品管线布局的策略和思路非常有意思,值得所有新型治疗手段的研发者参考。
坐标系的纵轴叫「生物学上的风险」,横轴是「技术的风险」。用通俗的话来说,纵轴越靠上,意味着生物学上的因果关系越不确定,也就是到底能不能治疗疾病不好说,当然风险越大。横轴越靠右,意味着技术上实现起来越困难,要解决的问题越多,挑战越大,当然风险也越高。
Moderna 公司自己的产品管线怎么布局呢?
首先,肯定是选择生物学和技术上风险都小的方向,这就是针对 CMV、流感和新冠的预防性疫苗。
其次,它选择了技术上有挑战但是生物上因果关系强的遗传病。可以这么理解,由于生物层面的因果关系比较明确,如果临床结果不好,只要去解决技术问题就可以了,而技术问题是相对容易解释和改进提升的。
最后,当然是那些技术上风险较大(虽然可能不是最大),但生物上不确定性特别强的方向,比如肿瘤疫苗以及和肿瘤免疫相关的细胞因子疗法。
与之前提到的那些治疗领域相比,这些方向如果取得突破,有着巨大的市场和丰厚的回报,但面临着两方面的不确定性和风险,所以选择和大公司共同开发,风险共担、收益共享。Moderna 之所以能成为史上最成功独角兽,从技术壁垒到战略方向,还是有不少值得学习的地方。
这里引出了的两个概念,即「生物上的风险」和「技术上的风险」,为我们下面要讨论的基因疗法提供了一个非常重要的分析框架。
以DNA为「靶点」的基因疗法
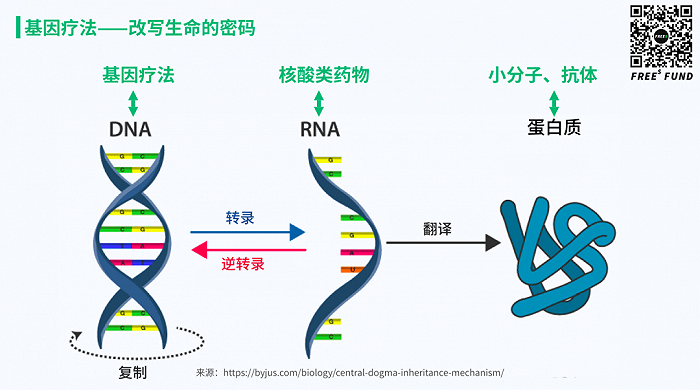
让我们再回到「中心法则」。自从发现了 DNA 是我们的遗传信息的核心载体,改变 DNA 的尝试就从来没有停止过。

说起基因疗法,不能不提起James Wilson。1999年9月17日,Jesse Gelsinger 在宾夕法尼亚大学 James Wilson 实验室接受了大剂量携带校正基因的腺病毒(Ad),以治疗罕见的代谢性肝病——鸟氨酸转氨甲酰酶缺乏症。治疗 4 天后,Jesse 由于强烈的免疫反应导致多器官衰竭和大脑死亡。James 被剥夺了头衔,他领导的基因治疗中心被解散,他被禁止在 2010 年之前进行任何临床试验。
James 缩小了实验室的规模,把精力放在寻找更安全的病毒上。他们的工作促使了新型腺相关病毒(AAV)的发现和传播,包括最近批准的基因疗法 Zolgensma 中使用的 AAV9。
2015 年 9 月 17 日,杰西去世 16 周年纪念日,基于新的 AAV 载体创办的生物技术公司 Regenxbio 在纳斯达克上市。根据宾大的最新统计,约有 42 家公司正在使用属于威尔逊专利的 AAV,涵盖近 100 个药物开发项目。基因治疗从低谷走向巅峰,而 James 见证了这一切。
回到前面的分析框架,基因疗法从技术上说最大的风险在于药物的递送。比核酸类药物的要求更高,基因治疗药物需要在细胞核内才能发挥作用,因为基因本身是在细胞核内的。所以,早期和目前流行的基因治疗药物,都选择用病毒作为药物递送的载体。99 年发生在 Jesse 身上的悲剧,跟使用了腺病毒这个病毒载体直接相关。前面分析过,核酸类药物的递送、生产都已经是挺大挑战了,更不要说使用有感染能力的活病毒作为载体。
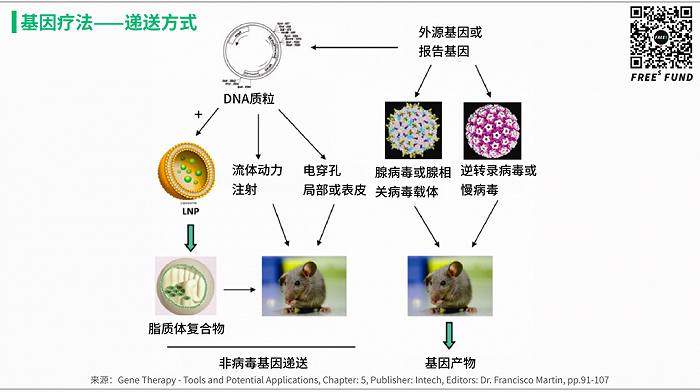
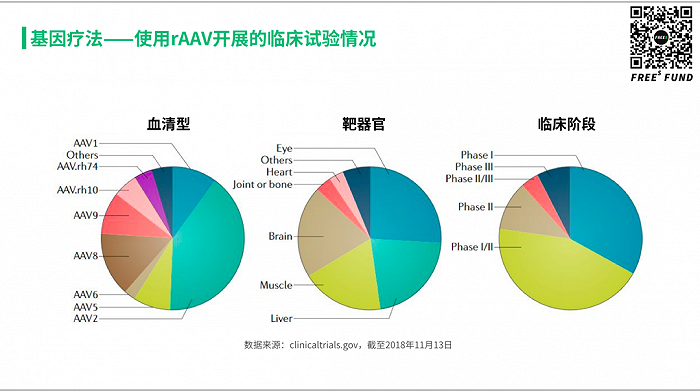
幸运的是,人们很快发现了腺相关病毒(AAV)可以作为这样的递送载体,将药物高效递送进入细胞核发挥作用,同时安全可控,对人体带来的风险和副作用较小。截至 2018 年底,约有 145 项使用 AAV 进行基因治疗的临床实验,针对的器官主要是眼睛、肌肉、肝脏和神经系统。当然绝大部分适应症都是单基因异常造成的遗传性疾病或者罕见疾病。但随着技术上的风险和不确定性被逐渐降低,基因疗法会很快拓展到像 AMD、帕金森氏症等常见疾病中。
基因疗法大体上可以分为四个方向,分别是基因替代、基因添加、基因沉默、基因编辑。
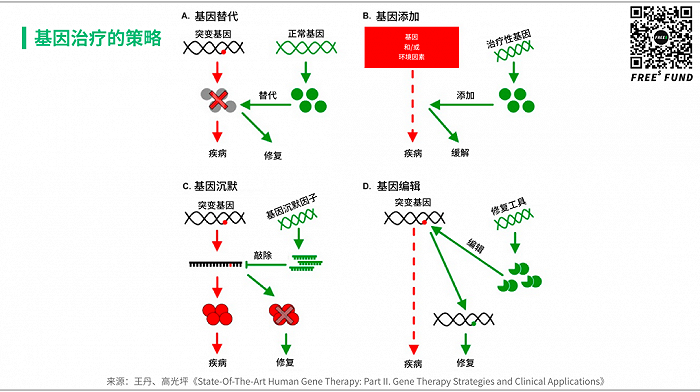
1)基因替代(gene replacement)
该策略旨在提供基因产物以补偿功能丧失突变。基因替代适用于治疗隐性单基因疾病,并且已经获得了最大的临床成功,如已上市的 Glybera 和 Luxturna。
2)基因添加(gene addition)
除了单基因疾病外,rAAV 介导的基因治疗还有可能通过基因添加,来解决复杂的遗传疾病和后天性疾病,如心力衰竭和传染病。此外,还可通过 rAAV 递送抗体,比如肌肉细胞被转导后,可以转化为生物工厂,产生治疗性抗体并分泌到血流中。
3)基因沉默(gene silencing)
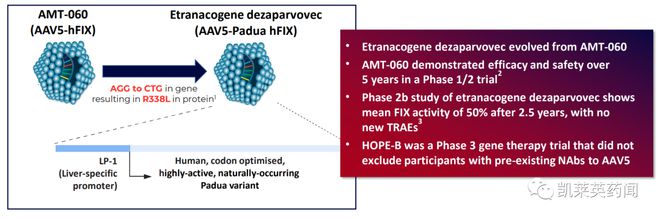
与基因替代相反,基因沉默主要解决由毒性增加的突变引起的单基因疾病。目前是用 rAAV 递送 RNAi 的策略实现基因沉默。然而,与核酸类药物(siRNA和ASO)相比,基于 rAAV 的 RNAi 疗法大多处于临床前开发阶段。近日,uniQure 公司针对亨廷顿病的 AMT-031 IND 申请获 FDA 批准。
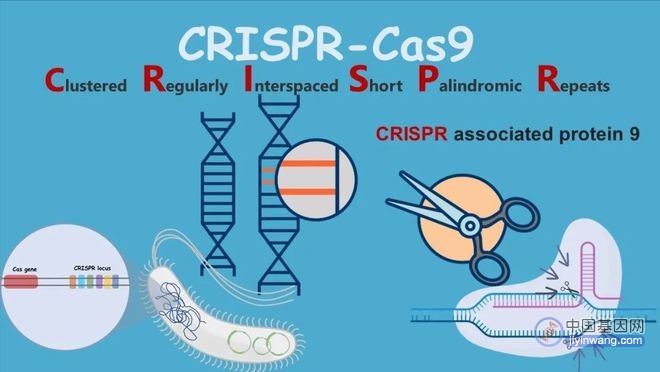
4)基因编辑(gene editing)
rAAV 可以用来递送 CRISPR 相关(Cas)蛋白,直接修复人类疾病的相关突变。
关于基因疗法的具体进展,有兴趣的读者可以去阅读相关报道或者综述。我们这里还是通过两个例子,来理解基因疗法的特点、局限和前景,以及为什么基因疗法引起了全社会如此规模的关注和探讨。
03、基因疗法有多强大?手握「上帝的手术刀」,我们可以干预遗传这一自然法则了吗?
▍SMA——群雄逐鹿,各显神通
SMA 是一种罕见的遗传性神经肌肉疾病,由于缺乏功能性 SMN1 基因,SMA导致运动神经元的快速和不可逆丧失,影响肌肉功能,包括呼吸、吞咽和基本运动。SMA 是 2 岁以下婴幼儿群体中的头号遗传病杀手,其中 1 型 SMA 是最常见的类型,约占所有病例的 60%。如果不进行治疗,90% 以上的患者在 2 岁时会死亡或需要永久性通气。
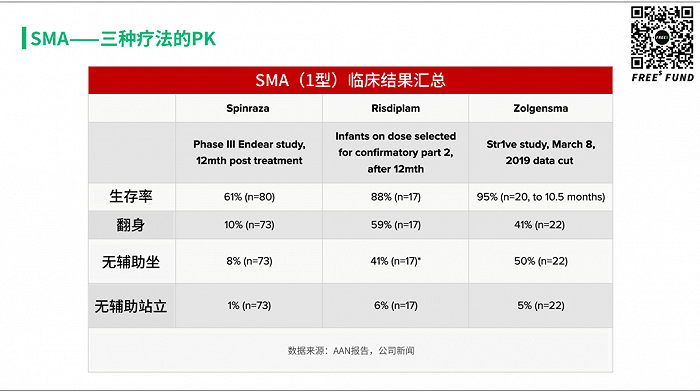
2016 年底,FDA 批准了 Ionis 公司开发的第一款 SMA 治疗药物 Spinraza。Spinraza 是一种反义寡核苷酸(ASO),通过鞘内注射(intrathecal injection)给药,将药物直接递送至脊髓周围的脑脊液(CSF)中。Spinraza 旨在改变 SMN2 前信使 RNA(pre-mRNA)的剪接,以增加全功能性 SMN 蛋白的生产,在 SMA 患者中,SMN 蛋白水平不足导致脊髓运动神经元功能退化。在临床研究中,Spinraza 治疗显著提高了 SMA 患者的运动机能。
2019 年 5 月,以 James Wilson 组开发的 AAV9 作为载体的 Zolgensma,获得美国 FDA 批准上市,成为全球首个治疗 SMA 的基因疗法。该药是一种一次性基因疗法,旨在通过替代缺失或不起作用的 SMN1 基因的功能,来解决SMA 疾病的基因根源。在单次静脉输注(IV)给药后,Zolgensma 将 SMN 基因的一个功能拷贝导入患者的细胞,持续表达 SMN 蛋白来阻止疾病进程,从而长期改善患者生存质量。
同时,罗氏公司正在开发一款口服小分子药物 Risdiplam,这是一种运动神经元生存基因 2(SMN2)剪接修饰剂,开发用于所有类型 SMA 的治疗。目前,该药正在接受美国 FDA 的优先审查,预计近期会获得审查结果。如果获得批准,Risdiplam 将成为治疗所有 3 种类型 SMA 的首个口服药物。
一个适应症,三种药物,核酸类 Spinraza、基因疗法 Zolgensma 和小分子Risdiplam。
从疗效上看,目前公布的临床结果,生存率上基因疗法看起来是最好的,95%都能存活;从患儿翻、坐和站的改善情况来看,小分子和基因疗法差不多,都比 Spinraza 数据要好。
从使用方便来看,Spinraza 需要做骨髓穿刺,确定是 1 型基因突变才能使用;使用 Zolgensma 不需要骨髓穿刺,但必须抗 AAV9 抗体为阴性;Risdiplam 不需要穿刺确定基因型,对三种基因型都适用,对患者有什么限制目前还不确定。
从定价来看,Spinraza 第一年 75 万美金,以后每年 37.5 万;Zolgensma 只需要静脉给药一次,药价达到了史上最贵的 210 万美金,分五年付清;Risdiplam 需要长期服用,目前定价未知。
对于同一种适应症,同时有了三种完全不同的疗法,这在人类疾病的治疗史上是不多见的。同样出乎意料的是,本来是基因疗法最擅长的领域,没想到竟然出现了来自小分子的竞争。无论这几种药物的市场和销售前景如何,对于 SMA 患儿来说都是最大的福音。
可以毫不夸张的说,基因疗法为我们打开了一扇新的大门,我们对疾病的干预手段更加丰富,对健康的认知和理解也会发生颠覆性的变化。同时,我们也面临着一系列伦理和道德的挑战。
▍从罕见病到常见病、从治疗到预防、从健康到增强——我们会走向何方?
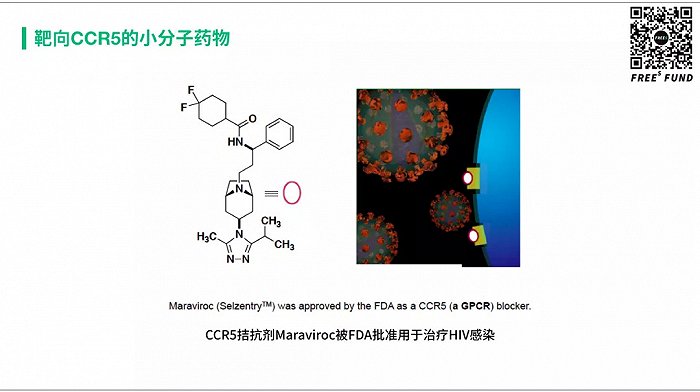
CCR5 是一个 GPCR,在 T 细胞上。HIV 病毒要想感染 T 细胞,需要结合这个受体。最开始发现这个基因跟 HIV 有关,是来自于一项流行病学研究。这项研究发现一小部分高风险人群对 HIV 病毒不易感,而该人群中编码 CCR5 的基因发生突变。随后在大规模人群基因测序中发现,在白种人中,大概有 10-20% 的人这个基因缺失了一半;大概有 1-2% 的人群这个基因彻底缺失,而这部分人几乎完全抵抗 HIV 感染。科学家随后发现了 CCR5 的功能和在 HIV 感染细胞中的关键作用。
CCR5 是一个膜蛋白,既可以用小分子,也可以用抗体来阻断,都可以阻止HIV 病毒的感染。2007 年,辉瑞公司开发的小分子 CCR5 拮抗剂 Maraviroc 获批上市。预计今年,CytoDyn 公司开发的抗体药物 leronlimab 可以获得 FDA 的批准。
在进行药物研发的同时,医学界一直有一个大胆的想法,能不能给艾滋病患者移植 CCR5 缺失的供体血液,从而达到治愈 HIV 的目的。这就要说到第一个和第二个「柏林病人」。由于第一位患者是匿名而且信息不全,我们主要来看看第二位。
2006 年,一名 40 岁的德国白人男性患者 Timothy Brown 住进了当地的一家医院,被诊断为急性粒细胞白血病。同时,这名患者在 10 年前已经确诊被艾滋病毒感染,一直在使用抗病毒疗法。他的医生 Gero Hütter,安排他接受来自于 CCR5 缺失的捐献者捐赠的骨髓进行移植。这样骨髓移植成功后,这个艾滋病毒感染患者体内的T细胞上的 CCR5 也会缺失,是不是就可以抵抗艾滋病毒了呢?
非常幸运,这样的供体被找到了,Timothy 先后接受了两次骨髓移植,2007 年一次,2008 年一次。Timothy 在第一次移植的那天就停止服用抗逆转录病毒药物。第一次骨髓移植后三个月,体内 HIV 迅速下降至无法检测的水平,而他的 CD4-T 细胞计数却增加了。截至 2011 年,布朗仍未恢复抗逆转录病毒疗法。尽管有争议,Timothy 被认为是第一位实现了功能性治愈的艾滋病人。
当我们有了基因疗法这个全新工具,人们便开始希望复制「柏林病人」的成功。如果把艾滋病人的T细胞进行改造,把 CCR5 这个靶点给沉默掉,是不是就可以治愈 HIV 了呢?一家叫 American Gene Technologies 的公司,开发了一款基因疗法 AGT103。原理是把病人的T细胞分离出来,用 AGT103 把CCR5 这个基因沉默掉,体外培养后再回输病人体内。这样病人的T细胞表面就不再有 CCR5 这个受体,也就不会再被 HIV 感染。和「柏林病人」一样, 这样就可以实现真正的治愈。目前,这个药物正在开展临床实验。
既然有这样大胆的想法,就难免会出现更疯狂的事情。这就是 2018 年底闹得沸沸扬扬的「贺建奎事件」,即直接在胚胎层面做了编辑,把 CCR5 这个基因敲掉,希望从此这个胎儿再没有被 HIV 感染的风险。当然,这个事件在全世界范围内引发了巨大的伦理挑战。
浙江大学生命科学研究院王立铭教授,把基因编辑比作「上帝的手术刀」。最近恰好重温了 1997 年的好莱坞影片,Gattaca(千钧一发),讲的是一个没有做过基因改造的「自然」人文森特,借助基因优秀却意外瘫痪的杰罗姆的身份,实现自己漫游太空梦想过程中的一系列遭遇。
如果,「贺建奎事件」只是一个开始,在我们拥有了「上帝的手术刀」以后,可以许个愿,让我们自己和我们的后代变得更美丽、更聪明、更长寿,这对人类这个物种来说,到底是拥有了梦想成真的阿拉丁神灯,还是打开了无法控制的潘多拉魔盒?
本篇总结
1,药物研发经历了从小分子、蛋白药物到核酸类药物,到今天已经开启了基因疗法时代。
2,小分子和短肽、抗体类药物作用的「靶点」是蛋白质,调节蛋白的功能;核酸类药物作用的「靶点」是mRNA,调节蛋白的表达;基因疗法药物作用的「靶点」是DNA,不仅可以改变蛋白的表达,甚至还能够可遗传地修改蛋白的编码序列。
3,基因疗法从因果关系强的罕见病做起,将会逐步拓展到多因素常见病的治疗和管理中。
互动思考
Q:在基因疗法领域,平台型公司还是产品管线公司会有更好的发展前景?
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。