奇迹or契机?细胞与基因疗法的破局之道!
长达十多年的无癌生存,意味着已经完全临床治愈,这是广大患者所期待的生命奇迹。
作为世界上第一个接受CAR-T细胞疗法的孩子,曾患致命性白血病的Emily现已无癌生存11年,成为生物医药里程碑的真实印证。
而以CAR-T为代表的细胞与基因疗法(CGT)也在近年来迅速发展为医药健康产业炙手可热的领域:它使人类能够以一种全新的范式,有效治疗乃至治愈非常棘手的疾病,让成千上万像Emily一样的患者改写自己的生命故事,也一次又一次鼓舞了全世界为攻克疾病不断寻找新疗法的研发人员们。
在可预见的未来,仅2023年就有多达16款全新的细胞或基因疗法有望在全球获批,将为更多患者带来“长久治愈”的可能。

聚力合作,推动产业创新
一项突破性疗法从诞生走向成熟,往往会改写生物医学的发展脉络。但不容忽视的是,细胞与基因疗法在技术、产能、商业化等方面仍存在拖慢进展的因素,克服现存的挑战,才能催生真正的变革。
细胞与基因疗法是“活的药物”,对生产环境的细微变化高度敏感,其工艺开发的难度也相应地比传统药物高出几个数量级。
以CAR-T疗法为例,该技术要从患者的血液中分离出免疫T细胞,经过工程化改造和数量扩增,重新输回患者体内,让T细胞通过识别并攻击特定的癌细胞,达到治疗肿瘤的目的。这一提取-改造-回输的过程,便涉及质粒、病毒、细胞三个不同对象,所需的培养、纯化、测试等工艺均不尽相同。
对很多创新生物医药企业而言,将CGT研发成果推向市场是一项艰巨的工作,既要满足繁复的工艺流程、居高不下的生产成本,还面临法规监管、工艺放大的稳定性和一致性、风险控制等诸多方面的挑战。
可喜的是,产业正向着一个更高效的模式努力。在新一代CGT疗法开发中,CTDMO(Contract Testing, Development and Manufacturing Organization)平台已成为产业合作创新的重要力量。
细胞和基因疗法公司+CTDMO强强联合的模式,使得研发企业能够保持相对轻量型的运营管理,更专注于核心药物的研发和创新,而规模化的测试、部分生产环节可以交给更加专业的CTDMO合作伙伴,以形成产业化优势,提升效率,降低成本,提升患者可及性。
作为药明康德(603259)旗下专注于细胞和基因疗法的CTDMO平台——药明生基(WuXi ATU)是全球少数“一站式”实现不同检测开发、生物安全、病毒清除和最终药物放行等测试环节的平台之一,不仅可以提高研发和工艺放大优化的效率,降低样品消耗率和多次转运所造成的不稳定性,更有利于完善把控工艺放大各环节的风险点,帮助开发者大幅缩短整个上市周期。
针对个体化治疗极高的质控要求,CGT疗法不但需要QbD(Quality by Design)的理念,同样依赖于独特的评估体系进行测试和表征。值得一提的是,药明生基在多年前就建立了内部分析和测试能力,能够表征复杂的病毒、细胞和生物用品,致力于攻克业界公认的难题。
药明生基内部搭建了4种测试能力,包括放行测试、脉冲控制测试和生物安全测试等,既可为全球合作伙伴提供平台化、标准化的测试服务,也可满足定制化测试的需求。在药明生基,单个基地内就能完成开发、生产、测试工作,避免了物料转运带来的不稳定性,有利于完善把控工艺放大各环节的风险,更大幅缩短了vein-to-vein(静脉到静脉)的时间周期,满足全球合作伙伴CGT药物快速放行的实际需求。
对此,药明生基首席商务官陈琪博士有着深刻的行业见解:“在CGT行业,检测及放行能力深度影响着创新疗法开发的进程和最终药物的安全性与有效性。药明生基自身拥有的完备检测体系,是我们非常核心的技术优势之一。”
突破瓶颈,赋能研发之梦
大规模生产是创新疗法应用的关键,却也是整个行业亟待攻克的瓶颈。
在“自体型”细胞疗法中,单个批次的生产只能用于一位患者的治疗,耗时也较久,通常需要18-30天,进一步限制了患者的可及性。
然而,有很多病情严重的患者,其体内健康的免疫细胞数量本就已不多,身体状况也不适合进行进一步的工程化改造。即便完成了改造,也有很多患者等不起长达数周的生产过程。
许多生物技术公司正在研究“通用型”(也叫“现货型”)细胞疗法。这种疗法由健康人的免疫细胞制造,通用于更加广泛的特定人群,且如同常规的注射药品一样,能够预先大批量生产。患者一旦需要,可以及时进行治疗,不必经历漫长等待。如药明生基赋能的美国生物技术公司Wugen的新型免疫细胞疗法WU-NK-101近日也进入人体临床试验,该疗法已经被美国FDA授予了用于治疗AML(复发或难治性急性髓系白血病)的孤儿药资格。
当“通用型”的理想场景照进现实,CGT领域无疑会迎来一个新的高速增长。那么,如何在保证品质的前提下,实现单批次产能的有效提升?
聚焦合作伙伴不同的研发生产需求,药明生基一方面在细胞疗法的开发上前瞻性布局了自动化和生产过程的一体化集成,提高细胞产品的稳定性、一致性,降低生物污染风险,推动细胞产品生产更加高质量、低成本和个性化。“自体细胞疗法面临较长的等待和治疗周期,如果没有自动化,一家细胞治疗公司每年可能只能至多惠及1万名患者,但有了自动化,这一数字将有望提升至超过10万。”药明生基总裁兼首席技术官David Chang表示。
另一方面,药明生基不断拓展平台的技术能力,以攻克大规模生产病毒载体的挑战。其所拥有的新一代载体生产工艺——TESSA 技术(Tet Enabled Self Silencing Adenovirus),可以将AAV(腺相关病毒)载体产率提升30-40倍,实心率可以达到95%,从DNA到IND开发流程能够在12个月内完成,且生产规模可以革命性地跃升至2000L,有望通过一个批次生产,可供更多患者治疗。截至目前,药明生基能够提供三种技术平台TESSA Hybrid、TESSA Pro和TESSA Single,满足全球合作伙伴不同的AAV生产需求。此外,Lenti Stable细胞系则能够助力LVV(慢病毒载体)的大规模生产。
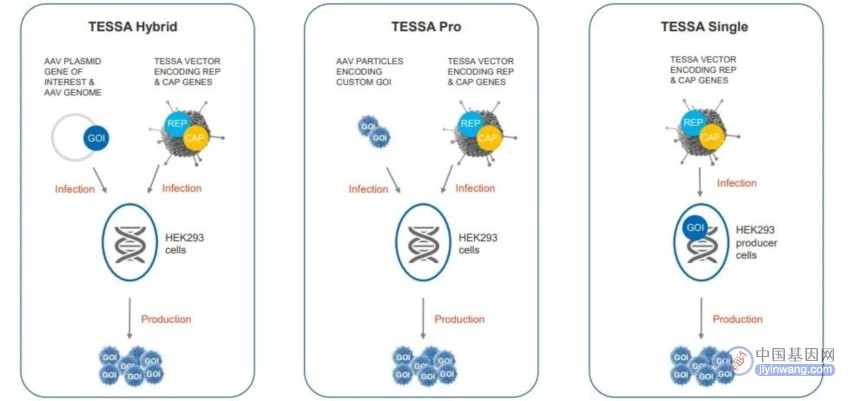
通过不断探索创新科技,药明生基不仅能够帮助全球创新合作伙伴,使其距离“现货型”细胞与基因疗法的问世更近一步,也持续助力全球CGT开发者突破病毒载体的产能瓶颈,降低CGT生产成本,从而改善患者可及性。
全球布局,释放无限潜能
通常,CGT药物临床阶段供应量在几十至一百人左右,但进入商业化阶段,其需求量可增加数十倍,对生产端造成很大压力。
与此同时,CGT药物对调配时效性有着很高要求。单从运输角度来看,大多数CGT药物需要在-80°至-180°C的温度下储存,否则存在降解的风险。以自体CAR-T药物为例,必须在极短时间内严控温度运输,并确保身份链和监管链完整。如果涉及不同国家及地区的远距离运输,成本又会大幅增加。
面对合作伙伴日益增长的需求,药明生基积极布局,在过去几年高效推进产能的全球化,分别在美国、英国、中国以及新加坡4个国家设立了基地。David Chang博士表示,“这些基地各有独特的价值定位,又能够紧密协同,赋能全球客户加速细胞与基因治疗产品的研发和生产进程,最终造福全球病患。”
其中,位于英国牛津的OXGENE是“创新中心”,专注于创新研发,特别是在病毒载体设计优化,以及开发新的生产技术方面,已经取得了诸多突破性成果。位于美国和中国的基地专注于开发和生产(D&M),美国费城基地可以提供独立的细胞和基因治疗测试服务,中国无锡基地更专注于提供CGT产品,并能提供独特的质粒载体。费城基地首席运营官RJ Fitch对各基地的协同合作感受深刻,“通过全球合作网络的联动,我们能够以更快的速度为客户提供更优质的服务。即使客户有更紧急的需求,但某个基地一时‘腾不出’产能,我们也能快速将生产安排在全球其他基地进行,避免由于场地原因造成项目延迟。”
就在去年,药明生基先是在4月与新加坡科技研究局(A*STAR)开展合作,以促进细胞和基因疗法领域的科研创新,同时建立联合人才发展计划,为行业培养下一代GMP生产领域的科学家和工程师;又于7月宣布在新加坡建立研发和生产基地,进一步夯实全球化运营网络。
据陈琪博士介绍,“新加坡的细胞治疗GMP中心会以商业化生产为主,预期在2026年建好首期。新加坡的产能建造以及落地将会更好地帮助我们在亚太地区赋能客户和病患的需求,将完全与我们美国、中国基地一样,在同一个质量体系下,执行生产以及检测放行,成为我们全球生产网络中重要的组成部分。”
畅想未来,引领产业变革
近日,药明生基战略合作伙伴德国基因治疗公司ViGeneron GmbH(ViGeneron)一款潜在的革命性基因疗法产品VG901通过欧洲药品管理局(European Medicines Agency, EMA)临床试验申请。药明生基CTDMO平台赋能VG901从开发直至临床获批,该产品适应症为CNGA1相关的视网膜色素变性症(Retinitis Pigmentosa,RP),目前业内尚无相关治疗药物获批上市。
作为一类全新的治疗模式,细胞和基因疗法大批进入临床应用的时间并不久。但就是在这短短几年里,许多生物医药公司勇敢涉足这一少有人走过的领域,为患者们带来了生命的希望。
现已问世的CGT主要集中于血液肿瘤或罕见病领域,而实际上,“实体瘤患者的数量是非实体瘤的几十上百倍,如果有可靠、可及的疗法,这将对每年数十万的患者群体产生巨大的价值。”David Chang博士指出,“为了助力这些疗法的研发和生产,药明生基也在提前准备,建立面积更小、周转更快、自动化程度更高的生产平台,赋能实现针对实体瘤或自身免疫性疾病的细胞疗法的突破,让创新疗法的生产稳定可靠、且更加可及。”
对药明生基而言,2023年会是里程碑式的一年,有四个潜在的商业化项目正在推进。这意味着药明生基将实现从赋能临床产品到赋能商业产品的重大跨越。
科学突破不仅影响着新兴疗法的下一步,更可能重塑治疗格局。畅想不远的未来,陈琪博士对CGT的前景充满信心:“行业的发展很可能会超出我们的想象。”在她看来,该领域3~5年内可能会发生很多的合作,促进创新技术更加可及。比如,基于AAV/LVV相关的体内治疗,有望走向商业化。“药明生基会拥抱新技术,更多地和客户进行一些项目早期的合作,不断对市场一些新技术进行前期的切入。”
我们期待,细胞与基因疗法终将逾越现有的障碍,发挥全部的潜能,让一次治疗、长久有效、潜在治愈的未来,真正来到每一位患者的身边。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。