光声非侵入手段激活瘤内基因编辑增效ACT疗法研究获进展
过继T细胞转移(adoptive T-cell transfer,ACT)疗法是颇具前景的肿瘤免疫疗法,但对实体瘤效果欠佳,亟需通过学科交叉来发展针对实体瘤增效的新理念和新技术。近日,中国科学院过程工程研究所生化工程国家重点实验室研究员魏炜团队与浙江大学药学院教授平渊团队交叉合作,通过非侵入手段激活实体瘤的基因编辑,同时调控实体瘤物理和免疫微环境,显著提升了多种ACT疗法对实体瘤的疗效。相关研究成果以 Non-Invasive Activation of Intratumoural Gene Editing for Improved Adoptive T-Cell Therapy in Solid Tumours为题,发表在《自然-纳米技术》( Nature Nanotechnology)上。
ACT疗法通过获取患者自身T细胞进行体外改造,使其回输患者体内后识别并攻击肿瘤细胞。然而,实体瘤细胞内的凋亡抗性保护其免于T细胞的杀伤,以及实体瘤细胞外的致密物理屏障、免疫抑制屏障等微环境限制了T细胞向实体瘤深处的浸润及杀伤功能的发挥,因而ACT对多数实体瘤疗效不佳。
面对以上挑战,魏炜团队基于多年肿瘤免疫治疗及生物剂型工程研究经验,与平渊团队展开交叉合作研究。双方在多维度协同改善细胞内凋亡抗性和细胞外微环境的新理念基础上,提出利用近红外光照射(NIR)或聚焦超声(FUS)非侵入性策略带来的温热效应,激活基因编辑敲除肿瘤细胞抗凋亡基因( HSP70和 BAG3),以及打破实体瘤的物理屏障和免疫抑制屏障。该工作通过上述协同作用,在动物肿瘤模型上显著增强了T细胞的瘤内浸润和对肿瘤细胞的杀伤效果。
其中,针对浅表肿瘤,科研团队发展了光驱动型基因编辑纳米器件(LEGEND),采用“纳米器件瘤周注射+NIR照射”的方式,在黑色素瘤等小鼠肿瘤模型以及人源化的患者来源肿瘤异种移植模型上显著提升了肿瘤浸润T细胞和嵌合抗原受体T细胞两种过继回输T细胞疗法的治疗效果。针对深部腔内肿瘤,该团队进一步发展了聚焦超声驱动型基因编辑纳米器件(FUGEND),采用“纳米器件静脉注射+FUS”的方式,在小鼠原位肝癌模型上同样证明了显著的ACT增效作用。
上述成果属于临床前研究,实际临床疗效仍有待进一步验证。鉴于该体系构建的通用性和灵活性,未来临床转化时可以按照不同治疗需求采用不同的基因编辑策略及非侵入操控方式。
近年来,过程工程所创制了一系列药物和疫苗递送新剂型,在动物模型上用于肿瘤、传染病、炎症性疾病的防治,同时,部分剂型已通过医院伦理批准进入个体化临床前和临床研究。
研究工作得到国家重点研发计划、国家自然科学基金和浙江省自然科学基金的支持。
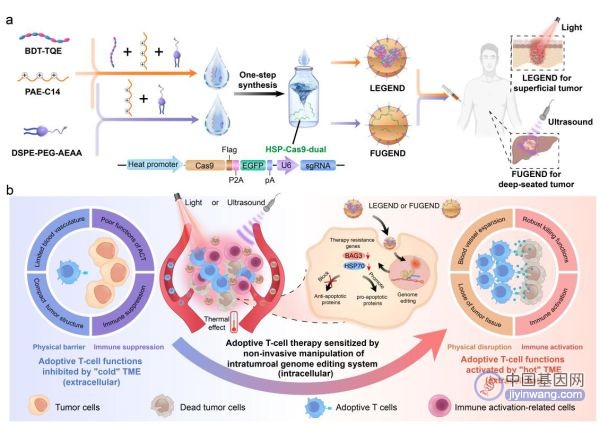
图1.光/声非侵入手段激活瘤内基因编辑增效ACT疗法的作用机制
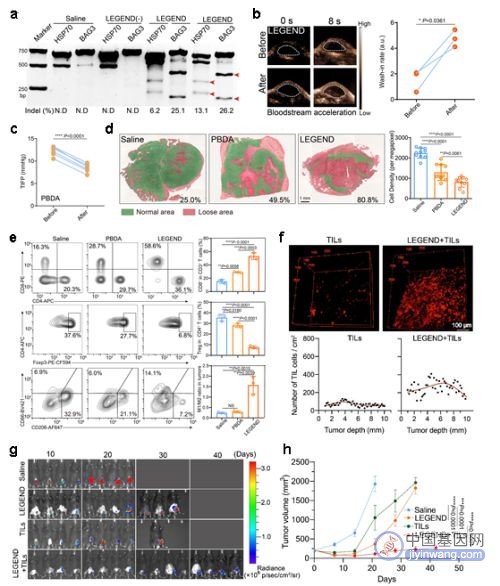
图2.LEGEND体系多维度协同改善细胞内凋亡抗性和细胞外微环境,提升TIL疗法治疗效果。a.LEGEND+NIR照射激活瘤内基因编辑,敲除肿瘤细胞抗凋亡基因(HSP70和BAG3);b-d.NIR温热效应打破实体瘤的物理屏障,包括血流加速(b)、间质压力降低(c)、组织疏松(d);e.NIR温热效应改善肿瘤免疫抑制微环境;f.LEGEND处理后显著增强TIL的瘤内浸润;g-h.LEGEND处理后显著提升TIL回输疗法的抑瘤效果。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。