基于CRISPR基因编辑技术治疗β0/β0型重度地中海贫血
β-地中海贫血是一种由于血红蛋白β链基因(β珠蛋白)异常引起的单基因遗传病。重型β-地贫患者严重缺乏或者不表达β-珠蛋白,导致成人血红蛋白(HbA)不足以及游离α-珠蛋白的有毒积累。如果没有接受定期输血,这些患者在出生后两年内就会发展为危及生命的溶血性贫血。目前,重型β-地贫的唯一治愈方法是异基因干细胞移植,然而由于免疫匹配供体的短缺,超过80%的患者无法及时找到匹配的供体。
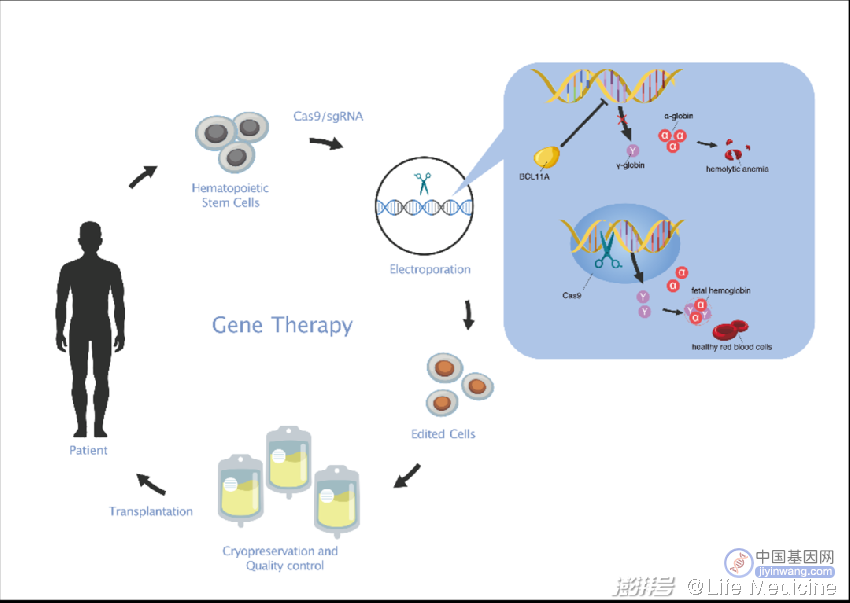
利用CRISPR/Cas9技术治疗β地中海贫血
近日,科研人员利用一种激活γ珠蛋白的策略治愈了β-地贫患者。早已有研究表明在胎儿发育的中后期直到新生儿出生后不久体内的血红蛋白主要为胎儿血红蛋白(HbF),由血红蛋白γ链与α链组成。出生后γ链才逐渐被BCL11A复合物沉默。研究人员将Cas9:sgRNA核糖核蛋白(RNP)电穿孔到纯化的造血干细胞中,靶向BCL11A基因的增强子区域,特异性的关闭了BCL11A在红系细胞中的表达,使患者体内恢复γ珠蛋白和胎儿血红蛋白,从而治愈了贫血症状并消除了游离α链毒性。

研究表明,接受治疗后两名患者在短期内便恢复了γ珠蛋的表达并脱离了输血依赖。整个临床试验并未发现严重的不良反应。Circle-seq也未检测到Cas9引起的脱靶。编辑后的干细胞多能分化能力未受影响,同时没有发现恶性克隆。总体来讲,该临床研究获得了突破性的成功。联合研究团队将继续对受试者进行跟踪随访已确定该治疗策略的长期安全性。由于CRISPR技术已经融入了许多其他成熟的生物技术,我们可以预见在不久的未来,将会有大量的CRISPR相关临床应用得以开展,更多的遗传病、难治疾病、甚至癌症的治疗能够得到突破。
英文全文链接:
https://doi.org/10.1093/lifemedi/lnad009
引用本文:
Liren Wang, Stefan Siwko, Dali Li, Waking up the silenced beauty: CRISPR/Cas9 mediated reactivation of fetal hemoglobin genes to treat severe beta-thalassemia in young patients, Life Medicine, 2023;, lnad009, https://doi.org/10.1093/lifemedi/lnad009
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。