细胞与基因治疗研究核心之病毒基因导入平台,你了解多少?
细胞与基因治疗作为治疗人类疾病、维护人类健康的很有发展前景的手段之一而备受关注。像一些难治性肿瘤、常见和罕见遗传性疾病,或者使用传统的治疗手段难以治愈,或者难以使用传统方法来治疗,细胞与基因疗法或将成为治疗这些疾病的有效手段。
在细胞和基因治疗研究中,病毒基因导入平台成为主要的基因导入手段。目前常用的病毒载体包括慢病毒、逆转录病毒、腺相关病毒、腺病毒等等。与逆转录病毒和腺病毒相比,慢病毒和腺相关病毒因为安全性较好,使用比例大幅提升,但逆转录病毒和腺病毒也有一定应用。
今天我们为大家介绍几个病毒基因导入平台的异同。
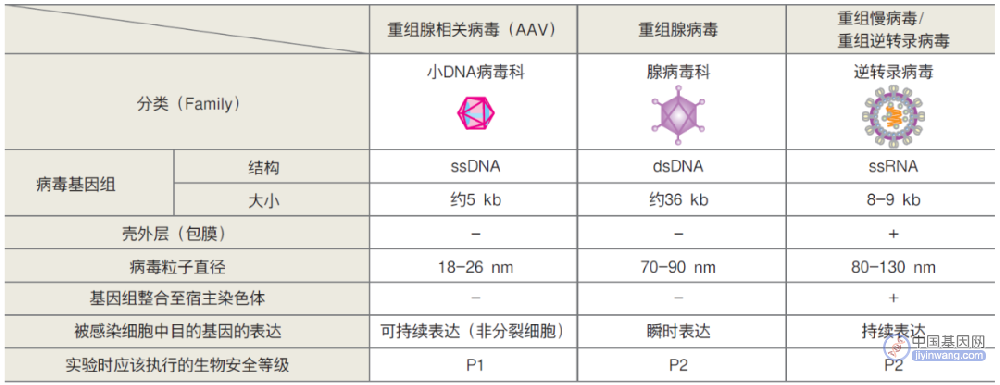
01
慢病毒(Lentivirus)
慢病毒是目前细胞与基因疗法研究,尤其是CAR-T细胞治疗,所使用的主要基因导入平台。慢病毒是单链RNA病毒,一般以人类免疫缺陷病毒1型(HIV-1)为基础开发的居多,可用于绝大多数哺乳动物细胞基因导入,包括使用逆转录病毒难以实现的造血干细胞及神经细胞等在内的非分裂细胞。使用重组慢病毒导入的目的基因也可以整合到宿主细胞的基因组中,可实现长期稳定的基因表达。
慢病毒表达载体
慢病毒表达载体是所有慢病毒基因导入系统的关键参与者。野生型慢病毒基因组约为9.7 kb(包含两个LTR)。人工构建大于此长度的基因组,将导致产生不稳定的病毒粒子和病毒滴度的明显下降。对于慢病毒表达载体来说,大部分病毒基因组已经被其他有用的序列所取代,如筛选标记或荧光蛋白质基因,但仍有足够的空间用于目的基因克隆。
由于每个慢病毒表达载体含有的有用序列不同,因此克隆转基因的可用空间也有所不同。经过优化的慢病毒表达载体,除了含有HIV-1 LTR和慢病毒包装信号(Ψ),也会包含一些特定元件(cPPT/CTS,RRE,WPRE),这些特定元件的存在有助于改善转基因表达、病毒滴度和整体慢病毒载体功能。
慢病毒包装制备
使用重组慢病毒的生物安全问题是,可能会产生致癌病毒或具有复制能力的重组慢病毒(RCL)。然而这些担忧,可以通过仔细考虑转基因插入物的性质,并确保病毒复制仅限于发生在提供这些基本功能的特定包装细胞中,而得到大大缓解。因此,重组慢病毒可以安全使用,是将外源性遗传物质单向转移到靶细胞的有用工具。
重组慢病毒的包装细胞一般为HEK 293T细胞,选择易于传染并能够高水平表达病毒蛋白的HEK 293T细胞,更有利于获得高病毒滴度。就慢病毒包装系统而言,目前市面上主要是第三代和第四代慢病毒包装系统,大家了解较多的是第三代包装系统,对第四代系统了解较少。
以Lenti-X™第四代慢病毒包装系统为例,这款包装系统Tet-Off和Tat反式激活因子驱动病毒必需成分高水平表达,诱导级联表达反应,从而可以制备出高滴度慢病毒,VSV-G型包装系统病毒滴度可达到107–108IFU/ml。另外,pol基因与vpr基因的融合可以确保反转录酶/整合酶蛋白质能够转运到重组慢病毒颗粒中。
慢病毒一般实验流程
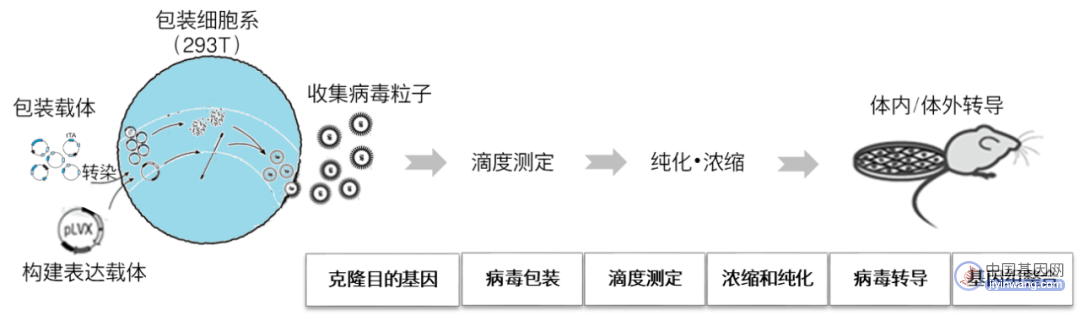
02
逆转录病毒(Retrovirus)
逆转录病毒在基因治疗方面有着丰富的应用实绩,但由于它相对慢病毒更容易引起插入性随机突变,近几年来应用较少。逆转录病毒也是单链RNA病毒,一般基于莫罗尼小鼠白血病病毒(MoMLV)开发。逆转录病毒能够将基因导入至多数处于增殖期的细胞中,由于导入基因可整合到染色体中,因此可以实现长期稳定的基因表达。重组逆转录病毒制备相对容易,但仍然需要在P2级实验室条件下操作。
逆转录病毒表达载体
野生型莫罗尼小鼠白血病病毒(MMLV)基因组约8.2 kb(包括两个LTR)。人工构建一个大于8.2 kb的基因组,同样也会导致产生不稳定的病毒粒子和病毒滴度的下降。与慢病毒表达载体相类似,大部分病毒基因组已被其他有用的序列(如筛选标记或荧光蛋白基因)取代,但仍有足够的空间用于克隆转基因。由于不同逆转录病毒表达载体包含的有用序列不同,因此用于克隆转基因的可用空间也不同。
逆转录病毒包装制备
与慢病毒相似,重组逆转录病毒也会有产生RCL的可能性,所以逆转录病毒包装质粒也会进行特别设计。病毒包装用质粒上插入有逆转录病毒的结构基因,gag-pol和env基因,这两种基因是逆转录病毒构建和复制所必需的基因,但是质粒上缺少包装信号Ψ序列和LTR序列,因此包装用质粒本身是无法包装成逆转录病毒的,只有将其和包含Ψ序列和LTR序列的逆转录病毒表达载体共转染到293或者293T包装细胞中,才能包装得到逆转录病毒,产生具有自我复制能力逆转录病毒的几率也非常低。
为方便使用,可以构建gag和pol基因稳定表达细胞系,作为逆转录病毒包装细胞。这样将含有env基因的表达质粒和克隆了目标基因的表达载体共转染包装细胞,就可以制备出重组逆转录病毒了。这样的包装细胞系,有助于降低转染难度,提高成功率。
逆转录病毒一般实验流程
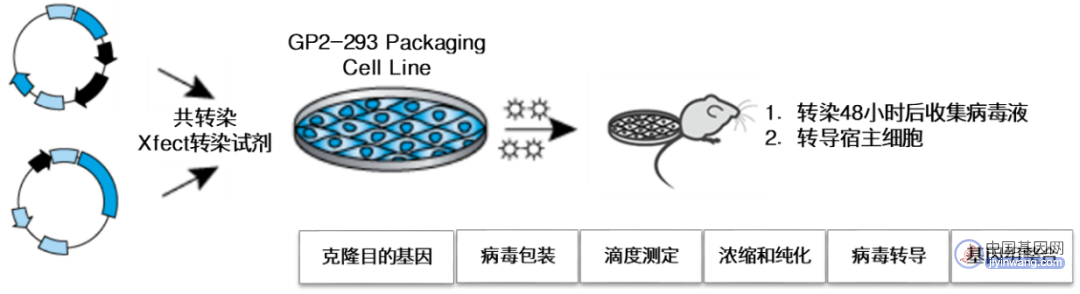
以稳定表达gag和pol基因的GP2-293包装细胞为例
03
腺相关病毒(Adeno-Associated Virus)
作为体内基因导入主要平台之一,腺相关病毒(AAV)已经在多个遗传性眼科疾病治疗临床试验中显现出有明显的治疗效果,而且不会引起显著的不良免疫反应。AAV也是一种广泛应用于癌症基因治疗的病毒载体。多种AAV载体已被用于肿瘤治疗,众多临床前研究结果显示,AAV基因治疗成功抑制肿瘤生长,致使肿瘤消退。另外,AAV还广泛应用于血液病、代谢类等疾病的治疗研究,展现出了广阔的应用前景。
由于AAV免疫原性和细胞毒性低,能够转导非分裂细胞,并且整合到宿主基因组中的频率非常低,因此被众多研究学者认为安全性更高。经过重组和改造的AAV拥有不同的血清型,根据血清型不同而具有不同的宿主范围和病毒特征,可以有效作用于特定细胞类型,包括分裂和非分裂细胞类型。使用者需要根据靶标细胞或者组织类型选择适合的血清型。目前使用频率较高的血清型为AAV2,其它血清型也逐渐被广泛使用。
AAV基因组结构
AAV基因组是约4.7 kb的单链线状DNA分子,在两端都有被称为反向末端重复序列(ITR)的发夹结构。ITR的功能在于基因组复制起始位点及辅助病毒粒子包装。AAV基因组包含了3个开放阅读框:Rep编码参与复制和转录的蛋白质;Cap编码病毒衣壳蛋白质;AAP编码用于病毒粒子形成的非结构蛋白质。Rep区域编码4种不同的蛋白质(Rep78, Rep68, Rep52和Rep40),Cap区域编码3种不同的蛋白质(VP1, VP2 和VP3 )。
AAV包装制备
一般来说,AAV只有在辅助病毒(如腺病毒或疱疹病毒)存在下才能复制。目前,AAV的包装制备大多使用无辅助病毒包装系统,也就是在不使用辅助病毒的情况下制备重组AAV。AAV的制备也是通过将编码重组AAV所需因子的质粒转染HEK 293细胞来完成的。制备AAV载体一般需要以下3种质粒:含有目的基因表达框和2个ITR的质粒,包含AAV2 Rep基因和各种血清型Cap基因的质粒,包含腺病毒E2A、E4、VA基因的质粒。
AAV一般实验流程
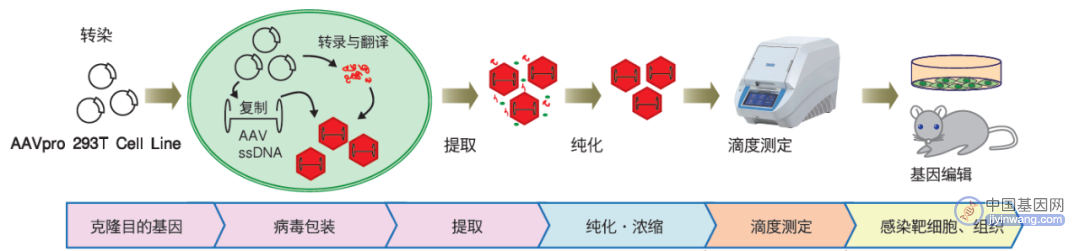
04
腺病毒(Adenovirus)
腺病毒是将基因导入哺乳动物细胞的可靠平台之一,早先也被应用于基因治疗研究,但现在应用较少。腺病毒的感染不依赖于细胞周期,所以可以将目标基因传递给原代或者经过转化的细胞系。在感染后细胞中,由于重组腺病毒基因组以多拷贝形式存在,目标基因将以高水平瞬时表达,腺病毒具有在哺乳动物细胞中高效生产蛋白质的优势。此外,腺病毒能够感染多种不同动物物种的增殖和静止细胞类型,适用范围广。
腺病毒表达载体
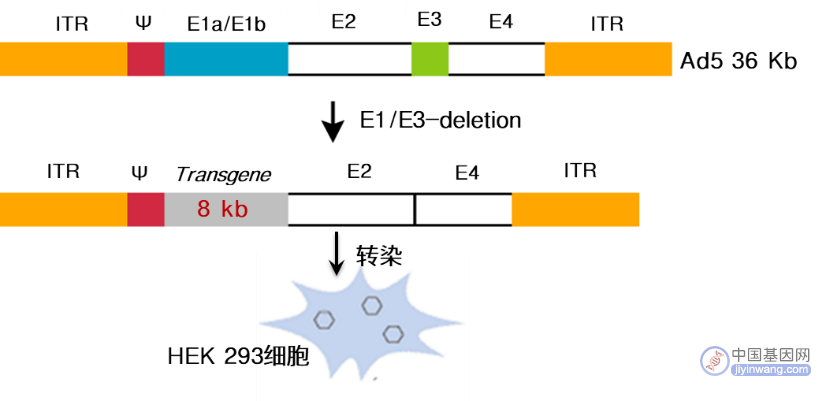
腺病毒是一种线性双链DNA病毒,目前多使用人5型腺病毒,这种病毒DNA基因组约36 kb,基因组两端包含反向末端重复序列(ITR)。常用的腺病毒表达载体,删除了早期转录复制基因E1和E3。由于E1和E3基因的缺失,腺病毒载体可插入约8 kb的外源基因。由于腺病毒载体大,克隆难度也高。传统方法是借助穿梭载体作为中间过渡,首先将目的基因克隆到穿梭载体,然后再重组到腺病毒病毒DNA上;当然也可以借助先进的克隆技术(In-Fusion®等)一步完成,高效方便。
腺病毒包装制备
E1基因对腺病毒的复制和转录至关重要,E3基因的缺失不影响腺病毒的复制。所以腺病毒包装必需依赖于表达E1基因的细胞系,比如HEK-293等。在包装前,需要将克隆了目的基因的重组腺病毒载体线性化,以暴露位于腺病毒基因组两端的反向末端重复序列(ITR),并从质粒骨架释放腺病毒基因组。原因是ITR包含腺病毒DNA复制起点,必须位于线性腺病毒DNA分子的末端,以支持复制复合物的形成。
线性化重组腺病毒载体转染HEK-293包装细胞,大约一周左右可以收获重组病毒。这部分病毒将被作为病毒种子再感染HEK-293包装细胞,使其自我复制来获得更高病毒滴度,再次收集病毒感染目标细胞。
腺病毒一般实验流程
05
病毒基因导入系统“专家”
Takara Bio想必大家并不陌生,甚至可能是很熟悉了。Takara Bio作为重要的生物技术企业,在病毒基因导入系统方面造诣颇深、体系完备,拥有慢病毒系统、逆转录病毒系统、腺相关病毒系统、腺病毒全套解决方案,为细胞与基因治疗研究护航加码。
慢病毒系统⇒ Lenti-XTM系列
慢病毒包装系统
Lenti-X Packaging Single Shots
第四代包装系统,高滴度,一步操作
慢病毒滴度测定&浓缩
Lenti-X p24 Rapid Titer Kit – ELISA法
Lenti-X GoStix Plus - 10 min定量测定
Lenti-X Concentrator – 高达100倍浓缩
慢病毒转导增强
RetroNectin GMP grade
已用于超过68种基因治疗临床试验方案
逆转录病毒系统⇒Retro-XTM系列
逆转录病毒包装系统
Retro-X Universal Packaging System
提供四种包膜质粒,按需选择
逆转录病毒滴度测定&浓缩
Retro-X qRT-PCR Titration Kit - qRT-PCR法
Retro-X Concentrator – 高达100倍浓缩
逆转录病毒整合位点分析
Retro-X Integration Site Analysis Kit
确认转导细胞基因组中的整合位点
腺相关病毒系统⇒ AAVpro®系列
腺相关病毒包装系统
AAVpro Packaging Plasmid(AAV1-6)
引入hsa-miR-342,滴度增加约2倍
腺相关病毒滴度测定
AAVpro Titration Kit Ver.2– qPCR法
腺相关病毒纯化和浓缩
AAVpro Purification Kit
通用型,用于从包装细胞纯化病毒
AAVpro Concentrator
通用型,用于从培养上清液中纯化病毒
腺病毒系统⇒ Adeno-XTM系列
腺病毒表达系统
Adeno-X Adenoviral System 3
无需穿梭质粒的表达系统,简便易用
腺病毒滴度测定
Adeno-X Rapid Titer Kit – ELISA法
Adeno-X GoStix - 10 min半定量测定
Adeno-X qPCR Titration Kit - qPCR法
腺病毒纯化
Adeno-X Purification Kit
色谱纯化方法
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。