Nature Medicine:AAV基因治疗酗酒,一次治疗,长期有效

众所周知,喝酒有害健康,许多研究表明,酒精是一种致癌物,喝酒与包括癌症在内的一系列伤害和疾病有关。
2018年8月,国际顶尖医学期刊《柳叶刀》发表了一项对全球195个国家和地区的酒精使用负担的大型研究,该研究指出酒精是全球15-49岁男性和女性患病和早逝的主要风险因素,全球近十分之一的死亡人数是饮酒所致【1】。
据统计,全球有近三亿人患有酒精使用障碍(AUD),他们通常会经历反复的戒酒周期,然后再复发,即使使用FDA批准的戒酒药物也是如此。
2023年8月14日,俄亥俄州立大学、俄勒冈健康与科学大学、维克森林大学医学院、加州大学旧金山分校的研究人员在国际顶尖医学期刊 Nature Medicine 上发表了题为:GDNF gene therapy for alcohol use disorder in male non-human primates 的研究论文【2】。
这项在非人灵长类动物恒河猴中的研究证明,使用腺相关病毒2型(AAV2)向中脑腹侧被盖区(VTA)递送人胶质源性神经营养因子(hGDNF),能够减少酒精使用,防止戒酒后的酒瘾复发。
论文通讯作者 Krystof Bankiewicz 教授表示,该基因疗法靶向长期饮酒引起的中脑边缘奖赏通路中的多巴胺功能的改变,实验结果显示,这种基因疗法可以防止戒酒后的酒瘾复发,可能为严重酒精成瘾(也称为酒精使用障碍)患者提供一次性、持续的治疗。

过量饮酒会改变中脑边缘奖励通路腹侧被盖区(VTA)神经元的神经递质多巴胺的释放,随着酒精使用障碍(AUD)的发展,这些改变会更加明显,它们包括多巴胺释放水平降低,多巴胺受体敏感性降低和多巴胺摄取增加。这些变化导致通路中的多巴胺水平低于正常水平。这种“低多巴胺能”状态会迫使他们在戒酒一段时间后重新开始饮酒。目前还没有治疗方法或药物能够靶向这一通路。
在这项研究中,研究团队在非人灵长类动物恒河猴进行了研究,使用腺相关病毒2型(AAV2)递送人胶质源性神经营养因子(hGDNF),GDNF是一种增强多巴胺能神经元的生长因子。将AAV2-hGDNF注射到8只恒河猴中脑腹侧被盖区(VTA),表达胶质源性神经营养因子,另外4只恒河猴按同样的程序注射无菌生理盐水作为对照组。
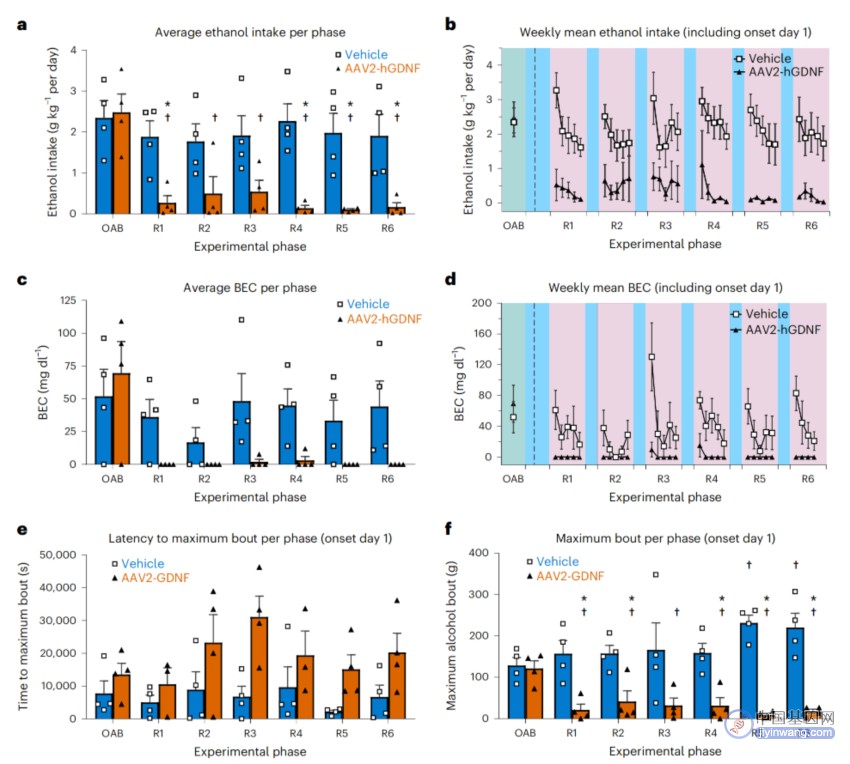
这些恒河猴在治疗前习惯于饮用4%的酒精,在接受治疗后,治疗组恒河猴的大脑中持续表达了人胶质源性神经营养因子(hGDNF),并在之后的12个月的反复戒酒-重新引入酒精挑战期间消除饮酒行为的复发,这种行为改变伴随着伏隔核多巴胺信号的神经生理调节,这种调节抵消了与慢性酒精使用相关的低多巴胺能信号状态,这表明了针对中脑腹侧被盖区(VTA)的GDNF基因治疗能够减少酒精使用、防止戒酒后的酒瘾复发,可能是酒精使用障碍(AUD)的潜在治疗策略。
论文链接:
1. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(18)31310-2/fulltext
2. https://www.nature.com/articles/s41591-023-02463-9
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。