中国医生在欧洲介绍全球首个先天性耳聋基因疗法重大突破
10月27日,舒易来医生在第30届欧洲基因和细胞治疗学会年会上分享了基因治疗药物RRG-003的全球首批多例基因治疗临床试验结果,其数据显示,5例患者中4例患者治疗后有明显的听力改善,并且耐受性和安全性良好。

舒易来医生在第30届欧洲基因和细胞治疗学会年会上作报告
视频中,一个小男孩背对镜头,母亲在他背后大喊了一声,他转过头来……小男孩的父母在视频画面上标记,这是他接受基因疗法RRG-003后的第28天。
近日,复旦大学附属眼耳鼻喉科医院(上海市五官科医院)耳鼻喉科研究院副院长、遗传性耳聋诊治中心主任舒易来医生在接受澎湃科技采访时介绍,这个小男孩今年两岁,患有先天性耳聋,接受治疗已经6个月。据小男孩母亲介绍,治疗前,他对任何声音都没有反应,无论是鞭炮声还是打雷声。因为听不见,之前他敲门都没有敲出声音,单纯模仿敲门的动作。
男孩母亲告诉舒易来团队:“治疗后并没有立刻起效,第14天时,孩子还不会对声音做出反应。我们很紧张。差不多一个月才看到效果,我们一家人激动得都哭了。”舒易来告诉澎湃科技:“我看到的时候,也觉得很欣慰、很开心。”
先天性耳聋,指因遗传因素或母体妊娠过程、分娩过程中的异常造成的听力障碍。患有先天性耳聋的儿童可能从小就无法接收到声音的刺激,往往因聋致哑,既听不见声音,也无法说话。由中国听力医学发展基金会发布的《中国听力健康报告(2021)》显示,中国新生儿耳聋发病率为1‰-3.47‰,每年新增耳聋新生儿约3万人,其中遗传因素致聋的比例达60%。
10月27日,舒易来在比利时布鲁塞尔举行的第30届欧洲基因和细胞治疗学会年会(ESGCT)上,向全球同行分享了团队与上海鼎新基因科技有限公司(以下简称“鼎新基因”)联合研发的基因治疗药物RRG-003的全球首批多例基因治疗临床试验结果,其数据显示,5例患者中4例患者治疗后有明显的听力改善,并且耐受性和安全性良好。
鼎新基因负责该项目执行的科学家高凯瑜博士称:“这是在中国上海自主完成的、全球第一项获得疗效的内耳基因治疗和双AAV载体的人体试验(Frist in human),临床意义重大,双载体技术路线、内耳给药、患儿听力评估以及语言功能恢复均是世界级的开创性工作。”
或可改变无药可治的局面
目前,全球尚无可治疗感音神经性耳聋的药物上市,主流的临床干预方式是助听器、人工耳蜗植入。人工耳蜗是模拟人类耳蜗工作原理的电子植入体,可以将声音信号转换为电信号,绕过损坏的耳蜗毛细胞,直接刺激耳蜗听神经,将声音信号发送到大脑里,使人产生听觉。也就是说,人工耳蜗是用电极、芯片、编码策略制造出来的电子音模拟人耳听到的自然声音。
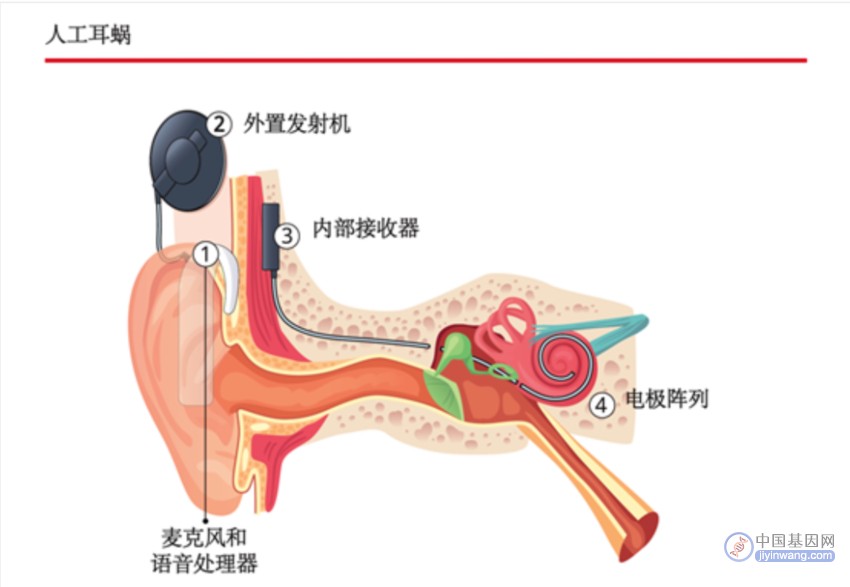
人工耳蜗。图片来源:世界卫生组织《世界听力报告》
既有人工耳蜗,为什么还需要基因疗法?据报道,人工耳蜗让很多聋哑儿童回到了有声世界,能与人交流,是听觉领域重大的发明和创造。患者通过人工耳蜗听到的声音,要经过长期的训练和学习这些“电波”的意义,而且在很多人同时说话或嘈杂环境中时,分辨率会下降。再者,手术植入人工耳蜗后,患者需要在耳朵附近长期佩戴外机,外机关闭或没电时,他们就听不见了。
上海市五官科医院耳鼻喉科主任李华伟教授表示,基因治疗是针对病因的治疗方法,患儿在接受基因治疗后,听见的声音和普通人无异,而且从外表也看不出治疗的痕迹。
“RRG-003是靶向OTOF基因的基因治疗药物。受试患者的OTOF基因有缺陷,无法正常地发挥作用,我们使用AAV载体将正常的基因注射到患者的耳朵里,它可以产生正常蛋白,弥补患儿本身的基因缺陷,让他们的听觉重新恢复。”舒易来解释。
OTOF基因编码一种与囊泡释放功能相关的“耳畸蛋白”。该基因突变可导致耳畸蛋白功能缺陷从而引起明显的听力障碍。过往的研究表明,OTOF是最有潜力率先实现耳聋治疗临床转化的靶向基因。
在启动人体临床研究之前,舒易来在先天性耳聋基因疗法研究的路上已经走了十多年。据其介绍,目前已有150多种基因被鉴定与先天性耳聋有关,其研究团队正在尝试的多个靶点基因在动物模型上也初见疗效,OTOF是第一个走上人体临床试验的。
在这项临床研究中,舒易来团队采用耳部注射的方式,实现了双载体AAV药物治疗先天性耳聋的全球首批临床给药。舒易来解释,之所以采用双AAV载体递送,是因为OTOF基因比较大,超过了AAV载体的装载容量,“打个比方,一辆车搬不动它,需要两辆车一起搬,药物注射入人体后,这两辆车就合并起来,形成了一个完整的基因。”
据悉,该研究纳入的第一批患者年龄为3-10岁,在确认安全性和有效性后,研究团队逐步放宽年龄限制,第二批患者招募时,1-3岁符合条件的患者也可以入组。舒易来表示,这项工作的开展离不开医院的大力支持,也离不开科主任李华伟教授的带领和一直以来的支持。
该临床试验从2022年10月开始正式启动患者招募,“招募信息发出后,当天就有好多人来联系我们。我们从中筛选出几位患者,都是耳聋程度特别严重,对声音没有反应的儿童。之所以选择这类儿童,是因为用药的效果在他们身上会被反映得更加容易判断。针对第一批患者,我们也更加注重安全性。” 舒易来说。
未来将继续随访
2022年12月28日,在李华伟教授的带领和支持下,舒易来团队进行了全球第一例先天性耳聋患儿的基因治疗,目前,该患儿的听力恢复已经持续了10个月。在安全性方面,舒易来表示:“局部注射大大降低了发生潜在风险的可能性,同时我们使用的剂量也很低。”
值得关注的是,招募的5位患儿中有1位的听力没有成功得到改善,舒易来分析了可能的原因:“我们发现这个儿童体内的AAV载体抗体水平比别人高很多,说明他以前可能接触过AAV。”
AAV虽然是一种免疫原性很低的载体,但仍然会引起人体的免疫反应。有数据显示,40%-80%的成人曾经历过AAV感染,人体内已经存在的针对AAV的中和抗体,成为AAV载体递送的一项可能的重大挑战。对此,舒易来表示,团队在手术前会检查患者体内的抗体水平,如果他/她曾经对AAV暴露过,相应抗体水平过高,就不会被纳入试验组。另一方面,目前临床试验中的儿童均只在一只耳朵中注射了RRG-003,而注射过RRG-003后,患儿体内也会产生抗体,另一只耳朵的注射可能要等很长一段时间。
为确保安全性和有效性,舒易来团队计划对这两批首先入组的患者继续观察,如果可能的话,会一直随访下去。同时,其研究团队也正在开发一些针对其他耳聋基因的基因疗法。希望有更多新的治疗药物被研发出来,让更多患者回到有声世界。
目前,全球已上市的基因疗法大多定价昂贵,普通家庭几乎难以负担。舒易来表示,解决这一问题的一种方式是纳入医保,另一个办法是按年付费。同时,整个医学界和产业界要共同努力降低成本,从而降低价格,惠及更多的患者。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。