3天令一个杜氏肌营养不良孩子重获新生,这款基因疗法能如期获批吗?
“如果这种疗法能让我的儿子多活一天,那就是一种治愈。这就是我所看到的。”
——布伦特·弗比,杜氏肌营养不良患童父亲

▲Furbees一家(图片来源:参考资料[1],Courtesy by Furbee Family)
照片中笑容灿烂的三口之家是田纳西州的一个普通家庭。谁也不会想到,中间的小男孩身患一种名为杜氏肌营养不良(DMD)的致命隐性遗传病。这种疾病在全球范围内的发病率为1/3500,几乎只在男性中发病。相比于正常人,DMD患者不仅会逐渐失去生活自理能力,平均寿命也远低于健康人。为了尽可能延长儿子小艾默生(Emerson)的生命,弗比夫妇踏上了艰难的求医问药之路…
曾经无药可医,一剂基因疗法使艾默生重获新生
从外表上看,艾默生与同龄的健康儿童无异,只有最亲近的家人通过细心观察才能看出一些端倪——小艾默生在上音乐课时会无故摔倒,在操场上攀爬游乐设施时也非常艰难。然而,医生一开始没发现艾默生有什么问题,对于弗比夫妇指出的艾默生身上的那些异常现象,她将之归结为艾默生的扁平足带来的小问题。
弗比夫妇对这个解释半信半疑,三个月后,他们又带艾默生进行了复查。这一次,医生通过血液检查找到了艾默生的真正病因——DMD。DMD是一种由编码肌营养不良蛋白的基因发生突变引起的遗传病,而肌营养不良蛋白是维持肌肉功能所必需的蛋白质。
在健康的肌肉组织中,肌营养不良蛋白就像一个减震器,能在肌肉细胞收缩和舒张时起稳定作用。而患有DMD的患者产生的肌营养不良蛋白很少或者根本就不生产。因此对于DMD患者来说,即使是日常的行为活动也会对肌肉造成伤害,使之逐渐分崩离析。而现在,医生在小艾默生的血液中已经检测到了他的肌肉正在崩溃的证据,一种肌肉细胞中的基本成分——肌酸激酶已经大量进入了艾默生的血液,显著高于正常水平。
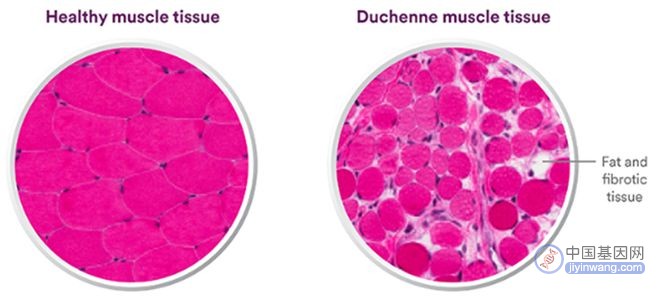
▲健康肌人的肉组织(左)与DMD患者的肌肉组织(右)的对比图(图片来源:Sarepta公司官网)
随后的消息对弗比夫妇来说更是有如同晴天霹雳。医生表示,根据近两个世纪的医学观察写成的数千篇论文的结果,小艾默生的未来已清晰可见——由于目前没有好的治疗方法,他的症状会逐渐恶化,极大概率会在12岁时坐上轮椅,然后在30岁或至多40岁时死去。
尽管医生已经给小艾默生宣判了死刑,弗比夫妇并没有就此放弃。2019年艾默生确诊后,他的园艺师父亲布伦特(Brent)自学了生物学知识,并十分留心该疾病的治疗领域是否有新的进展。某天晚上,布伦特从网上发现了一种新型基因疗法正在招募临床试验的患者,它或许能够治疗艾默生的病。在深入了解后,他毫不犹豫地展开了为艾默生争取临床试验入组资格的行动,包括举家搬迁到纳什维尔郊区从而使艾默生获得专门的护理,以及给该疗法在全美各个试验点的负责医生发送加入临床试验的申请邮件。
功夫不负有心人,2021年2月,小艾默生终于获得了参加临床试验的资格。那时候,艾默生的症状已经进一步恶化了,他的下肢力量已无法支撑他一步一个台阶地走上楼梯,只能先把两只脚都搬上同一级台阶,然后再费劲地搬向下一级台阶。好消息是,他很快便能尝试有望改变他命运的治疗方法了。
3月22日早上7点30分,弗比一家准时到达了为艾默生提供治疗的圣路易斯儿童医院(St. Louis Children’s Hospital)。为了使艾默生勇敢起来,布伦特告诉艾默生,他将接受的治疗就是使美国队长变得强大的神秘血清。那是艾默生最喜欢的超级英雄,在治疗当天,他还穿着印有美国队长图案的睡衣。艾默生还得知,如果他勇敢尝试的这种疗法有效,它还有望帮助其他像他一样具有“特殊”肌肉的男孩们。
小艾默生似乎理解了自己肩负的重要使命,他严阵以待,尽自己最大的努力完成了护士指挥他做的所有动作——这将确保药物能够充分分布到他的全身。治疗很快就结束了,到中午时,小艾默生就已出院了。
3天后,这种疗法的惊人效果完全超出了弗比夫妇的预期——艾默生已经可以一步接一步地上楼梯了!11天后,艾默生能够独自骑三轮车。那年夏天,艾默生甚至能够打儿童棒球了。现在,距离艾默生接受治疗已过去两年,6岁的他不仅看上去与普通孩子无异,甚至还很健壮。

▲艾默生4岁,治疗前8个月时的照片(左)和治疗后两年时的照片(右)(图片来源:参考资料[1],Courtesy by Furbee Family)
布伦特开心地表示:“从来没有一位家长问过我们,‘艾默生怎么了?’艾默生和其他孩子相比没有明显的区别。”这种疗法给艾默生带来的巨大转变太过神奇,布伦特由衷地希望每个像他们一样的家庭都能发生同样的“奇迹”。事实上,他的愿望很可能快要实现了。
治好艾默生的这款疗法名为SRP-9001,是Sarepta公司与罗氏公司合作开发的针对DMD的基因疗法。2022年9月,Sarepta已美国FDA提交了一份生物制品许可申请(BLA),以寻求SRP-9001的 。FDA随后授予了它 ,预计将于2023年5月29日前公布审评结果。如果获批,SRP-9001将成为首个治疗DMD的基因疗法。那么这款神奇的疗法是如何诞生的呢?
一款在酒吧中“诞生”的基因疗法
2015年11月,Sarepta当时的业务发展主管波·卡姆博(Bo Cumbo)先生在伦敦参加了DMD的研究会议。会议结束后,他在附近的一家酒吧中与同样与会的英国科学家乔治·迪克森(George Dickson)博士喝酒闲谈。当聊到DMD疗法的未来时,迪克森博士给卡姆博先生展示的一段视频令他感到难以置信。
视频的一开始出现了一只年轻的金毛猎犬,由于抗肌萎缩蛋白基因受损,它的走路姿势摇摇晃晃,脚步虚浮。当实验人员拿出食物和玩具试图引诱它跨过一道低矮的障碍物时,金毛有心无力,只能跟着实验员左右移动。镜头随后转到了一只类似的患有DMD的金毛身上,不同的是,这只金毛接受了由法国的研究小组Genethon开发的早期矫正基因疗法,因此它像正常的金毛一样在走廊上活蹦乱跳,并轻而易举地跳过了低矮的障碍物吃到了实验员手上的零食。
这个视频深深地震撼了卡姆博先生,他意识到DMD患者的未来掌握在基因疗法手上。当即,他给Sarepta当时的首席财务官桑迪·马哈特姆(Sandy Mahatme)先生打了电话:“桑迪,我们必须立即获得许可。”
随后,从2015年年底到2016年年初,Sarepta的管理团队开始制定基因治疗的战略。而后续一系列的工作也在争分夺秒地开展,例如获得足够公司继续运营的资金、拿到最可能有效的基因疗法的许可、接洽有可能开发DMD疗法的医院等等。
2016年7月,Sarepta当时的首席执行官艾德·凯伊(Ed Kaye)博士会见了全球知名的DMD医生——俄亥俄州全国儿童医院(Nationwide Children's Hospital)的杰里·门德尔(Jerry Mendell)教授,他在过去20多年的时间里一直在致力于开发一种基因疗法。在所有早期基因疗法中,门德尔教授士正在开发的项目是最有可能获得成功的,这款疗法的临床前证据充分,正准备进入临床试验。由于凯伊博士同为医生和科学家的身份,他很快便获得了门德尔教授的认同,并成功与门德尔教授签订了其在研基因疗法的独家许可协议。自此,SRP-9001的开发便正式步入了正轨。

▲Jerry Mendell教授(图片来源:Child Neurology Society官网)
由于基因疗法在当时都尚处于测试阶段,尽管门德尔教授万分确信他的基因疗法能够在临床试验中取得好的结果,保守起见,Sarepta对于这款早期的基因疗法一开始没有过多向外界透露,就连凯伊博士的继任者、Sarepta的现任首席执行官道格拉斯·英格拉姆(Doug Ingram)先生也是在接手Sarepta后才知道SRP-9001项目的存在。好在,SRP-9001并没有让大家失望。
小规模临床试验大获成功,首个安慰剂对照研究却意外失利
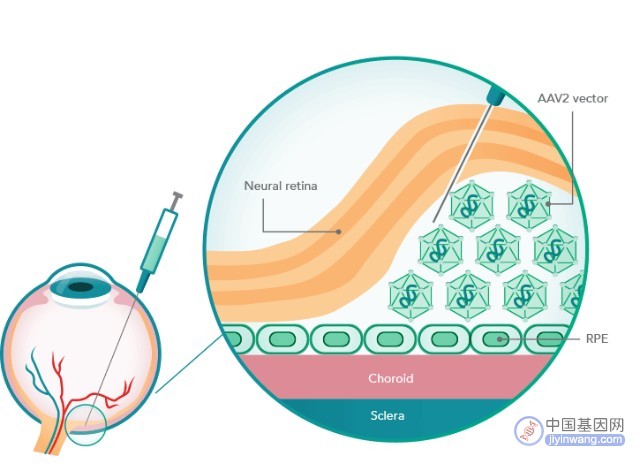
2018年1月,首位患者接受了SRP-9001的治疗,随即还有两位小男孩也加入了临床试验,他们的年龄分别只有4、5和6岁。随着输液的进行,数千万亿个“好”病毒被送进了孩子们体内,这些病毒都装载有能够针对性地产生肌营养不良蛋白中有效成分的基因拷贝。
经过一段时间的随访,研究人员对小男孩们进行了肌肉活检,并把结果与基线时活检的结果进行了对比。结果显示,这些孩子们肌肉中产生的微肌营养不良蛋白(microdystrophin)的平均水平已经恢复到了健康人水平的38%。这个结果大大超出了比研究人员们预期,它比之前预估的结果要好将近4倍!
此外,还有更直观的一个例子能用来说明这种疗法的效果有多好。当研究人员向Sarepta的高管展示这些小患者肌肉细胞的免疫荧光图像时,这名高管甚至要求研究人员再次核实该图片不是来自于健康受试者的参考图像。除了效果显著,SRP-9001的安全性也在可控范围内,没有一名男孩出现过严重的副作用。
SRP-9001的首个小规模临床试验大获成功,Sarepta公司还为投资者和媒体举办了一场公开活动来宣布这个好消息。在门德尔教授分享完该基因疗法的数据后,三名小患者上台与门德尔教授紧紧抱在了一起。这一幕令现场一大半的观众都潸然落泪,这些孩子未来的命运很可能会就此发生极大地转变。
几个月后,这些孩子被再次召回医院接受行动能力方面的测试,所有的孩子在肌肉功能、力量、行走能力和灵活性方面与治疗前相比都表现出来一致的改善——这也是DMD患者最想要看到的结果。研究人员认为,这些改善正是基因疗法使患者的微肌营养不良蛋白大幅度增加导致的。
在这些数据的激励下,Sarepta决定全面投入SRP-9001的临床开发,不仅扩大了工程病毒的生产规模,还迅速启动了首个SRP-9001的安慰剂对照研究。2019年年底,罗氏与Sarepta达成了28.5亿美元的 ,共同开发这一基因疗法。如果顺利的话,Sarepta预计能在2021年获得该临床试验的积极结果,然后向FDA递交上市申请。多少患有DMD的孩子正在逐渐枯萎、凋零,而他们的家人和临床医生却只能眼睁睁地看着。不能让他们再等下去了!
然而,就在所有人都认为这个临床试验毫无疑问会成功时,噩耗传来了——SRP-9001的首个安慰剂对照的随机试验失败了。研究人员报告称,尽管接受基因治疗患者的肌肉细胞中产生了大量的微肌营养不良蛋白,但与接受安慰剂治疗的患者相比,这些增加的微肌营养不良蛋白似乎没能转化为肌肉功能的改善。从数字上来看,SRP-9001治疗组患者的表现要优于安慰剂组患者,但也仅高一点,未能达到统计学上的显著差异。

▲Doug Ingram先生(图片来源:Sarepta公司官网)
英格拉姆先生在回忆起得知试验失败的那一天时,他说:“生命力从我身上流走了。很难描述那一刻的感觉,我就像脸上被揍了一拳一样。”他无法不去想,如果这项试验失败了,那些翘首以盼的DMD患者和家人们该怎么办?
2021年1月7日,Sarepta公开宣布SRP-9001的临床试验失败了,随之而来的是更严峻的危机——许多人开始怀疑,SRP-9001使患者产生的微肌营养不良蛋白是否真的能与完整版的微肌营养不良蛋白一样发挥作用。这是针对DMD开发基因疗法的历史遗留问题,不论是Sarepta公司内部还是外界,都迫切地想要知道确切的答案。
想要知道SRP-9001为何使用的是如今看到的微肌营养不良蛋白的版本,还得从1980年代说起。
那时候,生物技术上的一系列突破使基因疗法成为了可能,尤其是对于DMD这种因基因突变引起的遗传病来说,通过向患者体内递送功能版本的基因拷贝从而产生能够修复由于基因缺陷而功能不全蛋白的基因疗法,似乎是最具“救世主”潜力的疗法。
而事实上,开发DMD的基因疗法并没有想象中的那么简单。原因有二,一个是研究人员用来递送基因的病毒更倾向于首先感染肝脏和肺,很少能够进入DMD的目标组织——肌肉,第二是80年代后期,研究人员在研究编码肌营养不良蛋白的基因时发现,该基因巨大无比,病毒载体根本装不下它。因此,针对DMD的基因疗法开发一度陷入了困境。
直到1990年,一名肌营养不良蛋白基因缺失了一半、还腿脚方便地活到了61岁男子的病例报道为科学家们打开了思路。他的存在表明,即使肌营养不良蛋白基因不全也可能产生不影响功能的蛋白版本,这为科学家们开发精简版本的肌营养不良蛋白基因提供了依据。

随后,横在DMD基因疗法开发道路上的难题被一一清除。1996年,北卡罗来纳大学的基因治疗研究员裘德·萨穆尔斯基(Jude Samulski)博士设计出了能够感染肌肉细胞的腺相关病毒(AAV)。一些科学家也相继开发出了肌营养不良蛋白的精简版本。2006年,萨穆尔斯基博士与门德尔教授合作为一种新型基因疗法进行了试验。他们在6名肌肉萎缩症的患者的肱二头肌上注射了基因疗法,证实了萨穆尔斯基博士的AAV病毒能够安全地将微肌营养不良蛋白基因递送到人类的肌肉细胞中。
这次试验的成功使门德尔教授受到了极大的鼓舞,他知道下一步的计划应该是开发一种能够全身给药的基因疗法。门德尔教授并非基因工程和病毒方面的专家,在他的实验室新增一名大将路易斯·罗迪诺·克拉帕克(Louise Rodino-Klapac)博士后,此前有过基础研究经验的罗迪诺·克拉帕克博士开始全权负责设计新的能够用于全身给药的基因疗法。经过无数个辛苦付出的日日夜夜,终于在2016年,门德尔教授和罗迪诺·克拉帕克博士共同确认了这款基因疗法的最终版本,SRP-9001诞生了。

▲Louise Rodino-Klapac博士(图片来源:Sarepta公司官网)
对于微肌营养不良蛋白到底能不能起效,门德尔教授和罗迪诺·克拉帕克博士最有发言权,他们都亲眼见证过这种迷你版本的营养不良蛋白在患者身上产生的神奇作用。同样参与过精简肌营养不良蛋白的专家华盛顿大学的杰弗里·钱伯伦(Jeffrey Chamberlain)教授也表示,根据合理设计的基因产生的蛋白质实际上可能比在相对健康的DMD患者身上发现的一些微型基因具有更好的作用。
而首个随机对照研究失败的原因在罗迪诺·克拉帕克博士经过更深入的调查后被揭开——不知为何,许多程度更轻或进展更慢的DMD患者被分配到了安慰剂对照组中,这种不平衡的分组方法造成了最终基因治疗组与对照组之间的差异不够显著的问题。
但药物开发的过程中没有后悔药可吃,Sarepta无法在试验结束后要求重新分组,然后再分析出一个有利的结果宣布实验成功。Sarepta随即整理出了两个应对的办法:第一项随机对照安慰剂研究的数据继续收集,同时继续推进第二次规模更大的随机安慰剂对照研究的开展。
2022年春末夏初,Sarepta公司完成了这项工作。在总共包括49名患者的两个不同的数据集中,患者肌肉中产生的微肌营养不良蛋白分别到达正常水平的39%和54%,这个结果在某些方面甚至比之前的试验还要好。
此外,Sarepta还收集了所有研究中受试者的肌肉功能数据。由于缺乏可用作对比的对照组数据,Sarepta将患者的肌肉功能数据与一个单独的数据集进行了比较,该数据集由患病程度相似但未经治疗的DMD患者组成。在一年的时间里,这个“外部对照”组的男孩在同样的标准化测试中得分降低了0.1分,而接受基因疗法治疗的男孩在标准化的肌肉力量、表现和敏捷性测试中得分高了2.3分。

不过,随着接受基因治疗的患者人数增加和随访时间的延长,SRP-9001可能存在的安全性问题逐渐显现。7名受试者发生了与治疗相关的严重副作用,其中一名男孩出现了需要住院治疗的心脏病,另一名男孩则发生了肝损伤。该疗法常见的副作用是恶心和呕吐。
根据这些掌握的数据,Sarepta向FDA递交了加速批准SRP-9001的申请。尽管Sarepta内部的一些工作人员认为保险起见,应该等第二项大型随机对照研究的结果明确后再提起上市申请,英格拉姆先生依然坚持应推动SRP-9001尽快上市。他说:“我们面对的是一种每天都会导致患者死亡的退行性疾病,等待没有意义。我们有一个很好的替代终点(微肌营养不良蛋白水平),可以合理地预测患者的临床益处,并且有很好的数据表明它应该是可预测的。”
对于剩余的不确定性,英格拉姆先生表示当然有可能存在,但这就是FDA设置加速批准的意义,也是为什么生物医药公司要进行确认性临床试验的原因。目前,DMD患者组织和Sarepta的高管正夜以继日地准备在5月12日的全天听证会上提交更多额外的视频案例,以争取该疗法能够顺利获批。
虽有疑虑,但更多人充满期待
不仅仅是Sarepta内部,FDA内部、一些临床医生和患者家属都表示应该等新的临床试验结果出来再考虑是否批准该疗法。因为以目前的技术,患者只有一次接受基因治疗的机会,这将增加在最终结果出来之前就把药物推向市场的风险。此外,与所有其他基因疗法一样,这种益处能够持续多久、随着时间的延长是否会产生更多的副作用仍然是一个悬而未决的问题。
但也有很多人对SRP-9001的加速批准持支持态度。原因很简单,被损坏的肌肉无法再挽回,逝去的生命也不可能再回来。尽管这种基因疗法无法重建肌肉,但如果像艾默生这样的男孩如果能够尽早被治疗,他很可能会拥有一个与其他孩子一样完全正常的童年。而那些已经受到不可逆影响的孩子则有望阻止DMD进一步地危害他们的健康,肌肉将不再消瘦,他们也有可能以更健康的状态度过更长的一段时光。

艾默生的父亲表示,他不确定是否会在5月12日的听证会上为Sarepta作证,但如果有人询问他的意见,他很确定他会说什么。他知道艾默生的未来充满变数,没人知道他的儿子能从这款基因疗法中获益多少或者能获益多久,但他不在乎。他说:“我所理解的治愈和你认为的治愈是不一样的。如果这种疗法能让我的儿子多活一天,那就是一种治愈。这就是我所看到的。”
参考资料:
[1] A bellwether moment: Once a distant dream, gene therapy for Duchenne nears historic decision. Retrieved April 25, 2023, from https://www.statnews.com/2023/04/17/sarepta-gene-therapy-duchenne-muscular-dystrophy-fda-decision/
[2] England SB, Nicholson LV, Johnson MA, et al. Very mild muscular dystrophy associated with the deletion of 46% of dystrophin. Nature. 1990;343(6254):180-182. doi:10.1038/343180a0
[3] FDA staff leaned toward rejecting Sarepta gene therapy before top official intervened. Retrieved April 25, 2023, from https://www.statnews.com/2023/04/13/fda-staff-leaned-toward-rejecting-sarepta-gene-therapy-before-top-official-intervened/
[4] Sarepta Therapeutics Announces That U.S. FDA has Accepted for Filing and Granted Priority Review for the Biologics License Application for SRP-9001, Sarepta’s Gene Therapy for the Treatment of Ambulant Individuals with Duchenne Muscular Dystrophy. Retrieved April 25, 2023, from https://investorrelations.sarepta.com/news-releases/news-release-details/sarepta-therapeutics-announces-us-fda-has-accepted-filing-and?_ga=2.58073770.1044422834.1669665150-341127421.1669665150
[5] Sarepta Therapeutics Submits Biologics License Application for SRP-9001 for the Treatment of Ambulant Patients with Duchenne Muscular Dystrophy,Retrieved April 25, 2023, from https://investorrelations.sarepta.com/news-releases/news-release-details/sarepta-therapeutics-submits-biologics-license-application-srp?_ga=2.241143424.282841863.1664505466-1503290699.1664505466
[6] Roche enters licensing agreement with Sarepta Therapeutics to improve the lives of patients living with Duchenne muscular dystrophy. Retrieved April 25, 2023, from http://www.globenewswire.com/news-release/2019/12/23/1963846/0/en/Roche-enters-licensing-agreement-with-Sarepta-Therapeutics-to-improve-the-lives-of-patients-living-with-Duchenne-muscular-dystrophy.html
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。