人类基因组古病毒如何影响衰老?中国科学家研究提出干预策略

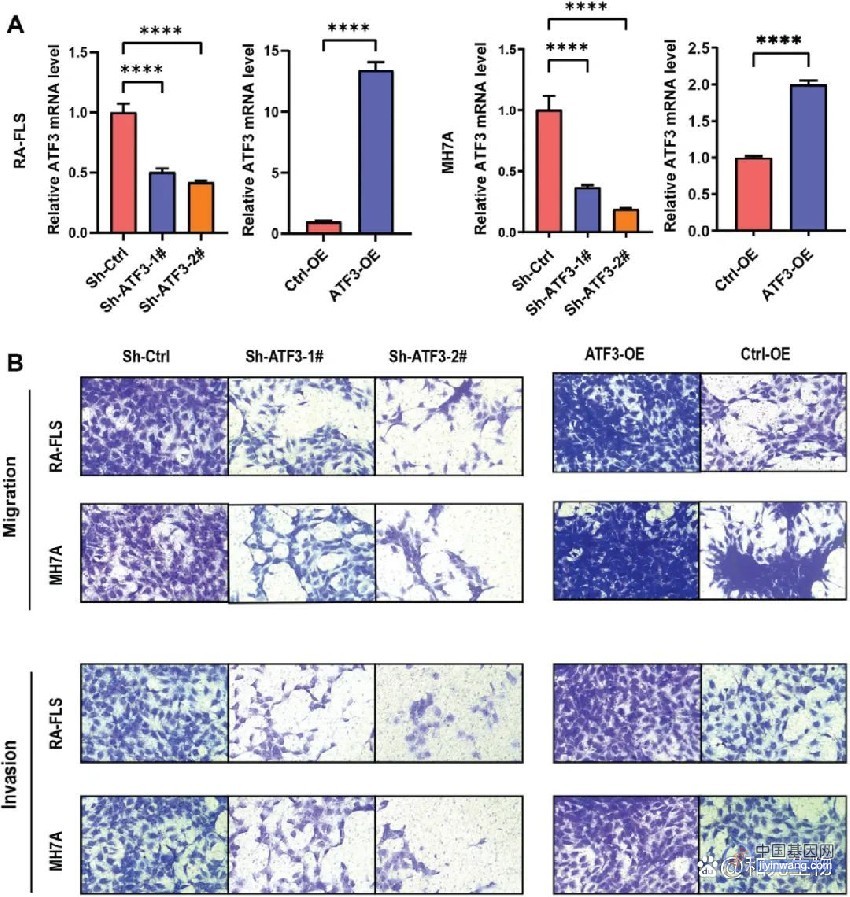
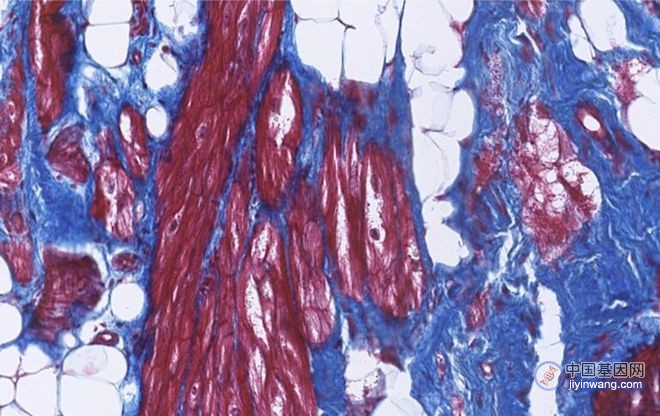
HERVK 病毒RNA (左) 和病毒颗粒(RVLP,右) 在衰老人类细胞中聚集。
中新网北京1月7日电 (记者 孙自法)人类数百万年演化过程中整合进入基因组中潜藏的古病毒,对人类健康特别是衰老有何影响?如何阻断它们复活及扩散?这些关键科学问题一直以来亟待解决,也吸引科学家长期持续聚焦研究。
中国科学家团队对数百万年前远古逆转录病毒入侵整合到人类基因组的遗迹——被誉为“古病毒化石”的内源性逆转录病毒(ERV)最新完成一项合作研究,首次发现年轻的ERV亚家族在细胞衰老过程中被再度唤醒,他们提出古病毒复活介导衰老程序化及传染性的理论,并且创新性发展出阻断ERV古病毒复活及扩散以实现延缓衰老的多维干预策略。
这项人类基因组古病毒与衰老关系研究的重要成果论文,由中国科学院动物研究所刘光慧课题组、曲静课题组和中科院北京基因组研究所张维绮课题组联合中科院遗传与发育生物学研究所、北京干细胞与再生医学研究院、首都医科大学宣武医院、昆明理工大学、华中农业大学、北京大学、北京医院等共同完成,北京时间1月6日夜间在国际著名学术期刊《细胞》(Cell)在线发表。
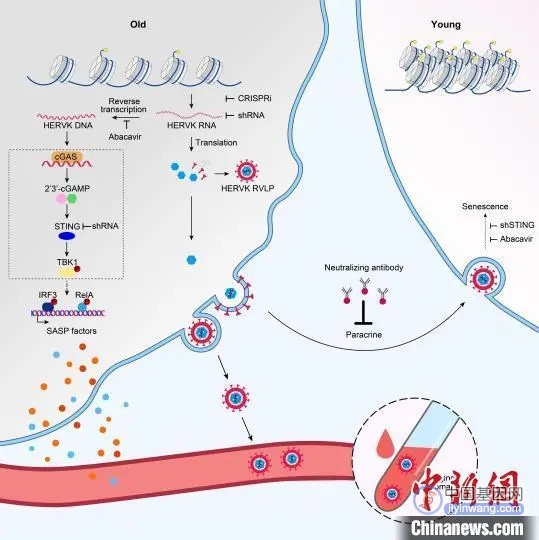
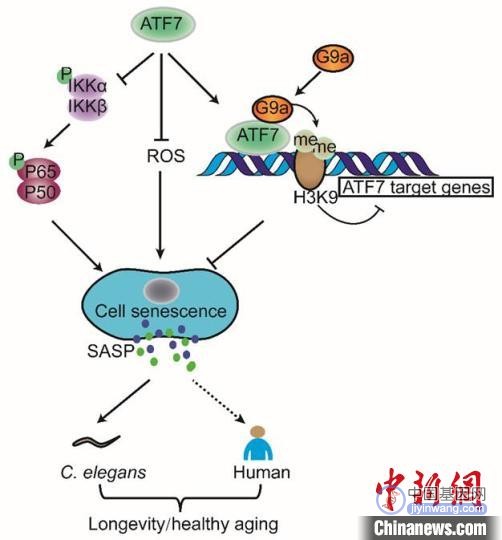
内源性古病毒复活驱动衰老的机制与干预策略。 中科院动物所 供图
探究古病毒元件是否参与衰老程序调控
合作团队介绍说,病毒与人类之间的协同进化关系源远流长,它们之间的交锋从未随停止过,在这场旷日持久的“战争”中,一方面,病毒使人类饱受疾病困扰,甚至死亡,并在此过程中对人类基因组不断利用与改造;另一方面,人类的免疫系统积极对抗病毒的入侵,使得整合到人类基因组中的病毒序列逐渐被宿主细胞的遗传调控系统接管,协同进化。
在百万年的漫长岁月里,大量ERV的遗传信息被人类细胞俘获,并经过突变、缺失等变异成为人类基因组中的“暗物质”潜伏下来,占据人类基因组序列的8%左右,并成为重要的基因记忆。人类与ERV之间的较量可谓“魔高一尺道高一丈”,然而,在生命的孕育及演化中又貌似呈现出和谐共生的景象。
合作团队指出,衰老是人类慢性疾病的最大危险因素,其中,细胞衰老是机体衰老及各种衰老相关疾病发生发展的重要诱因,表观遗传的程序化改变被认为是决定细胞衰老进程的关键因素。人类基因组潜藏着诸多“老化”信号,这些衰老信息流通常受到表观遗传的严密调控而处于沉默状态,但在增龄过程中,由于表观遗传的失序,这些“老化”信号逃离管控,进而激活启动细胞内的一系列衰老程序。
不过,占据人类基因组序列较大比例、如“死火山”般沉寂的ERV古病毒元件是否参与衰老的程序化调控尚且未知。沉睡在人类基因组中的ERV元件能否在衰老过程中逃脱宿主的监视而被再度唤醒?这些“死火山”的苏醒与爆发对细胞和组织的衰老有何影响?ERV古病毒的复活能否作为度量人类生物学年龄的标志物以及干预衰老的分子靶标?这一系列关键科学问题亟待解决,引发广泛关注。
内源性古病毒复活驱动开启衰老“潘多拉魔盒”。
开发出有效抑制古病毒复活等干预策略
在本次研究中,合作团队利用建立的不同衰老研究体系,包括儿童早衰综合征、成年早衰综合征、复制性衰老、生理性衰老的人间充质干细胞模型,人成纤维细胞衰老模型,以及小鼠、猴和人的生理性及病理性多器官衰老模型,结合高通量链特异性转录本测序、全基因组DNA(脱氧核糖核酸)甲基化测序、高分辨率单分子RNA(核糖核酸)原位杂交、免疫电镜和高灵敏的液滴数字PCR(聚合酶链式反应)等多学科交叉技术,发现衰老细胞中表观遗传去抑制(如异染色质减少)导致基因组中ERV的转录激活并翻译出病毒蛋白,进而包装成为病毒颗粒。
研究发现,一方面,衰老细胞中ERV的反转录产物通过激活cGAS-STING(一种蛋白)天然免疫通路诱发细胞衰老和炎症;另一方面,衰老细胞释放的ERV病毒颗粒可通过旁分泌或体液介导的方式在器官、组织、细胞间有效传递并放大衰老信号,最终使得年轻细胞因受“感染”而老化。深入的机制研究表明,ERV反转录产物在宿主细胞胞浆中的出现,会激活初始细胞及被感染细胞中固有的病毒防御机制。这种本能的细胞抗病毒反应意在降低病毒的损害,然而事与愿违,这些防御性机制却恰恰促进了细胞的早衰。
基于此,研究团队详细阐释了衰老细胞基因组中ERV古病毒程序性复活、触发细胞老化、借助病毒颗粒传递衰老信号、感染年轻细胞的全链条机制,又进一步通过对ERV古病毒潜伏、复活、细胞间传递等不同生命周期环节的解析,他们开发出有效抑制ERV古病毒复活及清除病毒颗粒的干预策略,即通过发展基于靶向ERV调控元件的CRISPR(基因编辑技术)基因沉默体系、靶向逆转录酶的小分子抑制药物、靶向病毒包膜蛋白的中和抗体等技术,阻断ERV的转录、反转录、病毒级联感染等多个环节,进而实现组织和机体衰老的延缓。
为衰老评估预警疾病防治提供线索思路
合作团队表示,他们最新完成的这项研究,系统定义并揭示衰老诱导的内源性逆转录病毒复活(AIR-ERV)可作为细胞、器官乃至机体衰老的驱动力及度量标志物,为衰老的程序化、级联放大和可干预性提供全新理论依据,为人类衰老的科学评估和预警、衰老及衰老相关疾病的防治提供重要的线索和思路。
在理论方面,该研究创造性提出衰老的程序化、跨细胞传递及可干预性,将ERV古病毒的复活定义为新的衰老时钟和驱动因素;在技术方面,此次研究综合运用多维表观基因组、转录靶向操控、单分子成像、病毒学、免疫学、化学生物学和分子病理学等前沿交叉技术,动态捕获ERV古病毒的复活、包装、颗粒化、跨细胞传递和激活天然免疫通路等多个生物学过程,成功刻画出ERV在衰老机体中的生命周期轨迹,开创出新的衰老研究范式;在转化医学方面,该研究以ERV古病毒复活链条的不同环节为靶标发展出多样化的衰老干预技术,为衰老相关疾病的防治提供了新的策略,对衰老转化医学领域具有潜在的应用价值。
因此,本次研究揭示病毒密码在远古时代便已融入人类的衰老及寿命调控程序,解码基因组中的古病毒元素将有助于深刻理解人类衰老的机制、健康长寿的规律以及多种老年疾病的诱因。ERV古病毒的复活或许为认识衰老的“潘多拉魔盒”提供一条崭新的路径,对魔盒的解读可为理解衰老规律开辟新的科学疆域,更为防治老年疾病带来全新希望。
合作团队认为,在这次研究基础上,未来围绕伴随衰老的ERV古病毒激活,将会涌现出更多的科学问题:ERV反转录本是否可以重新整合入宿主基因组,进而介导衰老相关的基因组不稳定性?ERV古病毒序列在人类基因组中是否具有遗传多态性?是否与老年健康相关?ERV的复活和感染效率是否具有组织和细胞类型特异性?ERV激活是否会选择性驱动特定衰老相关疾病的发生?体液中ERV检测能否应用于衰老和老年疾病的评估和预警?ERV生命周期的哪些靶向策略对于衰老和疾病干预最为有效?……他们期待随着科学研究不断深入和技术手段日益革新,这些问题将逐一得到解决。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。