Nature子刊:仅删除这个基因就能只吃不胖,助力新型减肥疗法的开发
在当今社会,肥胖已然成为一种世界性的流行病,并极大地增加了包括2型糖尿病、非酒精性脂肪性肝病、心血管疾病的发病率,还会增加癌症发病风险。近期,一项涵盖中国243个城市的1580万名成年人的研究报告显示,中国的超重人群占比34.8%,肥胖人群占比14.1%,形势十分严峻。
饮食、运动等生活因素在肥胖的发生发展中起着重要作用,而其中的关键在于代谢。科学家们注意到,肥胖与代谢异常密切有关,例如线粒体功能障碍。因此,如果能揭示肥胖与代谢的内在联系——某个关键的基因,就能从根源上抑制肥胖,让“天下肥胖人士俱欢颜”。
2024年1月29日,加州大学圣地亚哥分校的研究人员在 Nature Metabolism 上发表了题为:Obesity causes mitochondrial fragmentation and dysfunction in white adipocytes due to RalA activation 的研究论文。
该研究发现,当给小鼠喂食高脂肪食物时,其脂肪细胞内的线粒体会分裂得更小,燃烧脂肪的能力降低。这一过程是由一个名为RalA的基因控制的,而敲除这个基因,即使高脂饮食的小鼠也不会肥胖。这一机制的发现使得人类距离开发出通过增加脂肪燃烧来解决体重增加和相关代谢功能障碍的靶向疗法又近了一步。

高脂饮食会摄入过多热量并转化为脂肪,当身体积累了过多的脂肪时,肥胖及其并发症就会接踵而至。在肥胖的发展过程中,白色脂肪组织(WAT)长期扩张并经历以激素不敏感、炎症、纤维化和凋亡为特征的代谢变化。
值得一提的是,线粒体功能障碍是肥胖、胰岛素抵抗和脂肪肝疾病的一个重要特征,线粒体在健康脂肪组织中发挥重要的代谢作用,但肥胖个体的线粒体功能受到损伤。在这种情况下,脂肪细胞燃烧能量的能力开始丧失,这就是肥胖的人很难减肥的原因之一。然而,究竟是什么导致了线粒体损伤,以及它是如何导致肥胖以及其他并发症,仍然不得而知。
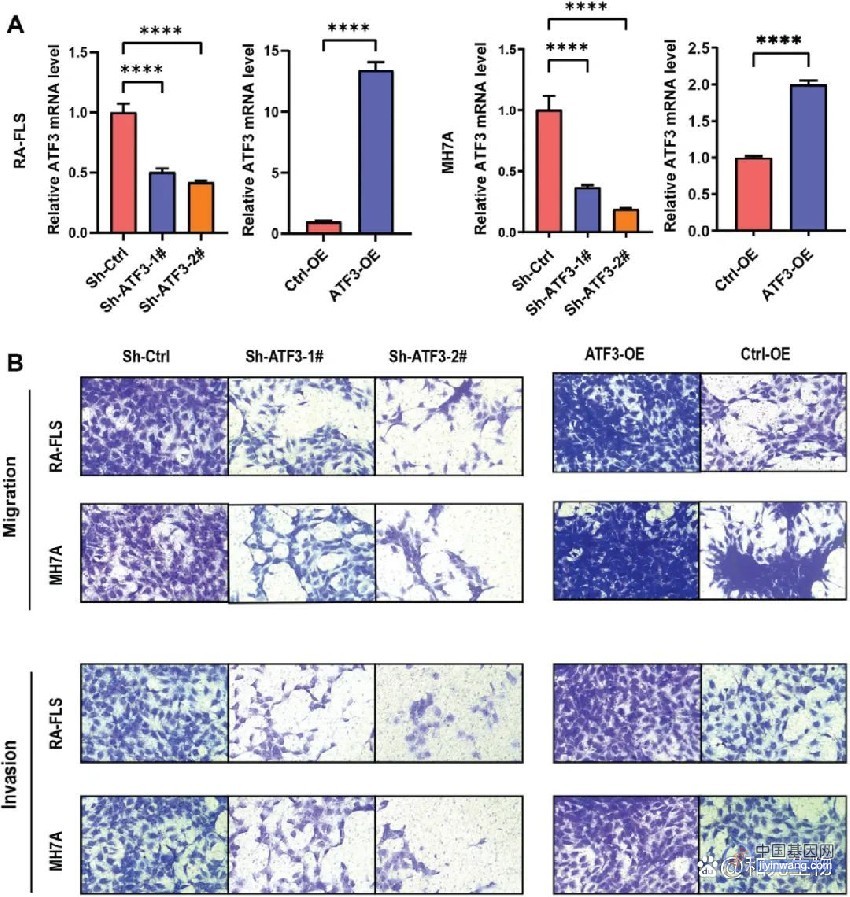
为了回答这个问题,Alan Saltiel教授团队更仔细地研究了肥胖和脂肪细胞中线粒体之间的联系。他们给小鼠喂食高脂肪食物以诱导肥胖,并测量这种饮食模式对白色脂肪细胞线粒体的影响。他们发现,在过多摄入脂肪后,小鼠白色脂肪组织中的线粒体发生了异常分裂——分裂成许多更小的、无效的线粒体,并导致氧化能力降低、脂肪消耗停滞,进一步加剧了肥胖。
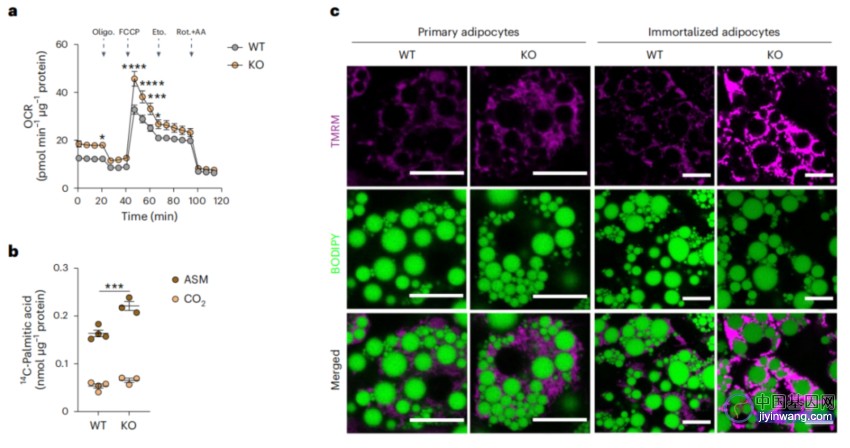
高脂肪饮食诱导小鼠白色脂肪组织中的线粒体的异常分裂
进一步研究发现,这种代谢效应是由一种叫做RalA的分子的活性驱动的。RalA是一种小GTPase,在高脂饮食(HFD)小鼠的白色脂肪细胞中表达量和活性均增加。RalA有许多功能——包括在线粒体发生故障时帮助分解线粒体。当这种分子过度活跃时,它会干扰线粒体的正常功能,引发与肥胖相关的代谢问题。
因此,RalA的慢性激活在抑制白色脂肪组织的能量消耗中起着关键作用,通过将线粒体动力学平衡转向过度分裂,导致代谢功能障碍和体重过度增加。
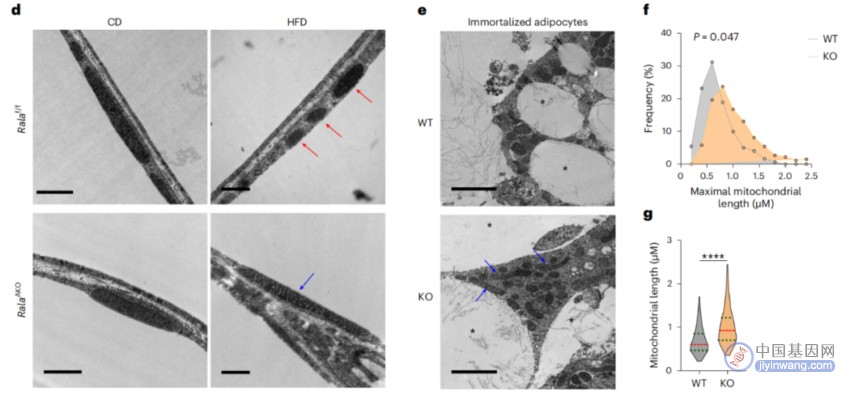
RalA的慢性激活抑制白色脂肪组织的能量消耗
作为印证,研究团队构建了RalA基因敲除小鼠,这些小鼠能免受高脂饮食引起的肥胖。线粒体形态学观察表明,敲除RalA可以逆转高脂饮食的白色脂肪细胞线粒体的裂变增加。有趣的是,小鼠体内受RaIA影响的一些蛋白质也类似于人类中与肥胖和胰岛素抵抗相关的蛋白质,这表明人类也存在类似的机制导致肥胖的发生。
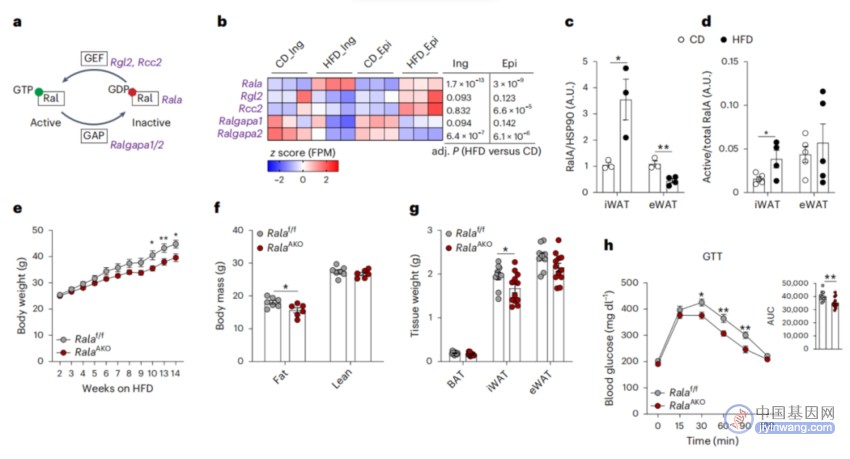
白色脂肪细胞特异性RalA缺失可保护小鼠免受高脂饮食诱导的肥胖
总的来说,这项发表于 Nature Metabolism 期刊的研究表明,高脂饮食通过引发线粒体异常分裂来诱导肥胖及其并发症,而RalA的慢性激活在这一过程中发挥着关键作用。这一机制的发现使得人类距离开发出通过增加脂肪燃烧来解决体重增加和相关代谢功能障碍的靶向疗法又近了一步。
论文链接:
https://www.nature.com/articles/s42255-024-00978-0
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。