拓展诺奖级发现,科学家发现这类“抗衰老基因”还有新作用
2016年,发现“细胞自噬”机制的科学家大隅良典摘得了诺贝尔生理学或医学奖。自噬(autophagy),即“把自己吃掉”,是细胞分解自身组成部分以便循环利用的生理过程,在真核生物中普遍存在。借助自噬作用,细胞通过多个步骤回收或处理细胞内的蛋白质、受损的DNA和RNA分子、细胞器等,从而可获得合成新蛋白和构建细胞器的原料。
大隅良典教授与同事们的一系列工作不仅首次在酵母细胞中详细描述了自噬现象,还首次鉴定出了自噬作用需要的关键基因:自噬相关基因ATG1。此后,研究人员陆续找到了30多个ATG基因,和自噬有关的信号通路得以被阐明。
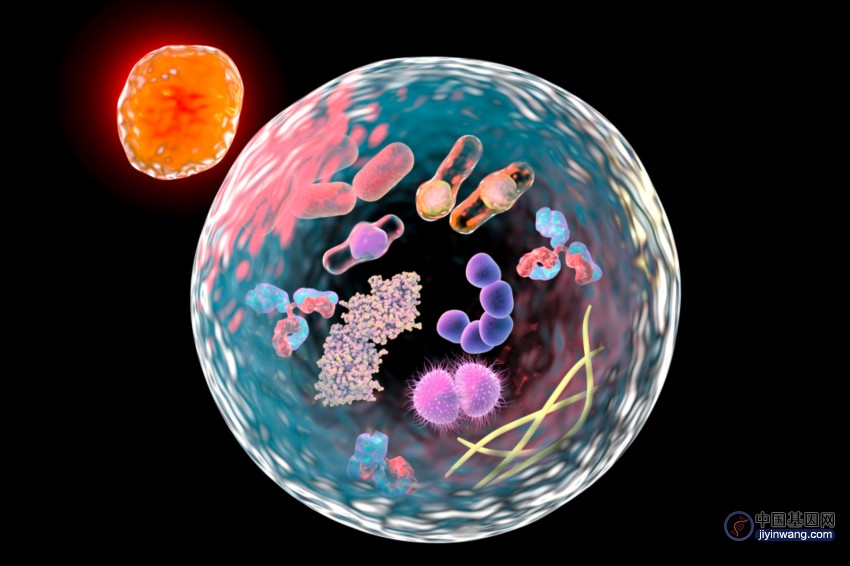
▲自噬是对细胞稳态至关重要的降解途径
近年来,随着对自噬作用的更深入理解,科学家们发现自噬是衰老以及衰老相关疾病——包括肿瘤、心血管疾病、神经退行性疾病等的关键参与者,也逐渐揭示单个ATG基因的功能及其在疾病和生理过程中的作用,多个自噬基因被看作延长生物寿命的潜在靶点。
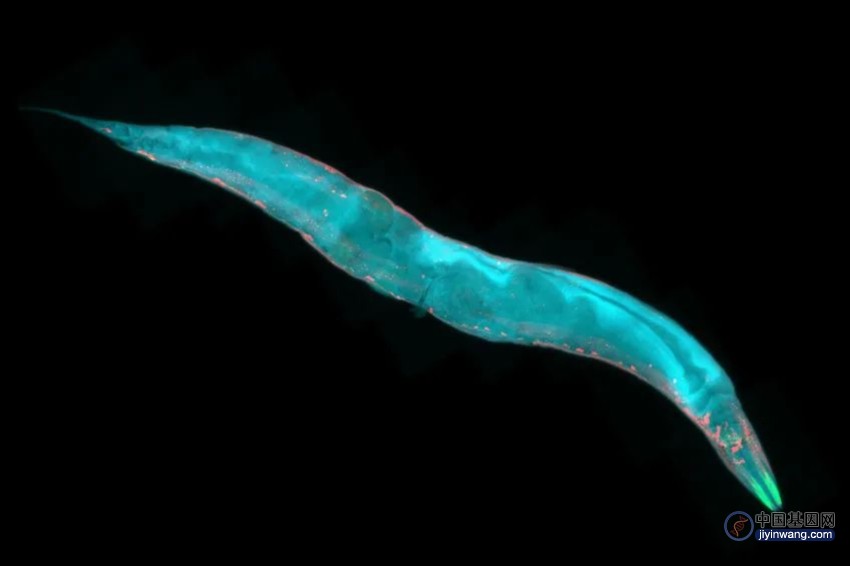
目前任职于巴克老龄化研究所(Buck Institute)的Malene Hansen教授多年来也在研究ATG基因,尤其是在神经元中起作用的ATG,因为这类细胞在神经退行性疾病中首当其冲受损死亡。为此,她和合作者在秀丽隐杆线虫(Caenorhabditis elegans)身上展开实验,这种透明小蠕虫的神经系统一目了然,经常用于研究衰老。
当他们逐一抑制线虫神经元中的ATG基因后,却发现了自噬基因的新功能。近日,研究团队在《自然》子刊Nature Aging发表了他们的结果。

根据已阐明的自噬过程,需要被处理的蛋白质、细胞膜等“待回收垃圾”,会被隔离在有膜的囊泡中,形成自噬体,然后输送到溶酶体那里进行降解。但新研究发现,形成自噬体不是自噬基因起作用的唯一方式。
研究人员发现,在自噬体形成早期阶段起作用的一些Atg蛋白被抑制后,会导致线虫寿命延长。这不免令人好奇:难以形成自噬体的情况下,动物是怎么处理那些待回收垃圾的呢?
亨廷顿病是一种神经退行性疾病,由于过长的多聚谷氨酰胺(polyQ)蛋白会异常聚集在神经元内,形成有害的蛋白质沉积,导致细胞死亡。以此为模型,研究人员进一步探索了在缺少特定ATG基因时,线虫会如何处理应丢弃的蛋白质聚集体。
结果他们发现,在不依赖自噬体形成的情况下,神经元细胞内会形成另一种大囊泡Exophers,它们就像大垃圾袋一样装着PolyQ蛋白聚集体,将其“挤”出细胞。这种“大垃圾袋”是2017年刚被发现的,研究人员推测,在神经元内细胞太多或是正常的回收机制被破坏时,“大垃圾袋”就派上了用场。
由于Exophers的形成让神经元中的致病蛋白质大大减少,线虫不仅神经元更健康,整体寿命也随着延长。
在这个过程中,研究人员还确认了有一个ATG基因,即线虫的atg-16.2对于Exophers的形成是不可或缺的。当这个基因被抑制时,线虫无法形成Exophers、丢弃PolyQ蛋白聚集体,也就无法延长寿命。
研究作者推测,atg-16.2编码的蛋白质在衰老过程中起着过去未被发现的作用。“如果我们发现的机制在其他生物体中是保守的,我们推测它在衰老中发挥的作用可能比以前所理解的更广泛,并可能提供一种延长寿命的方法。”Hansen教授指出。
参考资料:
[1] Yongzhi Yang et al., (2024) Autophagy protein ATG-16.2 and its WD40 domain mediate the beneficial effects of inhibiting early-acting autophagy genes in C. elegans neurons. Nature Aging Doi: https://doi.org/10.1038/s43587-023-00548-1
[2] New roles for autophagy genes in cellular waste management and aging. Retrieved Jan. 5, 2024 from https://www.eurekalert.org/news-releases/1030052
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。