基因治疗先驱公司Sangamo,ZFN基因编辑工具为什么掉队了?
Sangamo Therapeutics,这家1995年成立的基因治疗先驱近来烦心事不少。
近日,Sangamo 宣布了战略调整计划,这也意味着公司要在美国裁员27%。通过业务和结构调整和其他计划采取的降本举措,Sangamo预计每年可节省约3100万美元,为公司提供接下来12个月的运营资金。此外,技术运营执行副总裁 R. Andrew Ramelmeier 博士将于今年7月离开公司。
3月17日,公司公告称Novartis和Biogen分别决定终止了合作协议:与Novartis合作始于2020年7月,基于ZFN共同开发三个临床前CNS管线;与Biogen合作始于2020年2月,基于ZFN和AAV载体共同开发治疗tau蛋白病的ST-501、治疗PD的ST-502、靶向DM1等四种临床前基因疗法。
去年1月,公司公告称Sanofi决定终止合作协议:这项始于2014年1月的合作,基于ZFN共同开发治疗SCD的临床前通用型细胞治疗药物,终止前已进入I/II期临床。
Sangamo的市值已从高点的26亿美元,一路滑落至2.7亿。
Sangamo因其坚持——或者说垄断ZFN技术路线而知名,总裁兼首席执行官和董事会成员Sandy Macrae博士曾获得过诺贝尔医学奖(2013年)提名。广泛的涉及领域、独特的研究平台,还有夺目的合作管线,Sangamo一直是基因治疗领域的旗帜之一,但现在,这面孤独的旗帜好像已经失去了荣耀和色彩。
在Sangamo与ZFN技术风雨飘摇时,另一边,CRISPR技术又传来新的重磅融资:Beam衍生公司Orbital获2.7亿美元A轮融资,Orbital 将 LNP 和 VLP 以及环状 RNA 结合在一起,正在 RNA 技术、递送方法、数据科学和自动化的交叉点构建一个技术平台,涉足下一代疫苗、蛋白质替代品和免疫调节剂,并正与大型制药公司在内的潜在合作伙伴沟通合作。
ZFN与CRISPR作为两代基因编辑工具,其冰火两重天的现状值得玩味。

ZFN独行侠
Sangamo Therapeutics公司总部位于美国加州里士满,于2000年上市。在公司时任CEO Edward Lanphier的努力下,ZFN技术从设计、优化到临床应用的整套技术体系的专利被Sangamo*锁定,再也没有其它机构从事ZFN的研发。
ZFN是一个带定位系统的基因剪刀,锌指蛋白用于识别和结合特定的基因序列,FokI核酸内切酶可以通过二聚体化特异性地切割目的基因,并且可以切割真核基因组的任意识别序列。
ZFN的主要优势在于基因修复方式多样、精准更换基因、对基因表达强度影响较小。与CRISPR相比,ZFN作为基因编辑工具的主要劣势是开发高质量基因编辑产品费时且繁琐。虽然这种明显的差异仍然存在,但Sangamo已经改进了开发过程,周期由三个月缩短至10天,并减少了它的费用。
由于Sangamo的研究和开发工作,ZFN在基因编辑领域取得了多项*:*个编辑人类细胞基因、*个编辑体外基因和*个编辑体内基因。
Sangamo具有先发优势,但从ZFN被发现到现在已近40年,Sangamo成立也近30年,公司还尚未有冲线的产品。反观更晚起步的CRISPR,今年已经撞线在即,Vertex Pharmaceuticals 和 CRISPR Therapeutics 提交了用于镰状细胞病和 β 地中海贫血治疗的 exa-cel 的 BLA 申请,Bluebird bio 提交了基因治疗 lovo-cel 上市申请(BLA),用于 12 岁及以上有血管闭塞事件史的镰状细胞病(SCD)患者治疗。
根据Sangamo的公开信息,其进度最快的管线是与辉瑞公司合作的血友病A项目(此前的SB-525),为肝靶向 AAV 基因疗法,辉瑞正在主导临床III期的研究,以评估在中度或重度 A 型血友病成年男性参与者中的临床疗效和安全性。

▲ Sangamo公司最新管线情况,来源:公司Q1财报
在Sangamo的*季度财报电话会上,公司宣布了接下来的三大战略重点:
Nav1.7和Prion,这是Sangamo神经学表观遗传调控领域的重点临床前项目,Nav1.7用于治疗慢性神经性疼痛,预计将于2024年提交IND,Prion计划在2025年提交IND。
针对法布瑞氏症(此前的ST-920)的III期临床准备,该病是因X染色体上出现缺陷而导致的遗传疾病,它主要是因制造α-半乳糖甘酵素的基因发生缺陷,Sangamo表示其产品在I/II期试验中已展现出良好的安全性,正在推进III期试验的计划。
TX200 CAR-Treg 临床研究,TX200用于实体器官移植,Sangamo计划通过I/II期临床研究推进 TX200在肾移植中的应用,并计划加速剂量递增。
从公司最新的管线列表可以看到,Sangamo的重点项目全部为自有管线,合作项目和此前比可以用寥寥无几来形容。Sangamo在独行侠的路上似乎越走越远。
技术发展,需要开枝散叶
当业内对比ZFN与CRISPR时,无一不提到ZFN面临的一大问题是专利上的封锁。
专利一直是基因治疗领域的关键竞争壁垒,Sangamo干脆从源头避免这个问题,所以ZFN领域只有Sangamo自己摸索前路,这也导致ZFN技术自问世至今没有获得大规模的应用,也没有突破性进展。
CRISPR技术则在“不那么体面”的专利之争中迅速发展。2013年11月,张锋连同Doudna等人共同建立了Editas Medicine,但最终由于专利方面未谈拢,Doudna便选择了单飞并于2014年创立了Intellia Therapeutics。此外,Charpentier也没有闲着,其同样于2013年创立了CRISPR Therapeutics。如今,这三家企业已成为CRISPR基因编辑技术领域的头部企业。
CRISPR在一路的专利纷争中,不断有细分路径出现,如2016年碱基编辑出现,可以做到定点的修饰某一个或者某几个点突变,能够定向改变基因组中某个特定位置的特定碱基,并且只改变单个目标碱基,而不会影响到其他碱基;2019年刘如谦博士公开的引导编辑可以实现4种碱基之间的任意变换及小片段的精准插入和删除。
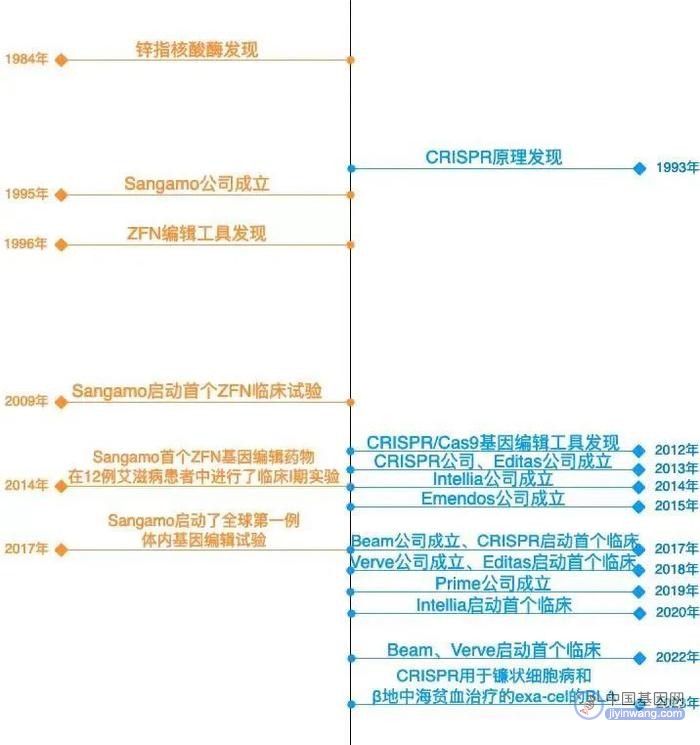
▲ ZFN与CRISPR技术相关公司时间线/ 动脉新医药整理
针对专利问题,布局CRISPR技术的众多公司一方面想办法绕开CRISPR-Cas9,另一方面,在想办法争夺尚未尘埃落定的专利。辉大基因自主开发的CRISPR-Cas13系统——Cas13X(也称为Cas13e)和Cas13Y(也称为Cas13f),既可以降低RNA的靶基因表达,还可以通过改造与脱氨酶结合进而实现RNA单碱基编辑,且编辑效率接近80%;吐露港生物(ToloBio)在美国申请Cas12蛋白诊断专利,公司利用Cas12a的反式切割活性开发了HOLMES诊断系统,在专利上与Mammoth Biosciences展开了艰难的竞争并击败对手。
这一切,让CRISPR领域更显百花齐放的状态。
反观Sangamo,公司之外的科学家们仍无法了解其筛选和优化ZFN技术的详细过程,在此之上的进一步完善和进步当然无从谈起。要让技术飞速成长、开花结果,Sangamo公司内部的少数科学家远远不足以实现这一目标。就算学术界的科学家想要利用Sangamo公司的技术进行基础研究,比如对某个生物的基因进行定点突变并研究其生理功能,也只能委托Sangamo公司设计和完成,堪称是黑箱操作。ZFN原本基础研究和临床应用方面都表现出色,却被限制在Sangamo公司内部,无法释放其潜力,丧失了原本的先发优势。
从某种意义上说,Sangamo公司对专利的*保护,作为商业实践可能还是会写进许多商学院和法学院的案例教材,被人长久讨论,但ZFN技术和其相关的研究是否能被铭记,要被打一个问号。毕竟不论在科学上的争执还是商业上的竞赛,最终是为了释放造福人类的潜力。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。