初创Biotech方拓生物,搅动AAV基因疗法“江湖”
自2021年开始,在资本寒冬和“新冠”交织影响下,许多Biotech不得不放慢步调,消减管线,卖掉工厂,裁减团队。但这家初创的生物技术公司先是果断投入1亿多元人民币建好占地4000平方米GMP厂房(从开建到启用仅花费不到半年),而后又一举拿下了1.6亿美元B轮融资。
2023年,当不少Biotech都节省开支放慢脚步的时候,这家Biotech公司像是突然按下了加速键。
4月,FT-003 IND获批;7月,FT-004 IND获批;8月,FT003又一适应症临床批件落定;11月,潜在First-in-class药物FT-002 IND获批;12月,FT-001启动II期……
这一年,公司原总裁、CMO李新燕升任CEO挑起了大梁。这家Biotech就是成立于2019年的方拓生物。

方拓生物CEO 李新燕
方拓生物如何能在逆流中走出惊人的效率曲线?它的“野蛮”生长又将在何时迎来集中爆发?
01
眼科破局,孵化AAV基因疗法
2017年底,FDA批准了首个眼部疾病基因疗法Luxturna上市,在业内掀起新的研究热潮。罗氏、诺华等MNC,过去几年均有披露数十亿美元的大额眼科AAV基因疗法合作。
MNC为何对眼科AAV基因疗法如此热衷?李新燕介绍,目前,大约有2%与基因治疗相关的临床试验聚焦于眼科疾病。眼睛作为AAV基因治疗药物的靶器官,有其独特的优势,如眼睛是相对免疫豁免器官,针对AAV的免疫反应相对较弱,有利于AAV的转染和转录;局部给药,安全性高;有效性和安全性评价方法直接,结果易于评价;药量需求小,对AAV的生产规模要求不高,等等。
李新燕对写意君说,跨入这片价值洼地是方拓生物的战略布局。目前公司第一梯队管线(FT-001、FT-002、FT-003)均针对眼科疾病开发。
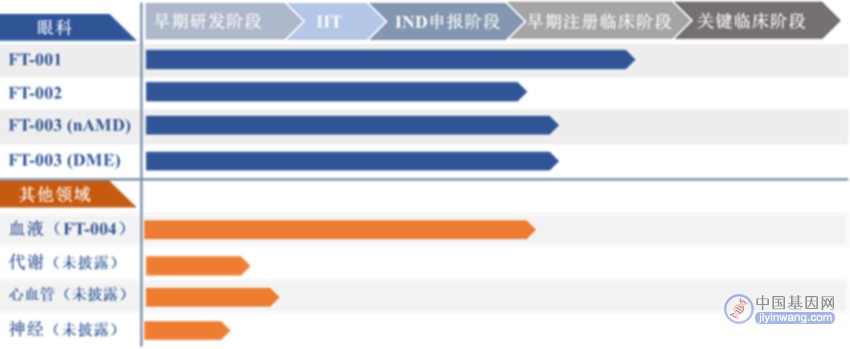
方拓生物管线进展(图源:公司官网)
以FT-001为例,这是一款针对RPE65基因变异导致的遗传性视网膜病的AAV基因疗法,该疾病表现为幼年发病,视力逐步丧失甚至失明。方拓生物FT-001项目从启动到获得FDA临床试验许可,仅用了不到两年时间,并于2022年9月获CDE临床试验批准。
临床I期结果显示,患者接受FT-001治疗后,从第4周开始患者视功能各项检测指标明显持续改善。李新燕透露,目前该项目已启动II期临床,并完成了病人入组。
针对wAMD患者,方拓生物推出了FT-003,采用玻璃体给药方式,预期患者一次注射,长期有效。
近年来,湿性年龄相关性黄斑病变(wAMD)日渐受到关注。2016年以来,我国wAMD患者人数维持在3亿人以上,有报道预计到2030年增至4.9亿人。尽管抗VEGF药物治疗将眼底血管性疾病的治疗上升到了新的阶段,但仅能让约一半的患者得到持续有效的水肿积液消退。
李新燕称,FT-003的IIT结果显示,接受了低剂量治疗的三例患者中有两例患者展现出持续的视力改善、视网膜水肿明显消退, 12个月内没有再接受过抗VEGF治疗,并且安全性和耐受性良好。
一个新的里程碑是,2023年8月,FT-003的又一适应症糖尿病黄斑水肿(DME)获批临床。据悉,每3个糖尿病患者就有1个糖尿病视网膜病变,每3个糖尿病视网膜病变患者中就有1个是DME,市场规模极其可观。
此外,针对治疗X连锁视网膜色素变性(XLRP)这一尚未有药物获批的空白市场,方拓生物推出了AAV基因疗法FT-002。已经完成的IIT研究研究显示,18例患者,未发生明显的不良反应,且视敏度等视功能指标明显改善。
2023年12月,XLRP临床进展较快的Bota-vec,不久前被强生以4.15亿美元购买权益。而FT-002是中国在XLRP治疗领域首个获得临床试验许可及开展人体试验的基因治疗药物,是该适应症领域绝对的潜力竞争者。
除了眼科,AAV基因疗法也有望在更多的疾病领域发挥优势。方拓生物开发的FT-004也已进入临床阶段,适应症为血友病B(内源性FIX活性≤2%)。
国际上首款获批的血友病B基因疗法为uniQure与CSL Behring的etranacogene dezaparvovec,公布的定价为350万美元,而以方拓生物为代表的中国企业自研疗法有望大幅降低成本和售价。
非临床数据显示,FT-004注射模型动物后,可高效转染肝细胞,使其持续、稳定地表达和分泌具有活性的hFIX(人凝血因子9)蛋白,提高模型动物的凝血功能,并表现出了良好的安全性。针对血友病患者,FT-004有望实现一次注射,长期获益。
02
创新效率的背后
目前,方拓生物在中美各有一支团队,共计100余人。美国的研发中心负责早期研发、载体构建、工艺开发、质量检定方法的建立。中国团队负责中试放大、GMP生产、临床试验以及注册。
作为方拓生物在中国的“1号员工”,也是这家Biotech发展“高速路”的“核心工程师”,李新燕告诉写意君,方拓生物高效创新的背后是这四个要素:资金、生产基地、科学沟通和执行力。
第一位的是资金。资本寒冬时期,方拓生物如何融到1.6亿美元?
事实上,这笔钱早在2021年就已“预订”好的。协定之后,方拓生物与B轮投资人(领投方博裕资本,红杉中国,正心谷、史带投资等参与跟投,原股东奥博资本、泓元资本继续加持)将融资额拆成两笔,2021年4月到位的第一笔资金用以推进项目,如满足四项里程碑,方拓生物即可再拿到另一笔资金。
2022年7月,方拓生物的四项里程碑均如期或提前实现,于是顺利拿到B轮全部融资额1.6亿美元。
李新燕说,这笔融资“有幸运的成分”,但这种方法为Biotech应对市场波动、未雨绸缪提供了一种可行方案。
第二,生产基地。很长一段时间以来,自建与委外之争,涉及成本、模式等诸多面向,一直萦绕在本土Biotech的发展之路上。
方拓生物是自建派。李新燕表示,生产基地是把握AAV产品推进速度的“命脉”,全球仅有30%的企业能做全产业链,正说明这是竞争优势所在。在条件支持的情况下,一定要做。
对于方拓生物,不存在“建不建”的选择,问题是多久能建成完工。这家Biotech投入了超过1亿元人民币,仅用时半年,就完成了技术转移、工艺确定。李新燕透露,团队“6月拿到(厂房)钥匙,12月就验收通过了”。
在生产基地验收后,效率变得更可控。毕竟,“资源握在自己手里,就是想三个月拿到一项结果,也是可以做到的”,在李新燕看来,这是委托CDMO未必能实现的。
更远的考量是,打造可放大的技术平台,后续也能在降低生产成本、保证质量稳定上起到关键作用。
最后是沟通。这主要指与FDA和CDE就科学问题的沟通。方拓生物的第一款眼科药物产品FT-001,在2022年7月就先通过了FDA的临床许可,这种速度背后,与监管机构间的保持互动密不可分。
许多Biotech都曾折戟在与监管机构的沟通上,但这是李新燕的“舒适区”,她曾见证了近20年中国创新药市场的崛起和国内外监管环境的变革。
早在2009年,李新燕在完全没有可参照经验的情况下,带领另一家本土Biotech泽生科技团队,完成了一款全球创新治疗慢性心力衰竭药物的中国、澳大利亚的II期临床试验,并在2012年申请获得FDA批准开展美国II期临床研究。
“FDA对科学的深刻理解和灵活包容是值得学习的,CDE也在逐渐往这个方向走。只要科学逻辑是成立的、方法是可行的、结果是可验证的,和监管机构沟通就比较容易。”李新燕认为,最关键的研究结果要客观真实,首先要能说服自己,不要心存侥幸。
03
破与立:第二个“三年规划”
AAV这种新的治疗范式已经走过了“从0到1”的阶段,剩下的是怎样在商业化市场完成“从1到10”的升级。跳进AAV基因疗法“江湖”的方拓生物,前路面临着不少同行都会遇到的挑战,特别是如何降低产品的成本实现患者可支付。
在欧洲,25种已获批的基因疗法中,有7种因商业原因(而非临床原因)被撤出市场,甚至在细胞疗法市场上,一些产品上市已有7年,但市场上仍未出现“重磅炸弹”。
李新燕认为,平衡开发成本与患者支付,需要多方的合力。就方拓生物而言,技术是其着力点。“我们已建立有竞争优势的研发、生产技术平台,针对不同血清型AAV都能实现规模化生产,同时控制空载体率低至1%以下。”李新燕补充说。
当下,方拓生物已经进入第四年。在下一个三年中,公司计划完成C轮融资、继续推进临床试验以及促成与MNC的合作。关于管线,方拓生物定下的目标是,有一款产品完成III期临床试验并提交上市申请,两款产品进入临床III期,苏州GMP工厂拿到生产许可证,并开启一款产品的商业化生产。
李新燕坦言,想要实现这些目标,公司得进一步优化团队架构,比如招募BD、CMO等高管,还需要做好中美团队的配合与交流。在新的CMO到来之前,她仍需要担负起CEO和CMO双重责任,眼下首要就是优化几支势头正盛的先发管线的临床计划。
在新药研发领域浸淫20多年后,李新燕希望带领方拓生物,借助AAV基因疗法的优势,向更多人类疾病发起挑战。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。