全球首个!自闭症基因疗法即将启动人体试验!

自闭症基因疗法即将启动人体试验!
2024年1月31日,美国生物技术公司Jaguar Gene Therapy宣布,美国⻝品和药物管理局 (FDA)已批准该公司的基因疗法产品JAG201的研究性新药 (IND) 申请,Jaguar公司计划于今年下半年在美国启动针对存在 SHANK3 突变或缺失的 ASD 和 PMS 成人患者的I期临床试验。
JAG201基因疗法主要针对SHANK3基因突变或缺失引起的严重神经发育障碍,包括自闭症谱系障碍(ASD)和费伦‑麦克德米德综合症(Phelan-McDermid Syndrome,PMS)等遗传性疾病。
目前,这项基因疗法已在包括中国、美国、日本等多个国家完成专利申请和注册,专利持有人为著名的华人科学家、麻省理工-哈佛大学布罗德研究所高级科学家冯国平博士。JAG201正是基于冯国平等人的专利授权开发的基因疗法产品。
此前,冯国平等中国和美国团队共同完成的针对小鼠和猴子的试验显示,该疗法可以恢复突触功能,从而改善患者的神经行为、认知和运动功能。

JAG201基因疗法的英文专利
01
SHANK3是自闭症患者中突变频率最高的风险基因之一
自闭症是一种复杂的神经发育障碍,目前的研究表明,自闭症是环境与多基因变异的结果,科学家们已经确定了数百个与自闭症相关的基因。
但是,并非每一个基因变异都与自闭症风险有很强的关联,而SHANK3是自闭症患者中突变频率较高的风险基因之一。
冯国平在此前的采访中曾提到,有85% 左右的该基因突变者在临床上被诊断为自闭症。而基因测序研究也表明,大约1% 的 ASD 患者可能存在SHANK3突变。
SHANK3,全称是“SH3和多重锚蛋白重复域3”,也称为富含脯氨酸的突触相关蛋白2 (ProSAP2),是人类中由22号染色体上的 SHANK3基因编码的蛋白质。
该蛋白质含有5个相互作用的结构域,是突触的“多功能支架”蛋白,负责将神经递质受体、离子通道以及其他膜蛋白与肌动蛋白细胞骨架、G蛋白偶联信号传导途径相连。
研究表明,SHANK3 的异常基因剂量与严重的认知缺陷有关,并使具有SHANK3基因变异的人群增加了自闭症的易感性。也就是,具有这一基因变异的人群,会表现出典型的ASD特征,比如社交障碍、重复刻板行为、言语发育障碍等。

2019年,冯国平联合中国科学院深圳先进技术研究院、中山大学和华南农业大学的研究人员发表于Nature上的一项研究表明:具备 SHANK3基因突变的猴子大脑神经元功能连接减少,个体表现出社交回避、刻板行为等自闭症症状,这是一个典型的自闭症模型。
SHANK3 单倍体不⾜也会导致 PMS(也称为 22q13.3 缺失综合征),这是⼀种罕⻅的遗传性疾病,估计患病率为万分之⼀。
PMS患者的常见特征包括新生儿肌张力低下、整体发育迟缓、言语缺失到严重迟缓、自闭症行为和轻微的畸形特征。
由于与自闭症有诸多症状重叠,很多PMS患者也被诊断为自闭症。
02
解决突触功能障碍,能改善神经发育障碍者的生活
JAG201基因疗法是基于前述冯国平等人的专利授权。专利文档显示,该方法应用的策略是“使用AAV系统将Shank3基因的功能性拷贝递送至脑细胞以恢复细胞功能。”
冯国平等人之前的研究显示,SHANK3缺失会导致小鼠、猴子的突触功能障碍和行为异常。
在小鼠模型中,SHANK3基因的变异或缺失,导致了小鼠突触缺陷、社交互动受损、运动困难、重复梳理和焦虑水平增加,而当SHANK3蛋白水平恢复过后,小鼠的突触缺陷和行为异常都得到了改善。
在实际操作中,由于全长的SHANK3蛋白包括多个结构域,对应的基因编码达到5.2Kb,很难通过常见的腺相关病毒(AAV)载体将其递送到目标组织或者细胞。
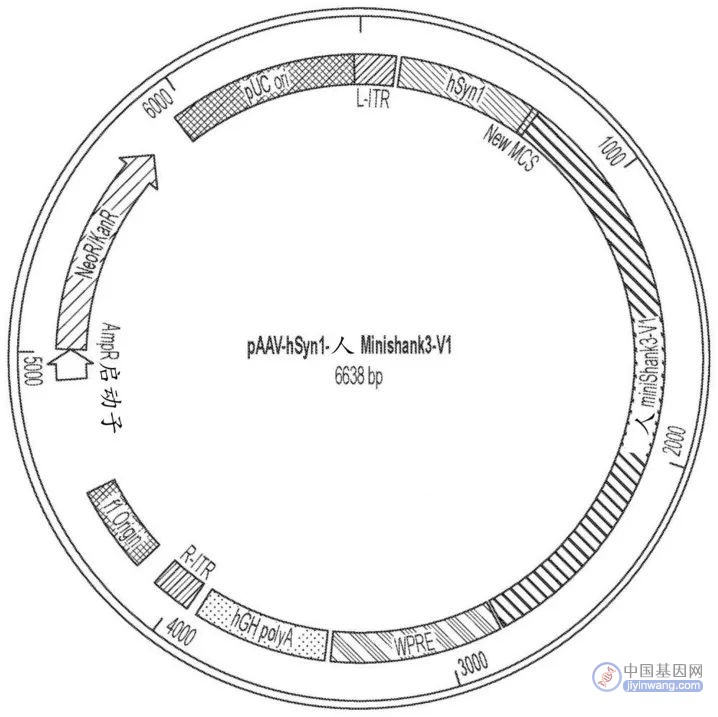
包含人miniShank3基因的AAV载体实例 图源:Shank3基因治疗专利申请
但冯国平等发现可以从全长SHANK3蛋白中去除或截去特定结构域以产生MiniShank3,使其能够被AAV递送,而MiniShank3也能实现恢复兴奋性神经元中的Shank3水平的目标。
本次获得FDA的IND申请,并将进入I期临床的JAG201基因疗法,使用的正是这一套方法。
JAG201通过AAV9载体,将功能性SHANK3小基因(即特定结构的MiniShank3)递送至中枢神经系统的神经元中,给药方式为一次性单侧脑室内(ICV)注射,靶向大脑和脊髓,旨在转导单倍剂量不足的神经元,提供适当的 SHANK3 水平,并持久恢复学习和记忆所需的突触功能,这是适当的神经发育和维持认知、交流、社交和运动技能的基础。
冯国平本人对即将开展的I期临床试验很有信心,在Jaguar公司发布的通稿中,他表示,由于之前在SHANK3功能不足的啮齿动物和非人类灵长类动物模型中,直接获得了非常好的临床前数据,这大大降低了JAG201的临床转化风险。
“现在,我非常高兴可以跟Jaguar公司一起,将JAG201推向临床”,冯国平表示,“我们相信解决突触功能障碍,可以积极改变许多神经发育障碍患者的生活”。

冯国平,桐庐县分水镇人,1982年毕业于浙江医科大学(现浙江大学)。1986年上海第二医科大学取得硕士。1989-1995年纽约州立大学博士。1995-2000年在华盛顿大学从事博士后研究。2000年杜克大学神经生物学系助理教授,2010年麻省理工学院终身教授。2019年美国艺术与科学学院院士。(图源麻省理工学院麦戈文研究所)
03
基因治疗自闭症还有多远?
随着生物技术的进步,基因治疗正逐渐从理论研究进入临床实践。
2023年11月17日,基于CRISPR-Cas9技术的基因编辑疗法Casgevy在英国获批上市,这也是全球首款获批上市的CRISPR基因编辑疗法。
10天后,上海交通大学医学院松江研究院/中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)仇子龙研究员团队开发的单碱基编辑技术,也被研究证实能改善特定的基因突变导致的自闭症症状。(自闭症基因治疗新进展:打一针后,小鼠的社交障碍逐渐消失了)
如今,随着美国FDA批准Jaguar公司的IND申请,自闭症基因疗法也正式进入临床试验阶段。
该公司负责人表示,希望该疗法,能够为有SHANK3基因缺失或者突变的自闭症和费伦‑麦克德米德综合症患者带来改变。“他们因为一系列临床表现,包括全面发育迟缓、言语和交流障碍,以及认知、社交和运动功能障碍,最终需要24小时的护理和监督。而截止目前,没有针对根本原因的治疗方案。”
但该项疗法要到正式上市,还有一定的距离,且针对的也是单基因变异/缺失的特定人群。
复旦大学遗传发育学博士丁爸,同时也是一位阿斯孩子的父亲,他向大米和小米表示,基因治疗经过动物试验走向临床很难得,或许未来可以定向治疗SHANK3基因缺失或病变引发的自闭症。
但他也认为,自闭症本身的基因治疗,还需要更多等待和数据。
一是因为临床试验本身有一个过程,成功与否还未可知;
二是即便通过了临床试验,后续还有NDA申请(上市申请)、FDA审查等流程;
三是该疗法本身也明确了,是针对SHANK3基因突变或缺失导致的ASD和PMS患者,这只占自闭症确诊人群的1%-2%左右。
中山大学附属第三医院主任医师邹小兵则认为,针对特定基因变异或缺失导致的自闭症患者而言,基因疗法的进展,是很有价值的一件事情。但对大多数自闭症儿童家长来说,及早发现、及时诊断和科学干预,还是目前应对自闭症的主要方式。
参考资料:
1.https://jaguargenetherapy.com/press-release/jaguar-gene-therapy-announces-fda-clearance-of-ind-to-study-jag201-in-a-genetic-form-of-autism-spectrum-disorder-and-phelan-mcdermid-syndrome/
2.G·冯, X·高, Y·梅. Shank3基因治疗方法[P].麻省理工学院: CN116406305A,2023-07-07.
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。







![基因测序行业深度研究报告:未来大健康领域黄金赛道[共77页] 基因测序行业深度研究报告:未来大健康领域黄金赛道[共77页]](/static/upload/other/20230126/1674744324488315.jpeg)