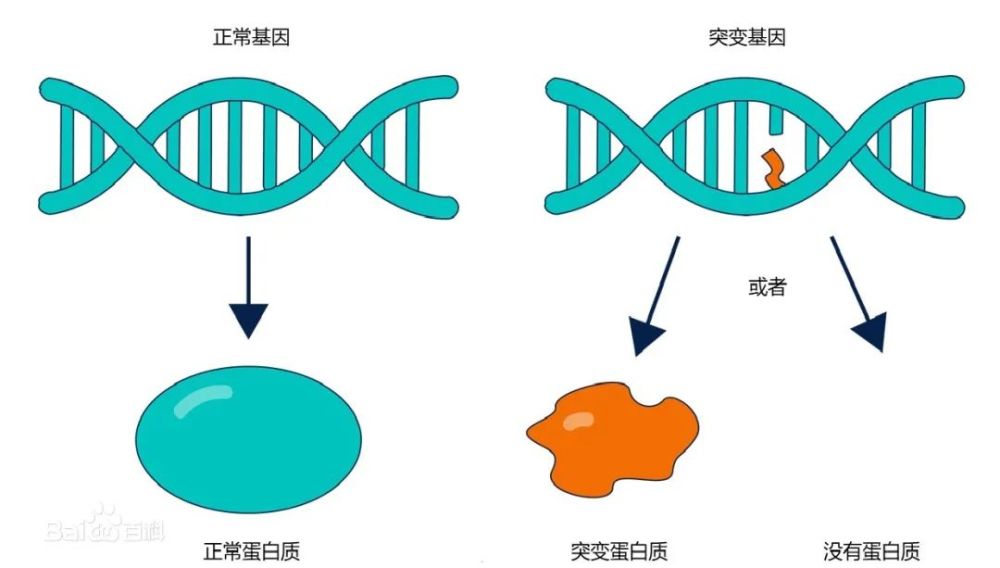
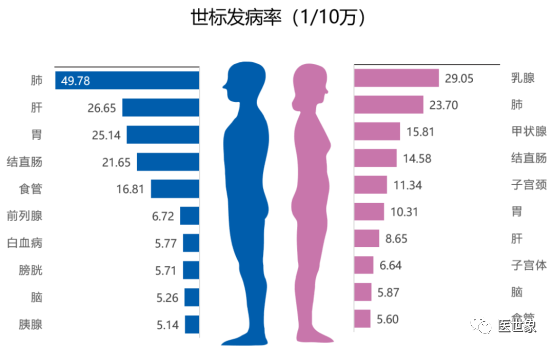
吸金超70亿,基因检测赛道上半年持续火热背后的四重变化
大概没有一个医疗赛道可以如基因检测一般,持续火热数年后,依然充满生机。
上半年,一级市场的基因检测项目共计获得超过70亿元融资,二级市场迎来3家基因检测上市公司,创造近580亿市值,基因检测的投资者、从业者、消费者都在变得成熟。伴随《医疗器械监督管理条例》的修订、上游技术平台竞争的加剧、前端生命组学数据算力和算法的崛起,基因检测产品的研发范式正面临怎样的变革?
上半年,肿瘤早筛仍然是基因检测行业的当红炸子鸡,但随着商业化落地进程的持续推进,众多的肿瘤早筛企业已经展示出分道扬镳的迹象。而肿瘤NGS的红海混战进行数年后,新药研发、MRD等更新更细分场景的出现,是否会能形成新的蓝海?
那么,左手资本与政策,右手技术与场景,红得发紫的基因检测到底蕴藏着哪些危与机?

上半年融资超70亿,产业链成熟度提升
据动脉网统计,2021年上半年,基因检测赛道共有30家公司完成了32次一级市场融资,累计金额超过70亿元。其中,宏基因组测序(mNGS)、肿瘤早筛、单细胞测序、伴随诊断仍然是基因检测赛道的投资热点,吸引了上半年投向该赛道全部资金的65%以上。
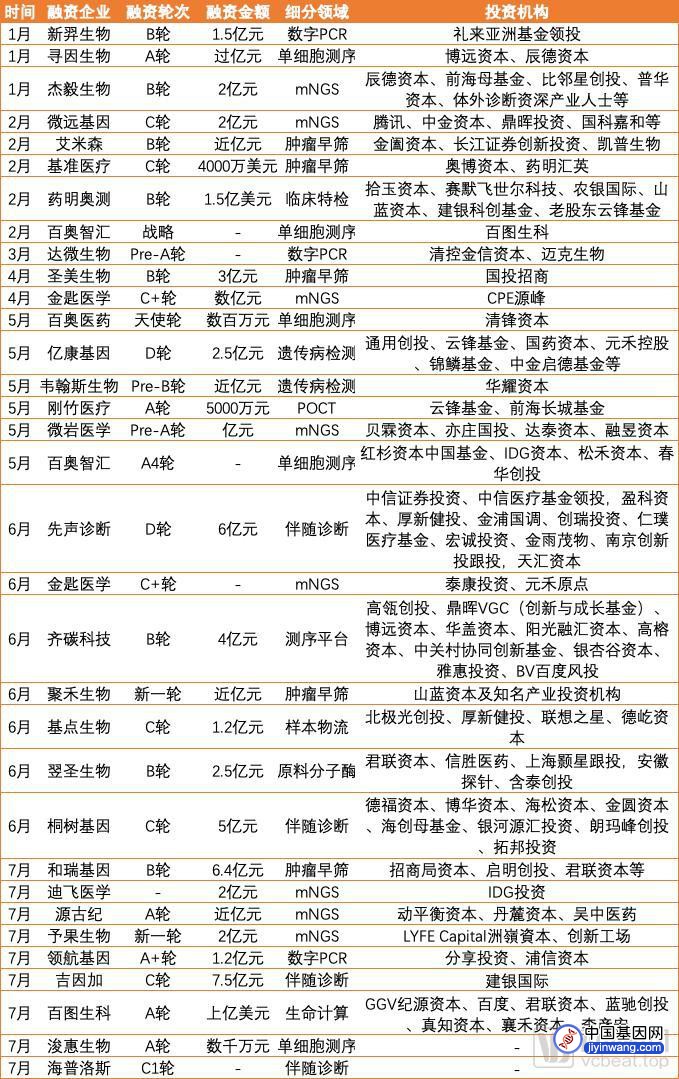
截至发稿,2021年国内基因检测赛道融资情况
对于上半年的基因检测融资,产业链成熟是绕不开的关键词。这种成熟体现在融资轮次、获投领域的产品进展和获投企业的产业链位置等方面。
首先是融资轮次。上半年,除了零星的天使轮、Pre-A轮和A轮融资事件外,均为B轮以后的中晚期融资,交易金额也从以往的百万级、千万级上升到亿元级为主。以mNGS领域为例,杰毅生物、微远基因、金匙医学、予果生物等过去两年中一直活跃着的mNGS明星项目相继完成新一轮的融资。伴随诊断的头部企业世和基因,也在前不久披露了旗下mNGS业务的融资,并一举引入IDG资本作为投资人。
mNGS融资进入更后期轮次,成交金额纷纷站上了2亿元的标准起跳线。这一方面由于随着临床研究的推进,mNGS产品开发所需的费用水涨船高,另一方面也体现了资本市场对这一领域的持续看好。不难发现,在前述mNGS项目融资中,多数早期投资人都选择了在中晚期轮次中持续跟进。例如,比邻星创投在Pre-A轮投资杰毅生物后,在B轮增持,国科嘉和则在A轮、B轮、C轮都投资了微远基因。
其次看产品进展。肿瘤早筛和单细胞测序的融资热度从去年下半年开始提升,并且在今年的上半年一直持续。7月初,贝瑞基因公告宣布子公司和瑞基因完成6.4亿元B1轮融资,是上半年肿瘤早筛企业融资额最高的一笔交易,而和瑞基因自成立以来累计完成近20亿融资,刷新了国内肿瘤早筛企业在一级市场融资的记录。
资本助力下,肿瘤早筛产品的成熟度进一步提高,各种前瞻性大队列研究、商业化落地、产品注册事件频频发生。例如,艾米森的肠癌早筛产品艾长康和宫颈癌早筛产品艾宫舒在上半年拿到了欧盟CE认证,基准医疗的膀胱癌早筛产品则获得了美国FDA的突破性医疗器械认定。
观察获投企业的产业链位置,可以发现基因检测赛道的向上趋势。齐碳科技、基点生物、翌圣生物在在上半年完成了B轮、C轮和B轮融资,募资总额近8亿元,主攻方向分别是单分子测序平台、生物低温保藏系统和分子酶,都属于基因检测服务的上游领域。此外,菲鹏生物、诺唯赞两家基因检测的上游原材料也即将上市,资本市场对基因检测的认知已经不只停留在中下游服务环节。
IPO方面,上半年延续并放大了上年燃石医学和泛生子两家基因检测企业密集上市的热度,诺辉健康、睿昂基因、诺禾致源纷纷登陆资本市场。这是继2017年华大基因、贝瑞基因相继上市3年后,基因检测领域掀起的又一次上市高潮。与上一轮上市高潮中,基因检测作为新颖技术进入二级市场不同,此时的资本市场对技术本身的认知更加成熟,企业则需要以技术、产品、场景的组合拳来说服市场。
其中,诺辉健康和诺禾致源分别摘下了“中国肿瘤早筛第一股”、“NGS科研服务第一股”的称号,睿昂基因则以血液病分子诊断为特色,加入了与上市IVD企业之列。截至发稿,诺禾致源的股价已经较发行之初翻倍。
随着凯普生物投资艾米森、赛默飞世尔投资药明奥测、IVD产业资深人士投资杰毅生物,可以隐约看到产业并购的逻辑正在进入基因检测。而产业并购正是行业经营变得如火如荼的重要标志。伴随新冠检测再造IVD行业的能量外溢,有业内人士预计,国内基因检测领域将在未来2-3年内进入爆发期。届时,渠道和产品的横向整合,检测与治疗的横向整合,将重塑整个市场的竞争格局。
政策、模式、算力驱动,基因检测研发范式正在变革
上半年,在基因检测的上游发生了两件半大事。
第一件大事是《医疗器械监督管理条例》修订带来的监管规则的明晰。以往,临床上的基因检测项目大多都没有取得产品注册证,属于仅在实验室内部研发、验证和使用的体外诊断项目,即LDT模式。尽管这种模式在国外十分常见,LDT对于技术平台、耗材选择的灵活性也更适合基因检测这样的前沿技术落地。
但监管风险始终与LDT模式相伴而生。3月18日,国务院公布修订后的《医疗器械监督管理条例》,已经从6月1日开始实施。其中的第53条规定让基因检测行业颇为振奋。第53条规定,对国内尚无同品种产品上市的体外诊断试剂,符合条件的医疗机构根据本单位的临床需要,可以自行研制,在执业医师指导下在本单位内使用。具体管理办法由国务院药品监督管理部门会同国务院卫生主管部门制定。由于“自行研制”且“在本单位内”的要求与LDT模式相近,业内认为这是LDT模式合法化的趋势。
更为重要的是,伴随LDT模式的合法化,可能会催生与IVD并行的LDT试剂注册流程。对于走在临床需求前沿,相关产品确实没有同种试剂的LDT企业而言无疑是极大的利好。尽管在实践中,LDT企业会通过室间质评或PCR实验室验收证书上加注具体检验项目的方式,来实现自身LDT业务的合法性进行背书,这种简介的认证方式,在市场冲击、监管压力之下,对于LDT企业的保护力十分有限。
随后,国家药品监督管理局、国家标准化管理委员会发布《关于进一步促进医疗器械标准化工作高质量发展的意见》,其中提出推进高通量测序等新型分子诊断技术、临床质谱技术、伴随诊断试剂、即时检验、溯源和参考测量系统等领域标准制修订工作。5月28日,国家药监局批准医疗器械标准管理中心,正式筹建医用高通量测序标准化技术归口单位。可以看出,尽管创新带来许多未知,监管端对于基因检测临床应用的支持是明确的。
第二件大事,是基因测序和芯片解决方案的全球领导者因美纳和领先的投资机构红杉资本中国基金,宣布共建智能医疗基因组学孵化器,致力于扶持生命科学初创企业。跨国企业在国内建立创新孵化中心并非新鲜事,阿斯利康、默沙东、微软等都在其列。但因美纳此举所释放出来的,这个占据全国基因测序市场近九成份额的巨头技术平台对于国内临床市场态度的转变,及这背后隐藏的基因检测上游竞争格局的复杂变化,却值得寻味。
因美纳垄断基因测序上游的地位似乎正在瓦解。当地时间7月20日,PacBio与Omniome公司前述了最终的合并协议,将以8亿美元收购后者。PacBio从事基因测序仪开发和经营的历史比因美纳更悠久,在高质量长读长测序平台技术中占有绝对优势,而Omniome的核心产品正好是高质量的短读长测序平台,所采用的SBB测序技术与因美纳专有的SBS技术路径十分接近。与Omniome合体后,长读长测序与短读长测序抱团取暖的能量无疑将挑战因美纳垄断短读长测序中多年形成的垄断市场。
挑战也来自国内。在国内,上半年,华大基因、安序源、德诺杰亿、阅微基因等大小厂商纷纷带着自主开发的基因测序仪闯进上游市场或者临床应用场景中。
3月末,贝康医疗与华大智造达成测序仪战略研发合作,双方致力于共同开发辅助生殖下一代自动化实验平台解决方案。其中,华大智造将基于胚胎单细胞水平测序研发国产化测序技术,贝康医疗则基于胚胎单细胞扩增SDWGA技术及PGT试剂盒操作流程,开发全球首个胚胎单细胞水平的自动化测序系统,并结合人工智能数据分析和报告自动生成系统。
在第二届感染性疾病诊断技术创新论坛(IDD)上,华大智造首次发布了DNBSEQ-E5基因测序仪。这款测序仪和一台笔记本电脑尺寸相当,最快能在4.5小时输出测序读长SE50的下机数据,可以即时响应特殊样本的紧急测序需求,对未知病原微生物进行快速检测。
此外,上半年,德诺杰亿、阅微基因自主研发的基因测序仪各自拿到了产品注册证。这两款基因测序仪都采用了第一次测序技术,即Sanger测序法作为技术基础。其中,阅微基因的智阅基因分析仪 GenReader 7010专为临床设计,是一款4通道基因分析系统,支持在同一反应板上设置Sanger测序和片段分析,兼容8联管和96孔板。开放式的检测平台,可同时进行多个项目检测。而安序源则通过俄罗斯Generis Biotech公司,进军欧洲市场。
最后的半件即是在上半年大火的生物计算,由于尚停留在起步阶段,其对上半年国内基因检测的影响只能算半件大事,但生物算力和算法的提升,无疑会极大改变基因检测的实践。以百图生科为代表的生物计算公司,开始尝试与众多基因检测公司建立合作生态,将样本流量与组学数据整合,以“大数据+算力”为特征的生物计算,为肿瘤基因检测产品开发基础提供了新的基础。
例如,从技术上,从“监督式学习”过渡到“无监督式学习”;从产品上,结合IoT家居产品、消费互联网数据以及互联网家庭医生,持续收集并整合个人数据实现区域、特定人群以及特定场景的基因检测甚至“C2B”研发模式。
上半年,清华大学自动化系的汪小我教授团队在Briefings in Bioinformatics上发表了基于深度学习的算法DISMIR,实现了通过血浆cfDNA的WGBS数据进行高精度的癌症检测,在将测试数据降采样到原始深度的1%之后(测序深度0.01×~0.1×),DISMIR的检测准确率AUC仍能维持在0.9左右,DISMIR与之前汪小我团队发布的cfDNA测序数据一体化分析流程软件包cfDNApipe共同构成了cfDNA液体活检数据解析的全流程解决方案。而DeepMind团队展示的基于神经网络全新设计的AlphaFold版本AlphaFold2,实现了蛋白质结构的原子水平精度预测,也为基因检测的生物标志物选择提供了更多选择。
所以在上半年,监管、产业链和数字基础的改变,带来了基因检测研发范式的改变,合规和技术成本降低的同时,整体门槛却明显提高。
从伴随诊断到药企服务,肿瘤NGS深入新药研发机理
经过了多年的混战,和在临床应用中的浮沉,肿瘤NGS企业与药企新药研发之间绑定得更深了,除了作为伴随诊断试剂为上市后的药物筛选患者,还进入了新药临床试验,为药企提供优化结果的服务。
实际上,肿瘤NGS企业为药企提供精准医学服务由来已久,一些肿瘤NGS企业原本就出自药企,例如誉衡药业与仁东医学、先声药业与先声诊断、贝达药业与瑞普基因等。上半年,燃石医学、艾德生物、求臻医学、仁东医学、泛生子等纷纷发布了药企服务的业务进展,从合作的时间线看,他们都或多或少介入了药企的临床试验。
例如,3月,基石药业的普拉替尼(Pralsetinib)胶囊通过优先审评程序,以商品名普吉华附条件上市,作为国内获批的首个RET抑制剂,用于既往接受过含铂化疗的转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。此前一年的6月,燃石医学就与基石药业合作开发Pralsetinib的伴随诊断,计划推出OncoScreen Mate (DNA+RNA) 融合检测产品。
再如,7月,泛生子联合基石药业开发的泰吉华伴随诊断试剂盒——人PDGFRA基因D842V突变检测试剂盒(PCR-荧光探针法)获国家药品监督管理局(NMPA)优先审批,并且率先尝试了与新药共同开发的模式。
在过去,肿瘤NGS企业的药企服务定制化特征明显,功能定位和服务内涵都没有标准化。这种状况在上半年有了改观。6月初,国家药品监督管理局药品审评中心(CDE)发布《生物标志物在抗肿瘤药物临床研发中应用的技术指导原则(征求意见稿)》(以下简称《指导原则》)。
《指导原则》一方面从药品监管者的视角,明确了生物标志物已逐步成为抗肿瘤药物研发过程中必不可少的一种工具,并首次对生物标志物精准筛选潜在获益人群、提高临床试验成功率、避免将获益可能性小的患者人群暴露于不必要的风险之中的功能予以确证。另一方面明确了一些技术细节,根据《指导意见》生物标志物包括基因突变、蛋白受体异常表达或者血液成分的变化等。《指导意见》同时明确的,还有不同类型的生物标志物在新药临床试验中受试者分层、富集人群、指导剂量选择、替代终点开发等作用。
从服务民生到跨界链接,肿瘤早筛的破局
2021年被业内视为肿瘤早筛的商业化元年。
有着星辰大海的肿瘤早筛,进入真正的爆发似乎已经箭在弦上。当地时间6月初,Grail在2021年ASCO年会上公布的前瞻性临床试验数据验证了Galleri的临床价值,后者如今在美国已经可以凭处方购买。这个消息极大提振了国内肿瘤早筛市场的信心。在全国两会上,全国人大代表、中国工程院院士、山东省肿瘤医院院长于金明建议将肿瘤筛查纳入医保。
上半年,DNA甲基化作为肿瘤早筛主流技术路径在更多产品开发中被广泛采用,但技术路径的迭代从未停止,比如将质谱技术应用到肺癌的早筛中。不过,最值得关注的,或许正式各家对于肿瘤早筛本身底层逻辑认知的更新,及催生出的服务民生和跨界链接两种迥然不同的商业化路径。
从某种意义上讲,参与政府民生工程并非纯粹的商业化,现阶段,民生工程对于肿瘤早筛企业更重要的价值在于以高成本换取大数据。这个过程中,肿瘤早筛产品优于传统筛查工具的阳性预测能力被验证和优化,并最终将其卫生经济学效益量化。上半年,鹍远生物、华大基因、世和基因、泰莱生物等企业参与为为数众多的政府民生项目。
总体而言,政府民生项目具有体量大、周期长的特点。例如,6月,江苏政府采购网公示,泰州医药高新区卫生局、泰州市高港区卫生健康委员会拟以5000万元预算金额,向拟定健为医学采购基于粪便样本的幽门螺杆菌核酸检测和结直肠癌早期筛查技术,后者是业内知名度更高的康为世纪的关联公司。
再如,同样是6月大型肿瘤早筛公益项目金陵队列宣布完成首站试点,12天时间为262位居民完成癌症早筛检查。金陵队列在南京江北新区卫生健康和民政局的支持下,以中国工程院沈洪兵院士为主要发起人,带领南京医科大学及世和基因等专业团队,为南京市居民免费提供10万例肿瘤早筛检测。据了解,“金陵队列I期”将惠及江北新区范围内约1.5万名45-75周岁符合参与要求的居民,重点筛查肺癌、结直肠癌和肝癌三个癌种,随访5年。
另一种路径是跨界合作。这种路径通常直接面对用户,以产品资质为基础,强调对于肿瘤的阴性预测价值,以提高市场渗透率、实现产品放量为目标。
比如,与商业保险合作。目前,肿瘤早筛与商业保险合作主要有前端和后端两种模式。在前端模式中,用户采购肿瘤早筛产品的同时获赠健康险的保障权益,是相对传统的产品+保险模式。后端模式则可以面向带病体,将肿瘤早筛产品设计进保险条款中,从而获得商业保险的导流,这种模式主要发生互联网保险平台中,如和瑞基因与阿里健康合作,为乙肝用户提供保障。
此外,与大型药企的医学市场部门合作,借助后者的医疗资源向院内渗透。比如,泛生子与正大天晴,就基于液体活检技术的肝癌早筛产品HCC screen签署中国独家战略合作协议;诺辉健康也在年初宣布了与阿斯利康中国的三年合作计划。
此外,拿下国内癌症早筛第一证的诺辉健康采用了更多元的跨界链接方式,除了与京东健康、阿里健康等互联网医疗平台合作推广外,还将肿瘤早筛的C端渠道拓展到专业的医学直播中,导入抖音、快手等短视频的巨大流量。在目前看到的肿瘤早筛商业化路径中,直接2C是对传统IVD行业代理商的经营模式颠覆最大的一种,也将可能是放量最快的一种。接下来还看诺辉健康如何真正实现渗透。
实际上,无论服务民生还是跨界链接,尽管底层逻辑不同,对于肿瘤早筛行业的意义是一致的,即批量拓展市场覆盖范围,也都面临着产品衔接、资源对接等环节的挑战,肿瘤早筛商业化元年的战绩如何,还需要用更多的数据来分辨。
新热点:MRD临床价值被验证还需要5年
微小残留病灶监测(MRD),是上半年基因检测新场景中绝对的热点,一众在院内提供基因检测的厂商,不是已经开发了MRD产品,便是正在准备开发这类产品的路上。
据动脉网不完全统计,2021年以来,桐树基因、慧渡医疗、泛生子、至本医疗等纷纷发布了自己的MRD监测产品,泛因医学的血液肿瘤MRD检测产品更是获得了欧盟的CE准入资质,闯入海外市场。此外,世和基因与中山大学、复旦大学等研究机构共同完成的国内首个多中心前瞻性肠癌MRD研究结果,在《Journal of Hematology & Oncolology》上正式发表,和瑞基因也计划在下半年布局MRD。
与此同时,临床端对于MRD的应用也表现出极大的认可。例如,在第18届中国肺癌高峰论坛上,国内首个《肺癌MRD的检测和临床应用共识》发布。明确肺癌MRD指的是经过治疗后,传统影像学(包括PET/CT)或实验室方法不能发现,但通过液体活检发现的癌来源分子异常,例如外周血可稳定检出丰度≥0.02%的ctDNA,包括肺癌驱动基因或其他的I/II 类基因变异,代表着肺癌的持续存在和临床进展可能。
不难发现,从NIPT、肿瘤NGS到mNGS,再到肿瘤早筛,定位新的热门应用场景,一直是基因检测新手和老兵皆宜的打法。但MRD是否真就是肿瘤NGS红海的一剂解药?或许还为时尚早。在7月举行的2021复旦中山液体活检临床应用高峰论坛上,吴一龙教授曾在主题报告中表示,MRD的临床价值完全被验证还需约5年。
诚然,任何一种基因检测产品落地的背后,都伴随着技术细节的标准化和临床价值的反复确认,MRD亦如此。而MRD的应用一旦铺开,则无疑会再造一个体量比伴随诊断更大的基因检测细分市场。
一直以来,关于基因检测赛道被资本催熟的质疑不绝于耳。但基因检测企业的研发投入比率远高于传统IVD行业是不争的事实。经过多年的发展,基因检测如同清道夫,在遗传疾病、肿瘤、传染疾病诊断场景中解决了许多复杂问题,让相对高端的特检项目在临床检验中拥有了更高的声量。
未来,临床常规检验项目的集约化、特检项目的专业化无疑是医学检验的发展趋势。对于基因检测企业而言,技术壁垒是先天优势,但如何与临床真实需求,甚至更广泛的大健康需求相结合,仍是跑步前进道路上需要解决的问题。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。