海马基因点突变导致“脾脏丢失”与“雄性怀孕”的协同进化机制取得进展
近日,中科院南海海洋研究所热带海洋生物资源与生态重点实验室林强研究员团队取得了“基因单个位点敲除导致整个动物器官丢失”的创新性研究进展,揭示了海马基因tlx1的特异性位点突变(tlx1A208T)调控其脾脏丢失的遗传机制,并首次提出海马“脾脏丢失”与“雄性怀孕”协同演化的新观点。德国康斯坦茨大学、基尔大学研究团队在免疫耐受研究层面进行了联合解析,相关研究成果于12月9日在线发表于Nature Communications(《自然·通讯》)。
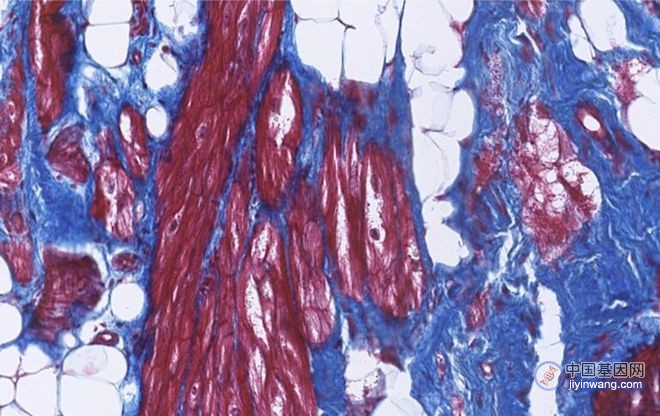
在动物界中,海龙科诸多物种“脾脏丢失”这一复杂性状是脊椎动物最为特异的进化特征之一(图1),也是当前国际学术界在鱼类演化领域所关注的焦点。海龙科鱼类具有“雄性怀孕”的独特繁殖模式,而作为“雄性怀孕”重要器官的育儿袋在进化过程中展现出了多种形式(Science Advances, 2021),并与哺乳动物的子宫呈现结构与基因的趋同进化现象(Nature, 2016; National Science Review, 2021)。在脊椎动物中,“雌性怀孕”已经独立进化了150多次,虽然这一繁殖策略为后代提供了明显的生存优势,但亲本在妊娠期间却一直经受着免疫耐受与免疫保护的权衡,即如何平衡亲本耐受与异体胚胎的免疫保护?在该研究领域,哺乳动物胚胎发育过程中的免疫调控研究报道较多,而“雄性怀孕”繁殖系统作为在脊椎动物中的一个全新研究体系,其雄性怀孕与免疫系统的协同进化机理仍是未知。
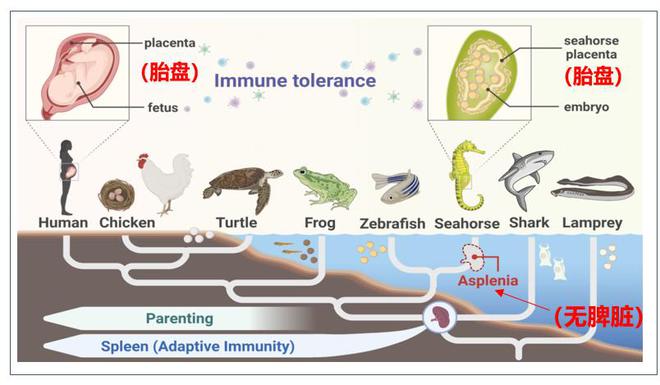
海马脾脏丢失及其独特的繁殖特征
动物进化多样性与免疫系统的复杂性是密切相关的。脾脏作为免疫系统的重要器官,在机体免疫过程中发挥着重要作用。海马等物种缺少脾脏,这在脊椎动物中是非常罕见的特异进化事件;那么,海马脾脏丢失的遗传基础如何?其免疫系统上的缺陷与“雄性怀孕”繁殖策略之间的进化关系如何?
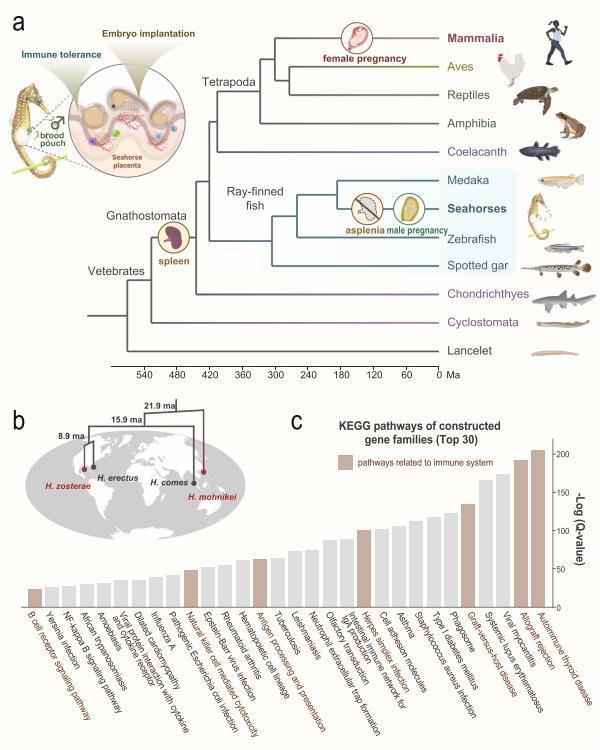
海马繁殖策略演化及其免疫系统关键基因丢失
基于上述科学问题,研究团队首先将海马与其他9个不同目的硬骨鱼进行比较基因组学分析,发现海马属中有1260个基因家族显著收缩。涵盖了多个免疫相关通路,如NOD样受体通路、异体移植物排斥反应、抗原处理和呈递等,基因丢失(gene loss)分析也同样支持这一结论(图2)。这一结果表明免疫相关基因家族的收缩或丢失在很大程度上促进了海马免疫系统中的修饰,并可能与其“雄性怀孕”及育儿袋结构的特异进化有关。
研究团队进一步聚焦海马“脾脏丢失”的遗传与进化机制解析。全基因组谱系特异性突变(lineage-specific mutation)分析表明,18种海马T-cell leukemia homeobox 1 (tlx1)基因的homeobox结构域存在一个谱系特异性位点突变(即丙氨酸Alanine→苏氨酸Threonine,tlx1A208T)(图3)。而特别值得注意的是,作为海马的近缘物种绿海龙(Syngnathoides)则保留有完整的脾脏,并且不存在该位点突变。
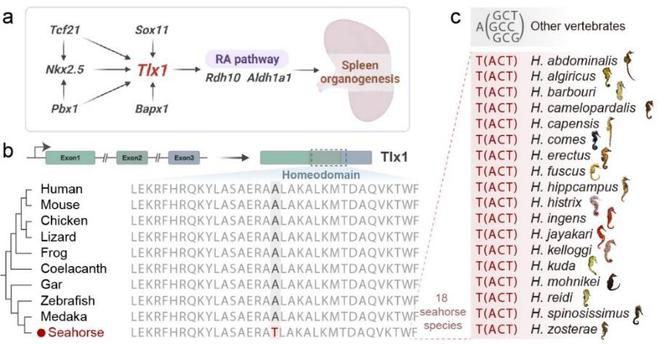
海马属tlx1基因的特异性位点突变
已有研究表明,tlx1是人、小鼠等脾脏发育的关键转录因子。基于上述分析结果,推测该位点的突变(tlx1A208T)可能是导致海马脾脏丢失的关键因素。因此,为了证实这一假设,团队利用模式物种斑马鱼实施了3次CRISPR/Cas9基因敲除验证,结果表明, 1、全基因tlx1敲除突变品系斑马鱼(tlx1 knockout)全部表现为先天性脾脏丢失(11/11),2、针对海马特异性位点的突变品系斑马鱼(tlx1A208T)亦出现脾脏丢失(27/27),3、相邻位点的突变品系斑马鱼(tlx1A207T)则有完整的脾脏(17/17),该结果精确验证了海马tlx1A208T位点的进化特异性和功能保守性(图4)。
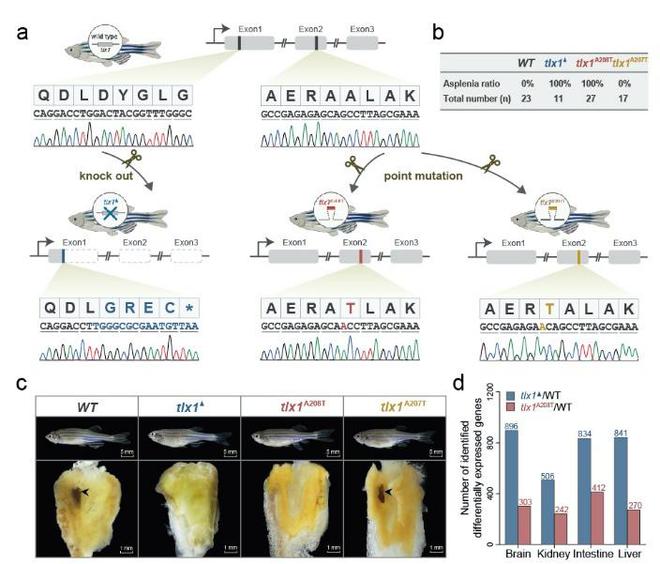
CRISPR/Cas9基因编辑揭示tlx1基因的错义突变导致斑马鱼无脾
众所周知,动物胎生过程中成功妊娠的前提是受精卵的顺利着床。尽管被母体免疫细胞识别,但母体-胎儿界面经历了免疫排异和免疫保护的动态变化,最终保障胎儿在子宫内正常发育。研究团队发现,在脾脏丢失的基础上,海龙科物种中许多涉及抗原识别和呈递、T/B淋巴细胞发育、补体激活等过程的基因均存在谱系特异性丢失或结构变异,这一结果也证实了海龙科物种为了实现其怀孕过程而出现了关键免疫基因家族或部分调控通路的协同演化(图5)。
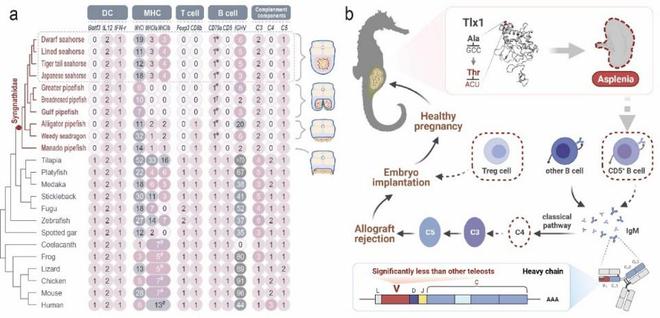
海马脾脏丢失和雄性怀孕的免疫基因组学基础
综上,该研究发现并证实了海马基因单位点突变(tlx1A208T)导致其脾脏丢失的假设,首次提出了海龙科鱼类“脾脏丢失”与“雄性怀孕”协同进化的新观点。相关成果拓展了学术界对脊椎动物繁殖过程中免疫系统适应进化的理解,并有望为医学上“无脾综合征”研究开辟新的思路。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。