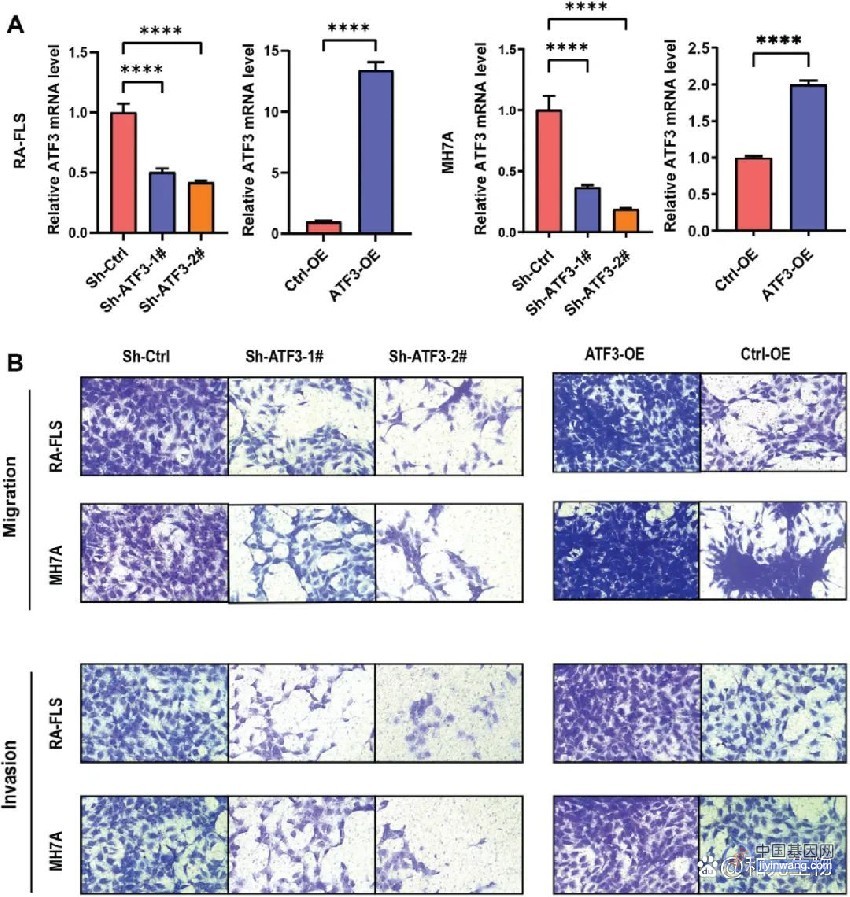
除了BRCA,还有哪些乳腺癌易感基因?应该如何进行筛查?
根据2021年世界卫生组织国际癌症研究机构(IARC)发布的数据:乳腺癌已取代肺癌成为全世界最常见的癌症。通过筛查提高乳腺癌早诊早治水平是改善患者预后的关键所在。已有研究证实,除了BRCA1、BRCA2以外,ATM、CHEK2和PALB2等也是乳腺癌的易感基因,但目前仍缺少对携带ATM、CHEK2和PALB2致病突变女性的乳腺癌筛查策略。
乳腺癌易感基因:不仅有BRCA1、BRCA2,还有……
在“朱丽效应”影响下,上世纪八九十年代发现的BRCA1、BRCA2已经成为家喻户晓的乳腺癌遗传易感基因。然而,除了BRCA1/2以外,是否还要其他乳腺癌易感基因?
2021年,NEJM杂志发表了一项由梅奥诊所和剑桥大学领导的研究,对全球25个国家超过11.3万名女性(60466名乳腺癌患者和53461名对照女性)的34个潜在易感基因进行了检测。结果发现,发现5个基因的蛋白截断变异与乳腺癌整体风险相关,除了大家熟知的BRCA1和BRCA2以外,另外3个是ATM、CHEK2和PALB2。与普通女性相比,上述基因变异的癌症风险分别为2.1~10.57倍不等。
按照ER阳性或阴性乳腺癌,BRCA1、BRCA2、PALB2、CHEK2、PTEN和ATM的蛋白截断变异与ER阳性乳腺癌风险增加有关,而BARD1、BRCA1、BRCA2、PALB2、RAD51C和RAD51D的蛋白截断变异则与ER阴性癌症风险增加有关。
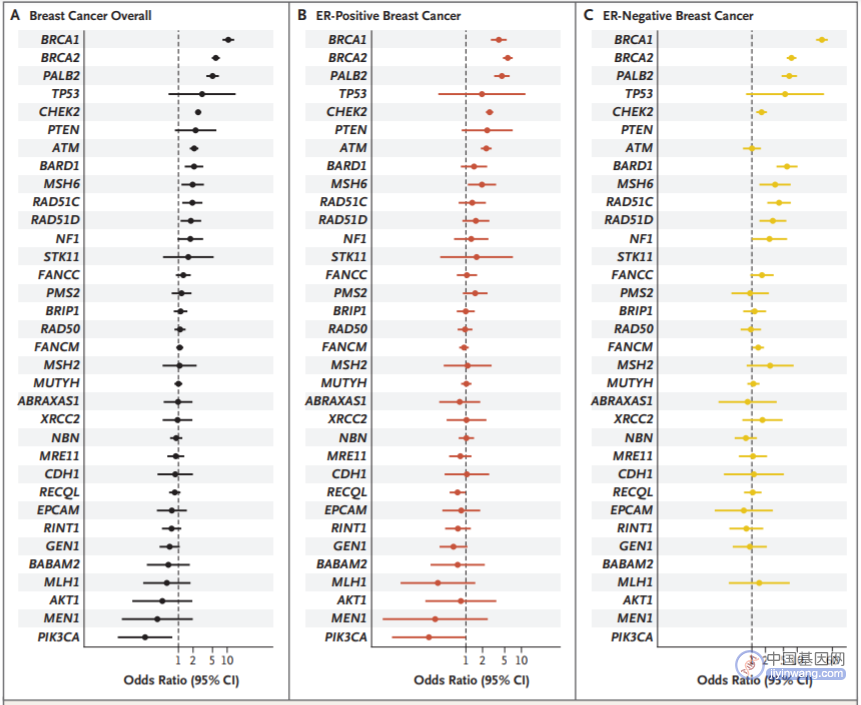
Δ不同基因突变的总体乳腺癌风险和ER+/-乳腺癌风险
尽管上述研究确定了有临床意义的乳腺癌易感基因,但目前临床上的乳腺癌筛查策略包含的易感基因仅有BRCA1/2突变。例如,美国USPSTF建议对乳腺癌、卵巢癌、输卵管癌、腹膜癌或有BRCA1/2基因突变家族史的人群进行风险评估,风险阳性人群应接受遗传咨询、基因检测等。《中国抗癌协会乳腺癌诊治指南与规范》建议将MRI联合X线用于BRCA1/2突变携带者的乳腺癌筛查。

ΔUSPSTF指南推荐

ΔCBCS指南
虽然NCCN指南建议,对于携带ATM和CHEK2(40岁开始)、PALB2(30岁开始)阳性突变的女性可以考虑每年进行一次X线和MRI检查。但整体上,当前国内外指南对BRCA1/2突变以外的致病性突变女性,仍缺乏具体的乳腺癌筛查建议。
ATM、CHEK2和PALB2突变的乳腺癌筛查策略
尽管对于携带ATM、CHEK2和PALB2致病性突变的女性,一些指南建议可以进行乳房X线和MRI筛查。但很少有数据可以指导这些女性的筛查方案。2月17日,JAMA oncology在线发表的一项研究,旨在评估ATM、CHEK2和PALB2致病性突变女性的不同起始筛查策略。

这项比较建模分析使用了癌症干预和监测建模网络(CISNET)的两个已建立的乳腺癌微模拟模型来评估不同的筛查策略,在12项以人群为基础的研究中,使用与易感性(携带者)相关的癌症风险估计联盟(cancer Risk Estimates)的汇总数据,对32247名乳腺癌病例和32544名对照人群进行了年龄特异性乳腺癌风险估计。
筛查起始年龄包括从25岁、30岁、35岁或40岁开始,一直到74岁,筛查方法为每年一次的钼靶和MRI检查。
研究结果显示,不同致病性突变女性的估计终生乳腺癌风险如下:
• ATM:20.9%(18.1%-23.7%),
• CHEK2:27.6%(23.4%-31.7%),
• PALB2:39.5%(35.6%-43.3%)。
在所有致病性突变中,与未筛查相比:
• 从40岁开始进行乳腺钼靶筛查可使乳腺癌死亡率降低36.4%~38.5%。
• 从35岁开始每年进行MRI筛查,然后从40岁开始每年进行钼靶联合MRI筛查,可使乳腺癌死亡率降低54.4%~57.6%。每1000名女性中,大约有4611~5001例假阳性筛查和1280~1368例良性活检。
• 从30岁开始进行MRI筛查,然后从40岁开始每年进行钼靶联合MRI筛查,可使乳腺癌死亡率降低55.4%~59.5%。每1000名女性中,大约有5075~5415例假阳性筛查和1439~1528例良性活检。
• 对于30岁开始MRI筛查,并且30岁或40岁开始联合钼靶筛查,二者之间的乳腺癌死亡率降低没有显著差异(0.1%~0.3%),但是如果30岁就开始MRI联合钼靶筛查,假阳性筛查会增加649~650例/1000名女性,良性活检会增加58~59例/1000名女性。
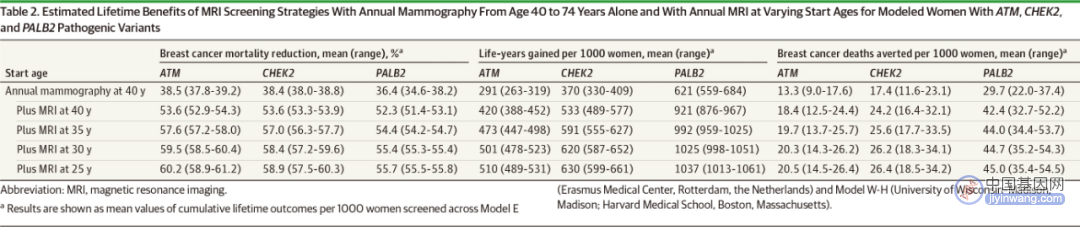
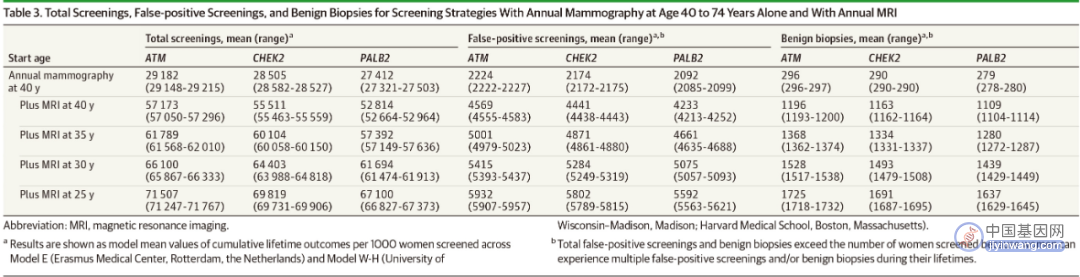

Δ不同筛查起始年龄、筛查方法的获益情况
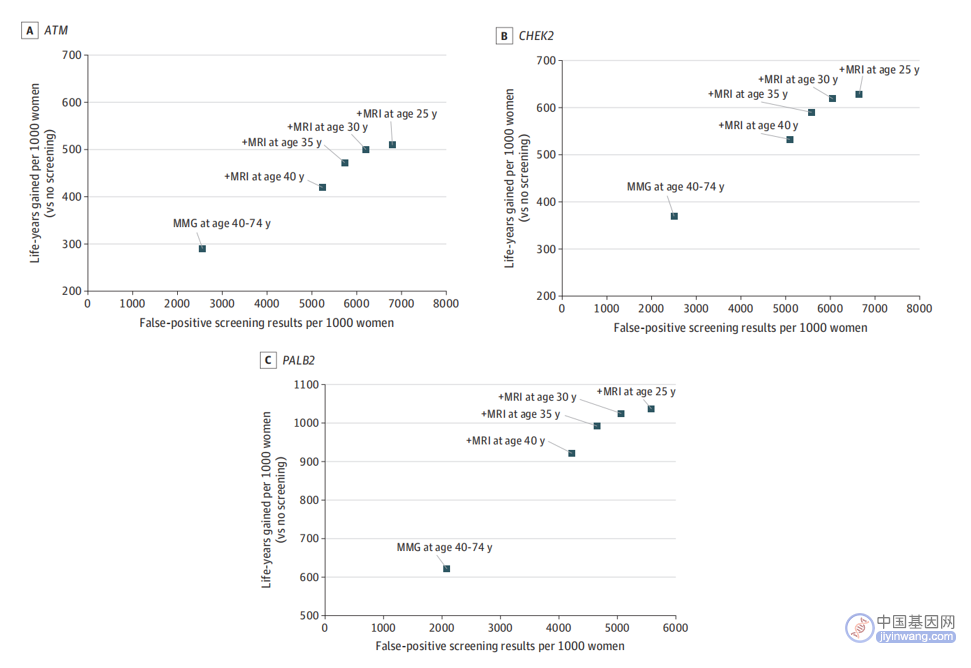
Δ不同致病性突变女性的假阳性筛查和生命延长
该研究结果表明,从30至35岁开始进行MRI筛查,然后在40岁时进行MRI联合钼靶筛查,可能会使携带ATM、CHEK2和PALB2致病性突变女性的乳腺癌死亡率降低50%以上。在MRI筛查中,40岁之前联合钼靶筛查可能没有额外的益处。
参考文献:
[1]Breast Cancer Association Consortium, et al. Breast Cancer Risk Genes - Association Analysis in More than 113,000 Women. N Engl J Med. 2021 Jan 20. doi: 10.1056/NEJMoa1913948.
[2]Jin J. Should I Be Tested for BRCA Mutations?. JAMA. 2019;322(7):702. doi:10.1001/jama.2019.11251
[3]中国抗癌协会乳腺癌专业委员会.中国抗癌协会乳腺癌诊治指南与规范(2021年版)[J].中国癌症杂志,2021,31(10):954-1040.
[4]National Comprehensive Cancer Network.NCCN clinical practice guidelines in oncology:genetic/familial high-risk assessment: breast,ovarian, and pancreatic. Version 1.2022-August 11,2021. Accessed November 17, 2021.
[5]Lowry KP, Geuzinge HA, Stout NK, et al. Breast Cancer Screening Strategies for Women With ATM, CHEK2, and PALB2 Pathogenic Variants: A Comparative Modeling Analysis [published online ahead of print, 2022 Feb 17]. JAMA Oncol. 2022;10.1001/jamaoncol.2021.6204.
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。