中美团队合作开发基因遗传信息新模型 精准预测冠心病患病风险

记者7日从中国科学院北京基因组研究所(国家生物信息中心)获悉,为实现对个体未来罹患冠心病风险的精准预测,该所汪敏先团队与美国博德研究所Amit V. Khera团队合作,最新成功开发出基于基因遗传信息预测冠心病患病风险的新模型,有望在冠心病高风险人群的早期识别及精确分层上发挥作用,促进冠心病精准防治。
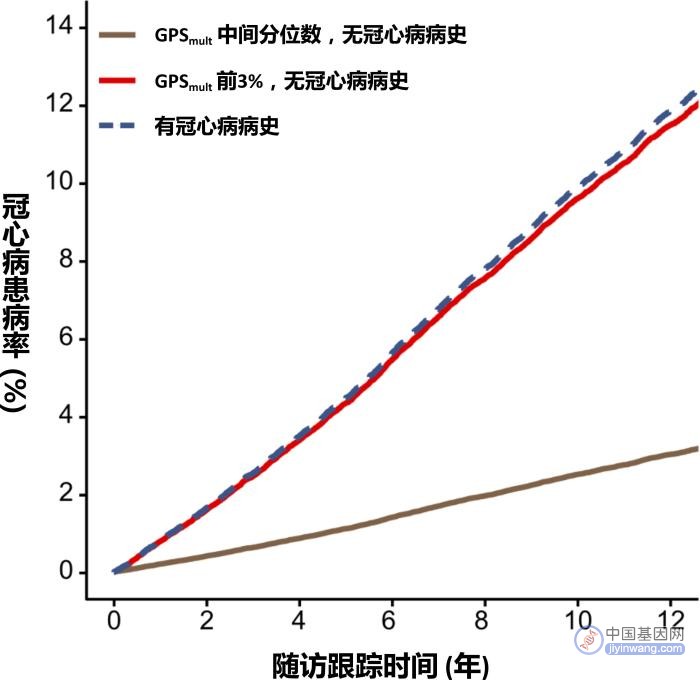
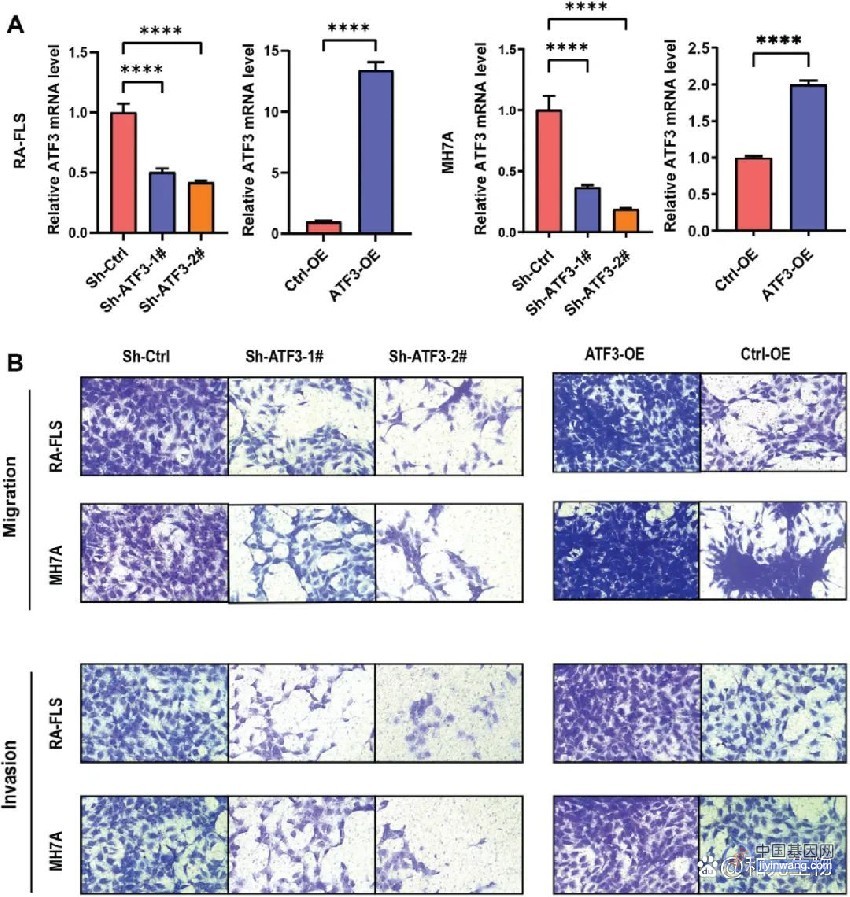
GPSmult识别的3%高风险个体发病风险与有既往病史的个体疾病风险相当。中科院北京基因组所供图
准确性超美国“金标准”
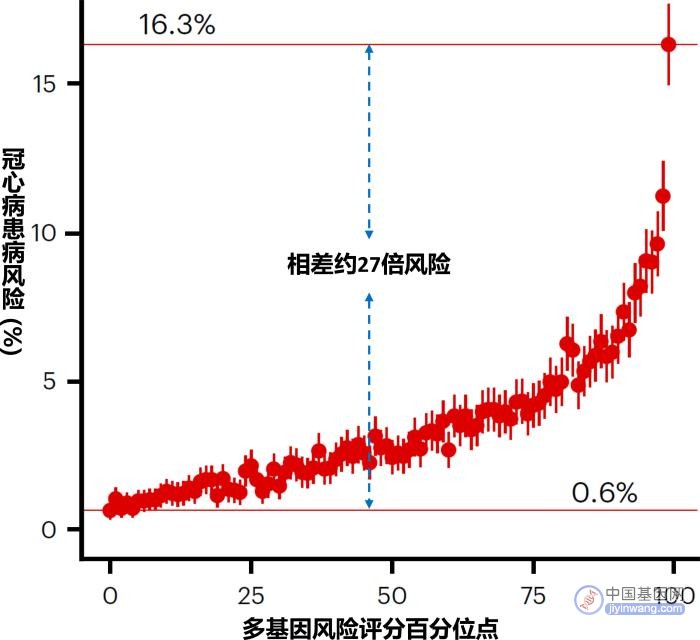
冠心病患病风险与多基因风险评分分布之间的关系。中科院北京基因组所供图
本项研究中,中美合作团队在利用冠心病单族裔及单疾病遗传关联信息的模型基础上,进一步开发整合不同族裔人群背景及多个冠心病临床危险因素信息的全基因组多基因风险评分新模型GPSmult。
该模型预测的准确性超过美国临床预防医学领域用于评估个体动脉粥样硬化性心血管疾病患病风险的“金标准”——美国心脏病学会/美国心脏协会合并队列方程组,大幅提高利用基因组遗传信息预测个体未来患冠心病风险的准确度,能够进一步改善约40%个体的风险预测准确性。
这项医疗健康领域重要成果论文,北京时间7月6日夜间在国际专业学术期刊《自然-医学》(Nature Medicine)在线发表,美方合作机构还包括麻省总医院、哈佛大学医学院和斯坦福大学医学院等。
大数据训练和验证预测模型
论文共同第一作者和共同通讯作者汪敏先研究员介绍说,利用来源于冠心病全基因组关联研究国际联盟的、全球多个族裔人群近27万例冠心病患者和118万例健康人群的全基因组对比关联研究结果,GPSmult首先分析基因变异与疾病之间的相关关系,随后对全基因组范围内与疾病风险相关的所有遗传变异位点进行建模整合。
为提高模型预测准确性,合作团队进一步整合基因变异与10种冠心病临床危险因素及关联共病之间的关联关系,使用样本数超过1346万例。在多族裔人群背景、总计超51万人的独立验证人群中,对GPSmult的准确性进行全面评估显示,与当前已发表的27种基于全基因组信息预测冠心病风险的模型相比,该新模型的准确性均有显著提升。
比较来看,美国心脏协会/美国心脏病学会合并队列方程主要利用血脂、血压、年龄及性别等传统心血管疾病危险因素建模,预测个体未来10年的动脉粥样硬化性心血管疾病风险,而GPSmult基于个体基因信息量化个体先天疾病风险,将两种模型整合使用预测效果更优。
通过对英国生物银行中32.6万多族裔人群的数据分析显示,在传统风险模型的多个疾病风险分层中,GPSmult均能进一步增强对个体患病风险的预测,且广泛适用于不同遗传背景的个体,特别是对南亚人群或者是传统危险分层处于高风险(风险大于20%)的个体,其增强效果更加明显。
正在开发人工智能模型
汪敏先指出,冠心病是导致人类死亡的最主要疾病之一,受个体遗传、代谢及不良生活方式的共同影响,其中遗传因素的影响约为40%-60%。由于个体基因信息在一生中基本保持不变,并且早在婴幼儿时期即可通过血液或唾液等无创方式采集获得,因此,GPSmult能在生命最早期基于个体基因信息预测其未来发生冠心病的风险,从而可为尽早预防与干预疾病争取广阔的时间窗口。
中科院北京基因组所透露,汪敏先团队长期致力于利用人群队列遗传大数据解析冠心病等心血管复杂疾病的遗传基础与机制,预测疾病未来发生风险。除利用基因遗传信息外,该团队正在开展利用人脸、眼底照片和计算机断层(CT)扫描、核磁共振等相关影像数据,开发人工智能模型,从医学影像学数据中提取疾病风险特征,从而表征和量化个体后天风险,整合先天遗传和后天环境因素等生命周期多阶段信息开发更加精准的风险预测新模型,促进个体健康管理。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。