高占成教授等:基因易感性与重症肺炎之间的内在关联
社区获得性肺炎(community-acquired pneumonia, CAP)是全球范围内最常见的感染性疾病之一,临床表现异质性高,轻症表现为呼吸急促和咳痰,重症表现为发热、呼吸窘迫和脓毒症。在美国,CAP是住院的第二大病因,并且是最常见的感染性死因,每年在美国10万成年人中约有650人因CAP住院。
大部分CAP患者经过一段时间的抗感染治疗即可痊愈,但也有部分患者的肺炎较为严重,病情进展迅速,快速进展为重症肺炎,随后可能因急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)或感染性休克而死亡。此前一些研究显示,肺炎的易感性及严重程度同时受到基因和外界环境的影响,基因的影响往往反映了在人群中某些易感基因的多态性。重症肺炎相关的易感基因涉及多个功能通路,主要包括:炎症因子、细胞表面蛋白等,通过不同基因型对宿主免疫状态、病原体清除等方面产生影响,从而导致肺炎的病程具有异质性。
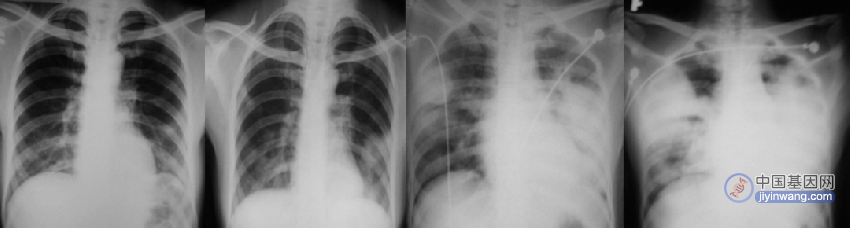
一、重症肺炎概述
在ATS/IDSA 2019年发布的成人社区获得性肺炎诊断与治疗临床指南中,重症肺炎的定义仍沿用2007年发布的指南,即满足1项主要标准或3项次要标准,其中主要标准为:呼吸衰竭需要机械通气,脓毒症休克需要血管升压药物;次要标准有:呼吸频率≥30次/分,氧合指数(PaO2/FiO2) <250mmHg,多肺叶浸润,意识或定向力障碍,高尿素血症(尿素氮≥7.1mmol/L),感染所致的白细胞减少(外周血白细胞计数<4×109/L),血小板减少[血小板计数(PLT<100×109/ L)],体温过低(核心温度<36℃),低血压需要积极地实施液体复苏。在后续的验证研究中,该标准对预测是否需要机械通气、血管升压支持表现出较好的效用,许多研究也以该标准对重症肺炎进行判别。
此外,肺炎严重指数(pneumonia severity index, PSI)和CURB-65评分系统也是临床实践中常用的肺炎严重程度的分级方法。PSI的评价因素来源于病史、体格检查、影像学检查及实验室检查结果,它可以将患者以初诊后30d内全因死亡风险分为5个等级。在肺炎预后研究小组(pneumonia patient outcomes research team,PORT)研究中,PSI Ⅰ、Ⅱ、Ⅲ级对应的30天死亡率分别为0.1%、0.6%和0.9%,而PSI Ⅳ、Ⅴ级对应的死亡率则分别为9.3%和27.0% 。CURB-65评分以是否存在意识改变、高尿素血症(尿素氮≥7mmol/L)、呼吸频率≥30次/分、收缩压<90mmHg或舒张压≤60mmHg及年龄≥65岁为评分依据(每项1分),将患者肺炎的严重程度评为0~5分。在推导队列中,其0~4分分别对应的30天全因死亡率分别为0.7%、2.1%、9.2%、14.5%和40.0%(评分为5分的患者过少)。CURB-65评分≥3分也作为部分研究中重症肺炎的判别标准。
二、与肺炎严重程度相关的基因易感性
1. 细胞因子相关基因:
细胞因子(cytokine)是一组蛋白质或多肽,在生物体内一般充当生物信号的传递者,可以由多种细胞释放。在发生作用时,每个细胞因子一般与特定的细胞表面受体结合,利用细胞内信号传导途径来改变细胞功能。细胞因子在免疫功能中发挥着重要作用,并且其功能也涉及多个胚胎发育环节。根据结构与功能的不同,细胞因子大致可以分为6大类,即:白细胞介素、干扰素、肿瘤坏死因子、集落刺激因子、生长因子和趋化因子。其中,以白介素和肿瘤坏死因子的基因型与重症肺炎的关系最为密切。
白细胞介素(interleukin,IL,简称白介素)与重症肺炎及其并发症有着紧密的关联。据报道,IL-1RN的SNP位点rs315952C与更低的ARDS发生率相关,可能的机制是IL1RA的表达水平增加。IL-6 -597G/A(rs1800797)和IL-10-592C/A (rs1800872)都与CAP的易感性和严重程度相关。而IL-10启动子基因1082GG(rs1800896)会使CAP或肺炎链球菌感染期间IL-10的水平明显增加,同时疾病的严重程度(重症肺炎发生率)、感染性休克和死亡率也会明显增加。
肿瘤坏死因子在炎症过程的发生发展中也起着重要作用,其结构或表达水平的改变都会对炎症过程产生影响。袁伟锋等的研究确定了肿瘤坏死因子-α(TNF-α)启动子序列上的5个多态性位点,并且-863A与-308A等位基因携带者患肺炎后发展为重症肺炎的概率更高,与5个多态性位点都为野生型的人群相比,拥有至少1个突变型的肺炎患者,其重症肺炎的发生率也较高。后续研究也发现,-308A等位基因(rs1800629)携带者更易发生脓毒症和感染性休克,并且其死亡率也更高。此外,肿瘤坏死因子受体(TNFR)中,携带TNFR1 -609T以及TNFR2 +1690C等位基因的个体,发展为重症肺炎的风险更高。
其他的一些细胞因子如IL-4、γ干扰素(IFN-γ)以及趋化因子CCL2、CCL5等多与特定病原体感染[如鼻病毒肺炎、严重急性呼吸综合征(SARS)等]的易感性相关,而与重症肺炎的发生率或肺炎的严重程度之间的关系尚需进一步研究。
2. 白细胞分化抗原:
白细胞分化抗原是指造血干细胞在分化成成熟血细胞的不同谱系和分化阶段中出现或消失的表面分子,同一小鼠抗人白细胞单克隆抗体所识别的同一种白细胞分化抗原称为同一分化群(cluster of differentiation, CD),包括CD14LPS受体,CD55DAS及CD209DC-SIGN。
CD14分子主要产生于巨噬细胞,属于固有免疫系统的一部分。它通过结合脂多糖(lipopolysaccharide,LPS)来识别细菌组分。此外,CD14也可以作为Toll样受体4(toll-like receptor 4,TLR4)的共受体发挥作用。在已有的研究中,CD14 -159CC (rs2563298) 个体在感染冠状病毒(SARS-CoV)或肺炎链球菌后都表现出更严重的症状,这可能与CD14-159CC个体中sCD14的水平较低、病原体载量较高有关。
CD209,也称树突状细胞特异性细胞间黏附分子-3-结合非整合素(dendritic cell-specific intercellular adhesion molecule-3-grabbing non-integrin,DC-SIGN),是介导病原体-树突状细胞及树突状细胞间通讯的重要分子。此前的研究表明,与原始型CD209 -336A个体相比,CD209 -336G个体在感染SARS后LDH水平更高,提示CD209基因的多态性会影响SARS患者的病情严重程度;此外,CD209 -336G个体CD209启动子序列对SP1和AP2蛋白的结合能力都更强,提示该突变位点可能通过改变CD209的表达水平进而改变宿主状态最终导致疾病严重程度不同。
CD55又称衰变加速因子(decay accelerating factor,DAF),表达于外周血细胞、内皮细胞和各种黏膜上皮细胞表面,其主要作用可以与补体C2竞争性地结合C4b,从而避免补体介导的细胞杀伤作用。此前的研究表明,在H1N1感染个体中,CD55的多态性(rs2564978)与流感的严重程度密切相关,这一效应可能是由于不同基因型个体呼吸道上皮细胞中CD55的表达水平不同,因而上皮细胞被补体杀伤情况不同导致的。
3. 其他
肺表面活性蛋白B(pulmonary surfactant-associated protein B,SFTPB)表达于肺泡内,可以将肺泡壁脂质分子重排以保证小肺泡通气。在此前的研究中,研究人员在非裔美国人中确定了SFTPB的不同基因型会对CAP的严重程度产生影响;SFTPB对CAP严重程度影响的机制可能涉及蛋白质结构变化(rs1130866)、影响SFTPB转录(rs3024793)以及mRNA稳定性(rs7316)等。后续的研究也证实,rs1130866位点与流感肺炎的严重程度相关,相较C/T和T/T基因型,C/C个体的流感重症率更高,预后更差。
维生素D受体(vitamin D receptor,VDR),也称为骨化三醇受体(calcitriol receptor),其编码基因位于12号染色体长臂(12q13.11)。在与骨化三醇(维生素D的活性形式)结合后,与维A酸X受体共同形成异二聚体并进入细胞核与基因组DNA上的维生素D反应元件(vitamin D responsive elements,VDRE)结合,促进或抑制特定基因的转录行为。维生素D可以通过VDR调节淋巴细胞和巨噬细胞的增殖、成熟以及细胞因子表达,从而发挥免疫调节作用。VDR基因rs2228570 T等位基因的存在显著增加了RSV细支气管炎的风险并且与死亡风险增高相关。
人类白细胞抗原(human leukocyte antigen, HLA)是编码人类主要组织相容性复合体(major histocompatibility complex, MHC)的基因,位于6号染色体短臂(6p21.31),包括一系列紧密连锁的基因座,与人类免疫功能密切相关。有研究认为HLA-B*4601和HLA-B*5401与SARS的严重程度相关。
跨膜丝氨酸蛋白酶2(transmembrane protease serine 2,TMPRSS2)属于跨膜蛋白,其不同突变型(rs383510)会导致该蛋白的表达量不同(增高),而TMPRSS2表达量增高会提高流感病毒的致病性,使其对下呼吸道感染的能力增强而导致快速进展的重症肺炎。
此外,仍有许多基因的多态性与特定病原体所引起肺部感染的易感性相关。血管紧张素转化酶-1(angiotensin converting enzyme -1,ACE1)D等位基因会增加SARS感染的风险;Toll样受体中TLR1、TLR2、TLR4及TLR9的某些等位基因会使结核菌、鼻病毒等病原体的易感性增加,但是它们与重症肺炎或疾病预后的关系尚需进一步研究。
三、与新型冠状病毒肺炎严重程度相关的基因易感性
新型冠状病毒肺炎(COVID-19)由一种新型冠状病毒(SARS-CoV-2)引起,引发了世界范围内的大流行,目前针对COVID-19和基因易感性有较多深入的研究。
1. 3p21.31基因座
在COVID-19的相关研究中,第一个由全基因组关联分析(genome wide association study, GWAS)确定的基因座是3p21.31,其与重症COVID-19以及呼吸衰竭相关。3p21.31位于一组基因簇中,其中包括钠亚氨基酸转运体1(SIT1)(SLC6A20)、人类亮氨酸拉链转录因子样1(LZTFL1)、CC基序趋化因子受体9(CCR9)、FYVE和卷曲线圈结构域含蛋白1(FYCO1)、C-X基序趋化因子受体6(CXCR6)和X-C基序趋化因子受体1(XCR1)基因。在另一项研究中,确定了两个该基因座的主要突变,即:rs2271616和rs10490770。rs2271616指向SLC6A20基因,该基因与ACE2相互作用的钠转运蛋白,可能与COVID-19的易感性相关。rs10490770则与COVID-19患者肺部CXCR6表达降低相关,可能会导致更高的重症风险。
2. ABO血型
第二个发现的与COVID-19相关的基因座位于9q34.2,与ABO血型基因座相重叠,初步探索认为O型血具有保护作用,而A型血则与重型COVID-19相关。但在ABO血型与COVID-19的相关研究中,研究人员发现了数个可能的混杂因素。首先,O型血与较低的ACE1活性相关,这可能会降低高血压等心血管疾病的风险,从而与较低的COVID-19的重症率有关。此外,ABO血型与至少8种血浆中蛋白质水平相关,其中包括Ⅷ因子、IL-6、TNF-α和CD209。而也有研究表明,ABO血型系统可能通过增强凝血作用来对COVID-19产生影响;因此,ABO血型系统对COVID-19易感性及严重性的直接影响机制尚需进一步研究。
3. ACE2
ACE2是位于细胞膜上的受体,于肺、心脏、肾及消化道高表达,功能是将血管紧张素Ⅱ分解为血管紧张素1-7。SARS-CoV-2可以通过棘突蛋白(S蛋白)的受体结构域与ACE2结合进入细胞内。ACE2水平对疾病严重程度的影响具有2个相反的效应:一方面,高水平ACE2会有更多的受体供病毒进入细胞;另一方面,ACE2活性的增加则可以发挥抗炎及预防血栓形成的作用。在一种罕见的X连锁变异体rs190509934中,携带等位基因C的个体ACE2表达较低使得感染风险降低,但对严重程度并没有显著影响。
4. 寡腺苷酸合成酶
寡腺苷酸合成酶1(oligoadenylate synthetase,OAS1)基因是干扰素诱导基因,主要在机体病毒防御方面发挥作用。与dsRNA结合后,OAS1以三磷酸腺苷为原料产生2′-5′寡腺苷酸并激活RNase L并诱导病毒RNA降解以阻断病毒复制。其变体「尼安德特单倍型」(rs10774671、rs1131454)通过降低OAS1降解水平来增强抗病毒作用,但这种由基因型决定的抗病毒作用不会在接受干扰素治疗的人群中显现,提示在整个干扰素诱导OAS1的抗病毒过程中,干扰素是更为重要的影响因素。
5. 其他
二肽基肽酶9(dipeptidyl peptidase 9,DPP9)属于丝氨酸蛋白酶家族,参与CXCL10、CXCL11等细胞因子的信息传递和抗原提呈过程。其部分变体(rs12610495)会导致DPP9水平降低,这一效应也与COVID-19严重程度增加有关。
酪氨酸激酶2(tyrosine kinase 2,TYK2)是多种细胞因子和Th细胞免疫应答所需的酶。TYK2变体rs74956615与COVID-19的严重程度密切相关,其机制可能与TYK2活性降低有关。
此外,尚有一些在其他病原体感染中表现出影响肺炎严重程度的基因(HLA-rs9380142、TMPRSS2等)也在COVID-19的重症肺炎发生率等方面表现出一定的影响,但其具体的作用机制仍需进一步研究。
四、结语
重症肺炎的影响因素有许多,其中既包括性别、年龄、是否吸烟、慢性病状态等宿主内在的因素,也包括感染病原体种类、疫苗接种情况等外在环境因素。随着人类基因组计划等一系列旨在阐述人类遗传因素的研究相继开展或完成,人类对遗传机制在重症肺炎的发生发展中所起的作用逐渐予以重视。尤其是在面对像COVID-19这样的呼吸系统疾病大流行的当下,针对不同基因型个体,建立有针对性的重症肺炎预警机制和治疗体系是十分必要的。
参考文献
[1] Xu J, Murphy S L, Kochanek K D, et al. Deaths: Final Data for 2013. Natl Vital Stat Rep. 2016;64(2).
[2] Ramirez J A, Wiemken T L, Peyrani P, et al. Adults Hospitalized With Pneumonia in the United States: Incidence, Epidemiology, and Mortality. Clin Infect Dis. 2017;65(11):1806-12.
[3] Lacoma A, Mateo L, Blanco I, et al. Impact of Host Genetics and Biological Response Modifiers on Respiratory Tract Infections. Front Immunol. 2019;10:1013.
[4] Metlay J P, Waterer G W, Long A C, et al. Diagnosis and Treatment of Adults with Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019;200(7):e45-e67.
[5] Liapikou A, Ferrer M, Polverino E, et al. Severe community-acquired pneumonia: validation of the Infectious Diseases Society of America/American Thoracic Society guidelines to predict an intensive care unit admission. Clin Infect Dis. 2009;48(4):377-85.
[6] 袁伟锋, 黄文杰, 梁坤. TNF-α基因单核苷酸多态性与肺炎的相关性研究. 中国病理生理杂志. 2008;24(12):2391-5.
[7] 李理, 郑少强, 袁伟锋, et al. 肿瘤坏死因子受体基因单核苷酸多态性与肺炎严重程度的相关性. 中国病理生理杂志. 2013;29(4):695-700.
[8] Fine M J, Auble T E, Yealy D M, et al. A prediction rule to identify low-risk patients with community-acquired pneumonia. N Engl J Med. 1997;336(4):243-50.
[9] Lim W S, van der Eerden M M, Laing R, et al. Defining community acquired pneumonia severity on presentation to hospital: an international derivation and validation study. Thorax. 2003;58(5):377-82.
[10] 郑少强, 袁伟锋, 李理, et al. NFκB1基因启动序列-94ins/delATTG多态性与社区获得性肺炎易感性及严重程度相关性研究. 中国感染与化疗杂志. 2012;12(2):133-6.
[11] Ghafouri-Fard S, Noroozi R, Vafaee R, et al. Effects of host genetic variations on response to, susceptibility and severity of respiratory infections. Biomed Pharmacother. 2020;128:110296.
[12] Meyer N J, Feng R, Li M, et al. IL1RN coding variant is associated with lower risk of acute respiratory distress syndrome and increased plasma IL-1 receptor antagonist. Am J Respir Crit Care Med. 2013;187(9):950-9.
[13] Chou S-C, Ko H-W, Lin Y-C. CRP/IL-6/IL-10 Single-Nucleotide Polymorphisms Correlate with the Susceptibility and Severity of Community-Acquired Pneumonia. Genet Test Mol Biomarkers. 2016;20(12):732-40.
[14] Gallagher P M, Lowe G, Fitzgerald T, et al. Association of IL-10 polymorphism with severity of illness in community acquired pneumonia. Thorax. 2003;58(2):154-6.
[15] Schaaf B M, Boehmke F, Esnaashari H, et al. Pneumococcal septic shock is associated with the interleukin-10-1082 gene promoter polymorphism. Am J Respir Crit Care Med. 2003;168(4):476-80.
[16] Wang H, Guo S, Wan C, et al. Tumor necrosis factor-α -308 G/A polymorphism and risk of sepsis, septic shock, and mortality: an updated meta-analysis. Oncotarget. 2017;8(55):94910-9.
[17] Yuan F F, Boehm I, Chan P K S, et al. High prevalence of the CD14-159CC genotype in patients infected with severe acute respiratory syndrome-associated coronavirus. Clin Vaccine Immunol. 2007;14(12):1644-5.
[18] Yuan F F, Marks K, Wong M, et al. Clinical relevance of TLR2, TLR4, CD14 and FcgammaRIIA gene polymorphisms in Streptococcus pneumoniae infection. Immunol Cell Biol. 2008;86(3):268-70.
[19] Chan K Y K, Xu M-S, Ching J C Y, et al. CD209 (DC-SIGN) -336A>G promoter polymorphism and severe acute respiratory syndrome in Hong Kong Chinese. Hum Immunol. 2010;71(7):702-7.
[20] Zhou J, To K K-W, Dong H, et al. A functional variation in CD55 increases the severity of 2009 pandemic H1N1 influenza A virus infection. J Infect Dis. 2012;206(4):495-503.
[21] Dahmer M K, O'Cain P, Patwari P P, et al. The influence of genetic variation in surfactant protein B on severe lung injury in African American children. Crit Care Med. 2011;39(5):1138-44.
[22] To K K W, Zhou J, Song Y-Q, et al. Surfactant protein B gene polymorphism is associated with severe influenza. Chest. 2014;145(6):1237-43.
[23] Liu P T, Stenger S, Tang D H, et al. Cutting edge: vitamin D-mediated human antimicrobial activity against Mycobacterium tuberculosis is dependent on the induction of cathelicidin. J Immunol. 2007;179(4):2060-3.
[24] Alvarez A E, Marson F A L, Bertuzzo C S, et al. Association between single nucleotide polymorphisms in TLR4, TLR2, TLR9, VDR, NOS2 and CCL5 genes with acute viral bronchiolitis. Gene. 2018;645.
[25] Lin M, Tseng H-K, Trejaut J A, et al. Association of HLA class I with severe acute respiratory syndrome coronavirus infection. BMC Med Genet. 2003;4:9.
[26] Cheng Z, Zhou J, To K K-W, et al. Identification of TMPRSS2 as a Susceptibility Gene for Severe 2009 Pandemic A(H1N1) Influenza and A(H7N9) Influenza. J Infect Dis. 2015;212(8):1214-21.
[27] Itoyama S, Keicho N, Quy T, et al. ACE1 polymorphism and progression of SARS. Biochem Biophys Res Commun. 2004;323(3):1124-9.
[28] Patarčić I, Gelemanović A, Kirin M, et al. The role of host genetic factors in respiratory tract infectious diseases: systematic review, meta-analyses and field synopsis. Sci Rep. 2015;5:16119.
[29] Ellinghaus D, Degenhardt F, Bujanda L, et al. Genomewide Association Study of Severe Covid-19 with Respiratory Failure. N Engl J Med. 2020;383(16):1522-34.
[30] Mapping the human genetic architecture of COVID-19. Nature. 2021;600(7889):472-7.
[31] Vuille-dit-Bille R N, Camargo S M, Emmenegger L, et al. Human intestine luminal ACE2 and amino acid transporter expression increased by ACE-inhibitors. Amino Acids. 2015;47(4):693-705.
[32] Dai Y, Wang J, Jeong H-H, et al. Association of CXCR6 with COVID-19 severity: delineating the host genetic factors in transcriptomic regulation. Hum Genet. 2021;140(9):1313-28.
[33] Dai X. ABO blood group predisposes to COVID-19 severity and cardiovascular diseases. Eur J Prev Cardiol. 2020;27(13):1436-7.
[34] Wang L, Balmat T J, Antonia A L, et al. An atlas connecting shared genetic architecture of human diseases and molecular phenotypes provides insight into COVID-19 susceptibility. Genome Med. 2021;13(1):83.
[35] Wool G D, Miller J L. The Impact of COVID-19 Disease on Platelets and Coagulation. Pathobiology. 2021;88(1):15-27.
[36] Shang J, Wan Y, Luo C, et al. Cell entry mechanisms of SARS-CoV-2. Proc Natl Acad Sci U S A. 2020;117(21):11727-34.
[37] Debnath M, Banerjee M, Berk M. Genetic gateways to COVID-19 infection: Implications for risk, severity, and outcomes. FASEB J. 2020;34(7):8787-95.
[38] Horowitz J E, Kosmicki J A, Damask A, et al. Genome-wide analysis in 756,646 individuals provides first genetic evidence that expression influences COVID-19 risk and yields genetic risk scores predictive of severe disease. medRxiv. 2021.
[39] Gaziano L, Giambartolomei C, Pereira A C, et al. Actionable druggable genome-wide Mendelian randomization identifies repurposing opportunities for COVID-19. Nat Med. 2021;27(4):668-76.
[40] Hu J, Wang X, Xing Y, et al. Origin and development of oligoadenylate synthetase immune system. BMC Evol Biol. 2018;18(1):201.
[41] Banday A R, Stanifer M L, Florez-Vargas O, et al. Genetic regulation of nonsense-mediated decay underlies association with risk of severe COVID-19. medRxiv. 2021.
[42] Zhang H, Maqsudi S, Rainczuk A, et al. Identification of novel dipeptidyl peptidase 9 substrates by two-dimensional differential in-gel electrophoresis. FEBS J. 2015;282(19):3737-57.
[43] Human genomics. The Genotype-Tissue Expression (GTEx) pilot analysis: multitissue gene regulation in humans. Science (New York, NY). 2015;348(6235):648-60.
[44] Pairo-Castineira E, Clohisey S, Klaric L, et al. Genetic mechanisms of critical illness in COVID-19. Nature. 2021;591(7848):92-8.
[45] Corman V M, Muth D, Niemeyer D, et al. Hosts and Sources of Endemic Human Coronaviruses. Adv Virus Res. 2018;100:163-88.
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。