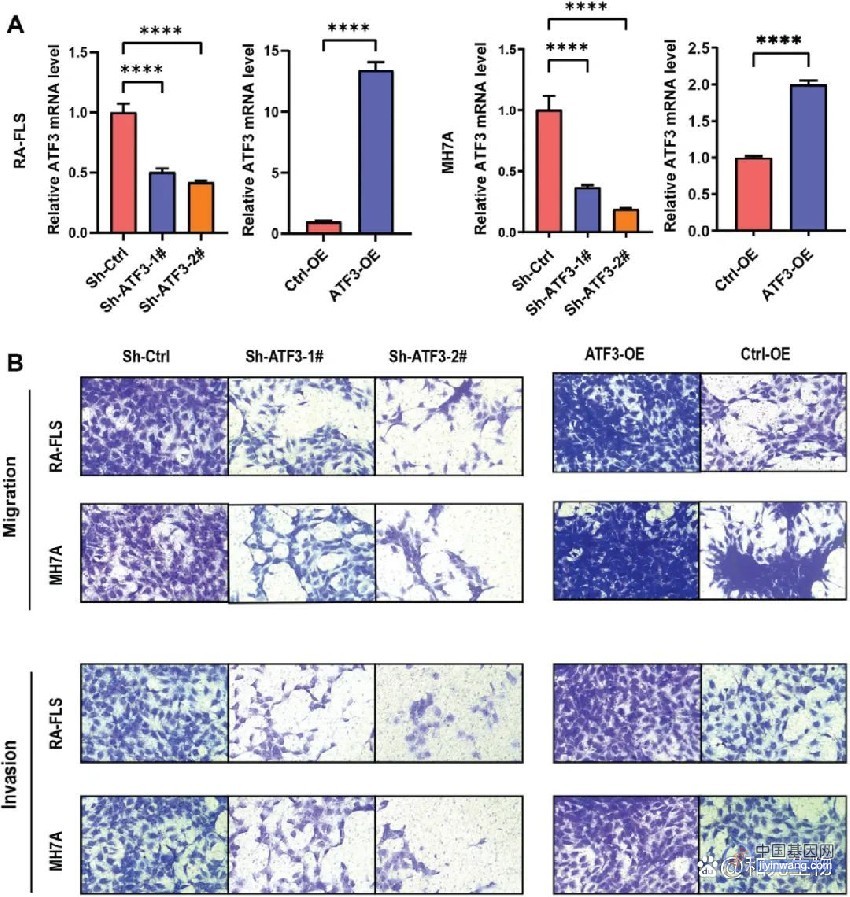
用于DNA杂交染色质结构解析的空间基因组校准器
在细胞的生命周期中,真核生物染色体经历剧烈的压缩和解压缩过程,这一动态的结构对于细胞核中DNA复制,重组,修复及基因转录等过程十分重要【1-3】。多路复用DNA荧光原位杂交(multiplexed DNA fluorescence in situ hybridization, M-DNA-FISH)是分析真核生物三维基因组结构的常用手段,能识别几十到几千个基因组位点,但其并不直接对染色质进行追踪,从噪点荧光信号中提取染色质构象信息一直以来都存在挑战,我们需要一个染色质追踪的新框架。
近日,加州大学表观基因组研究中心的任兵教授团队在Nature Biotechnology上发表了题为A spatial genome aligner for resolving chromatin architectures from multiplexed DNA FISH的文章,报道了一个空间基因组校准器,通过将信号对准DNA聚合物模型,从噪声中解析真正的染色质信号。作者用此方法对以往的全基因组染色体追踪数据进行再处理,发现非同期的小鼠胚胎干细胞S/G2期姐妹染色单体会发生空间聚集,并为成年小鼠皮层有丝分裂后期神经元中保持紧密配对的胞外染色体的存在提供了证据。

作者认为尽管染色质纤维形态高度可变,但其受限于聚合物的空间限制【4-5】,因此除信号光学性能外,他们将是否符合染色质聚合物模型(两个分散位点间基因组距离限制)纳入考量,并利用Hi-C中检测到的成对contact数据进行准确度的评估,作者发现在5kb,25kb和1Mb范围内,校准器都能重塑Hi-C中发现的染色质组织模式。此外,作者也注意到由DNA长度到染色质尺度的推断存在挑战,于是让他们将DNA持续长度固定在150bp,拟合基因组—空间距离尺度。
染色质是线性的柔性聚合物,高斯链(Gaussian chain)是解析其空间构象的一个简单且稳健的模型。此模型认为多聚物是由一系列单体构成的,由近似恒定长度的键相连,单体间能够相互旋转,沿着聚合物链,单体能够从一个过渡到另一个。对于链上任意两个单体而言,它们被向量距离分开的概率符合高斯分布。在M-DNA-FISH中,染色体被标记为分散位置且位点间间隔一定距离,这与高斯链上分散的单体及其恒定键长类似,于是作者认为在大的基因组尺度上,DNA构象可以用高斯链来模拟,成像位点上最有可能的聚合物是染色质纤维总长度与预期片段长度最相符的位点。在算法上,作者首先提取成像染色质荧光信号作为有向非循环图的节点,节点的拓扑次序取决于参考基因组的位点次序,而后再与邻近节点联系起来(图1)。
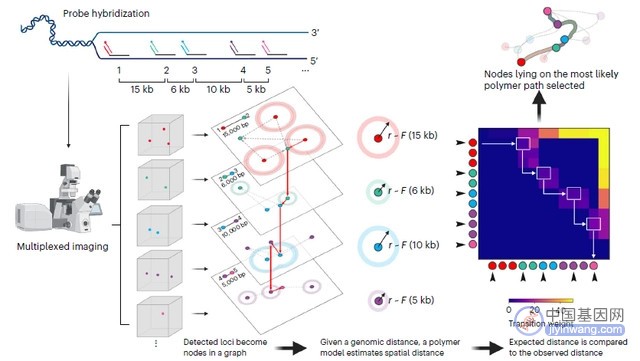
图1 空间基因组校准流程
通过对之前发表过的小鼠胚胎干细胞(mESCs)DNA seqFISH+数据的分析,作者衡量了空间基因组校准器,发现其能够在多个基因组尺度上实现单细胞分辨率的单分子染色质纤维解析。当应用于5kb分辨率的M-DNA-FISH数据时,校准器能够重塑区域内的拓扑相关结构域。由于整合了所有成像位点的相对位置,校准器实现了全局优化,使用动态程序设计,在线性时间内追踪最可能的聚合物纤维。至此,作者认为其能够在不同长度尺度下,在多个数据集及不同的M-DNA-FISH数据中模拟染色质纤维。
空间基因组校准器不依赖于染色质纤维的识别框架提供密度和倍性信息,作者认为间期细胞的染色体拷贝数可以直接通过物理上聚合纤维的计数获得,他们首先通过打乱参考基因组模拟聚合物模型来设置一个可能阈值,而后迭代应用空间基因组比对,由此产生了一个连续染色质纤维的正交数据集,这一过程称为“聚合物纤维核型分析”(Polymer fiber karyotyping)。这一策略使得其能够准确识别细胞核型,甚至区分间期中人眼不能识别的拷贝数,1,000个非整倍体细胞中间期染色体的计数验证了其准确度。
接下来,作者分别将空间基因组校准器应用于四倍体mESCs和小鼠皮层神经元中。他们发现mESCs中四倍体细胞实际上是复制的二倍体细胞,因其显示成对的姐妹染色单体,提示同源染色体的聚集,这一紧实的4N状态分散于通往S期的间期中,其很少在多个染色体中同步,看起来像是随机发生的。作者分析了701个完全分段的小鼠皮层神经元,并在单倍型分辨率的单细胞Dip-C测序中验证了核型分析结果,他们发现皮层神经元中普遍存在拷贝数变异且胞外染色体可能是由一个核型导致的,胞外染色体与另一个染色质纤维共享一个染色质领域,这可能为胞外染色质的起源带来新的见解。
综上,文章提出了一个用于多路复用FISH染色质结构解析的空间基因组校准器,它利用基因组距离分离成像位点,并评估信号属于位点的物理概率,在不同的尺度下它都能够有效模拟染色质结构,并能够用于间期细胞中染色体倍性的预测。
原文链接:
https://doi.org/10.1038/s41587-022-01568-9
参考文献
1. Pope, B. et al. Topologically associating domains arestable units of replication-timing regulation. Nature 515,402–405 (2014).
2. Schuster-Böckler, B. & Lehner, B. Chromatin organization is amajor influence on regional mutation rates in human cancer cells.Nature 488, 504–507 (2012).
3. Arnould, C. et al. Loop extrusion as a mechanism for formation ofDNA damage repair foci. Nature 590, 660–665 (2021).
4. Yamakawa, H. & Yoshizaki, T. Helical Wormlike Chains in PolymerSolutions (Springer, 2016).
5. Ross, B. & Wiggins, P. Measuring chromosome conformation withdegenerate labels. Phys. Rev. E. 86, 011918 (2012).
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。