科学家总结癌症基因组学发展历程,展望未来发展方向
近日,北京大学生物医学前沿创新中心主任、生命科学学院教授张泽民受邀全面总结了癌症基因组学的发展历程,展望了其未来发展方向。相关文章于4月13日发表于《细胞》。
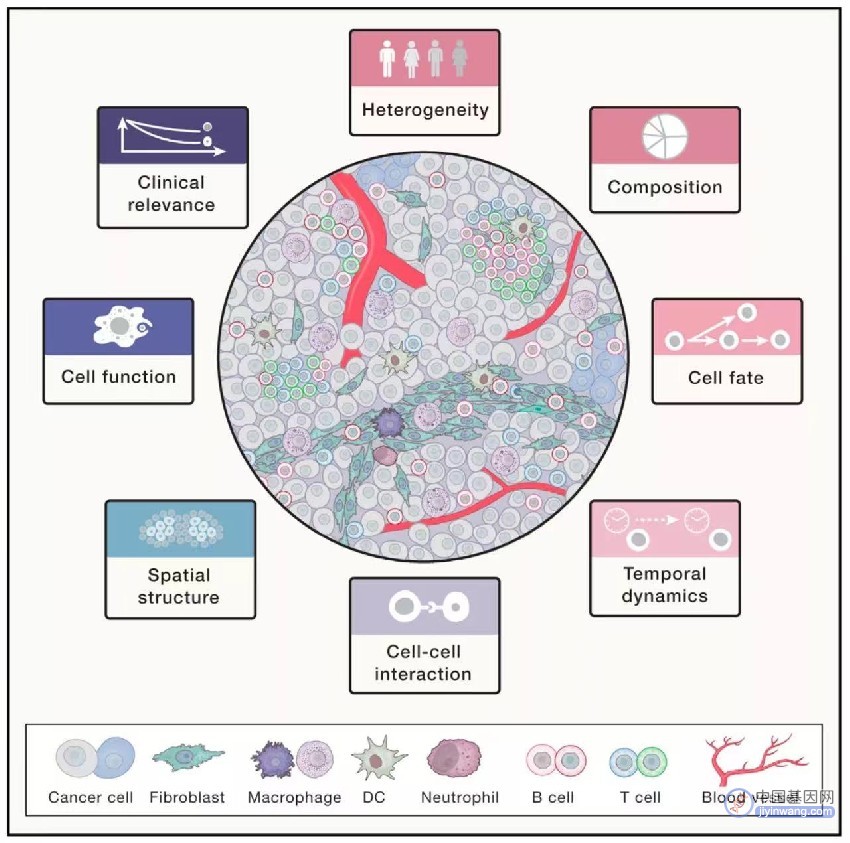
刻画肿瘤微环境的特征
“在很长一段时间内癌症发生、发展过程中的分子驱动机制仍不完全清楚。”张泽民告诉《中国科学报》,癌症基因组学技术能够系统性地鉴定癌细胞的突变和基因表达情况,这对于理解致癌机制、癌细胞分子特征以及癌症的分型十分重要。
此外,癌症基因组学也极大地促进了癌症精准医疗的发展。例如,具有EGFR突变的非小细胞肺癌患者和具有BRAF突变的黑素瘤患者可以对相应靶向药产生临床响应。
“世界上没有两个完全相同的肿瘤。” 张泽民教授表示,“每个肿瘤都具有其特有的突变组合或分子特征,癌症基因组学可以帮助我们理解为什么每个肿瘤都是独特的,即了解肿瘤的异质性。”
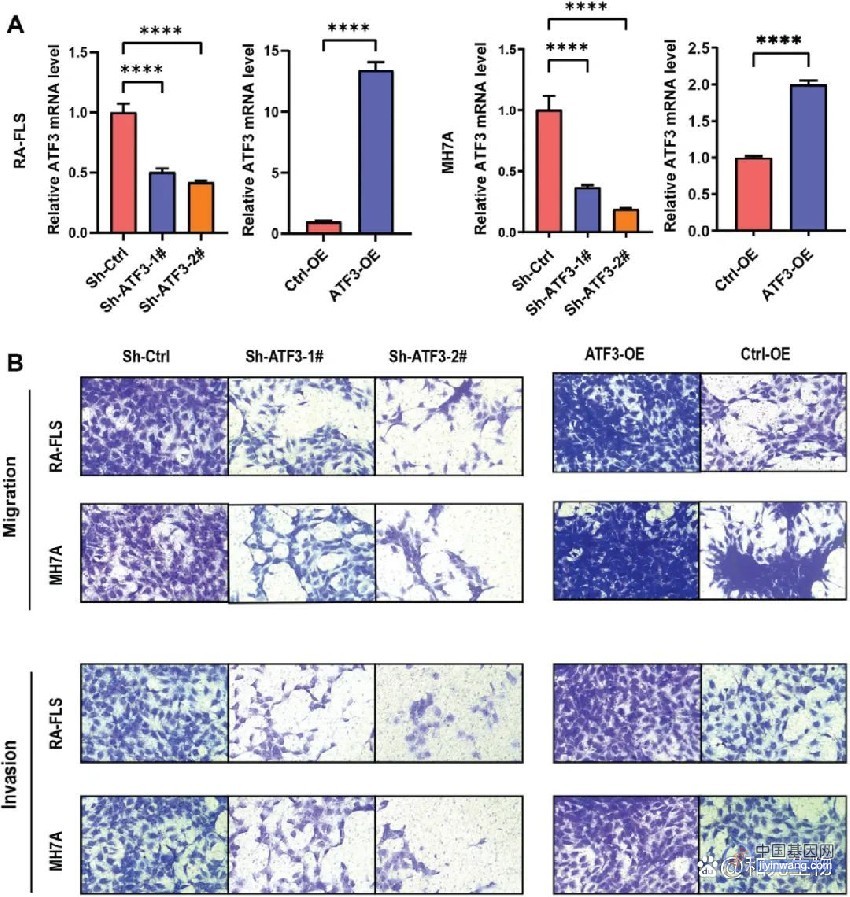
肿瘤中除了癌细胞,也有多种其他的细胞类型,包括免疫细胞和非免疫细胞。特定的细胞类型可能促进癌症的发展,也可能具有抗肿瘤的功能,有些细胞类型甚至可能同时具有抗肿瘤和促肿瘤的功能。因此,全面理解肿瘤的细胞组成,即刻画“肿瘤微环境”,能极大加速我们对肿瘤的理解。单细胞测序技术的出现使得癌症基因组学进入了新的阶段,研究者不仅可以全面刻画肿瘤中不同细胞类群的功能状态、组分、相互作用关系和空间分布,也可以解析癌症治疗过程中肿瘤微环境的动态变化,帮助我们理解肿瘤的异质性、以及癌症治疗例如免疫治疗的响应和抵抗机制。
在肿瘤治疗方面,随着研究的视野从癌细胞提升至整个肿瘤生态系统,文章突出强调了一种新的治疗方案开发思路。传统疗法关注癌细胞,通过干扰 “靶基因”直接杀死癌细胞。
在此基础上,文章提出肿瘤治疗的“靶细胞”理论,通过识别并干预肿瘤微环境中的“靶细胞”,扰动肿瘤微环境中的细胞相互作用网络,进而增强免疫系统杀伤癌细胞的能力,从而有效控制甚至消灭肿瘤。张泽民表示,“靶细胞的研究思路有望拓展当前的免疫检查点抑制疗法,为肿瘤治疗提供新的前景。”
当前,肿瘤基因组学仍处在迅猛发展之中。随着数据的累积和新的技术的开发,未来几年内,肿瘤基因组学有望在基础肿瘤生物学与临床转化应用的多个方面产生重要的突破性成果。
例如,我们将逐渐掌握人类肿瘤的完整组成成分以及各个成分的相互作用关系,全面理解肿瘤发展的时空动态变化规律;与此同时,我们也将能够系统性阐述癌症发生的早期因果机制,准确定位肿瘤恶性转化的时间点,并指出不同肿瘤微环境类型产生的动态过程与影响因素,为肿瘤的精准治疗提供依据;进一步,结合液体活检技术对肿瘤微环境状态的无创探测,基因组学方法将助力癌症的早期发现与治疗。
相关论文信息:
https://www.cell.com/cell/fulltext/S0092-8674(23)00143-5
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。