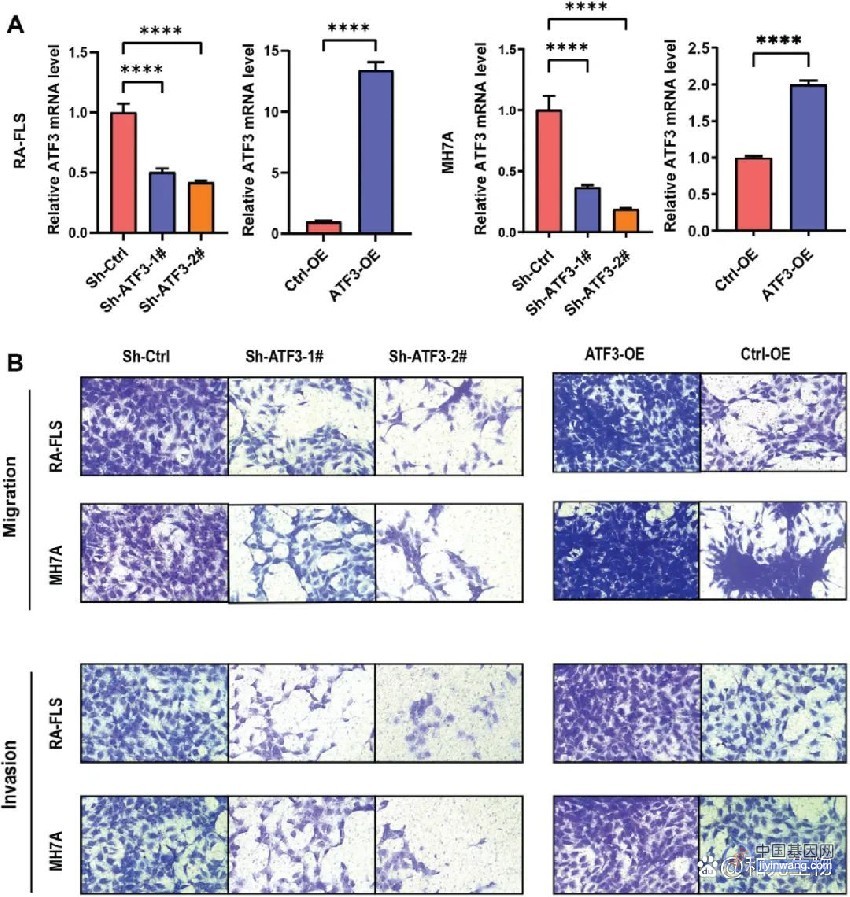
Nature:基因组定位涉及精神分裂症的基因和突触生物学
精神分裂症的遗传率为60 - 80%,其中大部分可归因于常见的风险等位基因。在一项分阶段的全基因组关联研究中,共有76755名精神分裂症患者和243649名对照个体,该研究报告了287个不同基因组位点的常见变异关联。这种关联集中在在中枢神经系统的兴奋性和抑制性神经元中表达的基因中,但在其他组织或细胞类型中不存在。利用精细定位和功能基因组数据,研究者确定了120个基因(106个蛋白编码)可能在某些位点上支持相关性,包括16个具有可信的因果非同义或非翻译区域变异的基因。也涉及到与神经元功能相关的基本过程,包括突触的组织,分化和传递。近期,来自全世界的几百位科学家发现候选基因在精神分裂症患者中与罕见的破坏性编码变异相关的基因中富集,包括谷氨酸受体亚基GRIN2A和转录因子SP4,并且在神经发育障碍中也富集了与此类变异相关的基因。这项研究发表在Nature上:DOI:10.1038/s41586-022-04434-5。

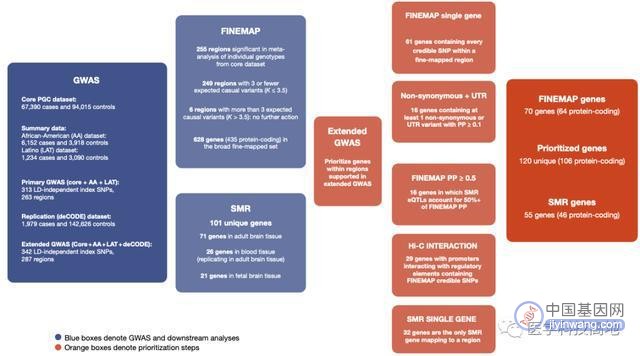
GWAS和基因优先级的概述
(下图中) 总结GWAS、精细映射(FINEMAP)和SMR分析的流程图,以及这些分析如何决定基因优先级。
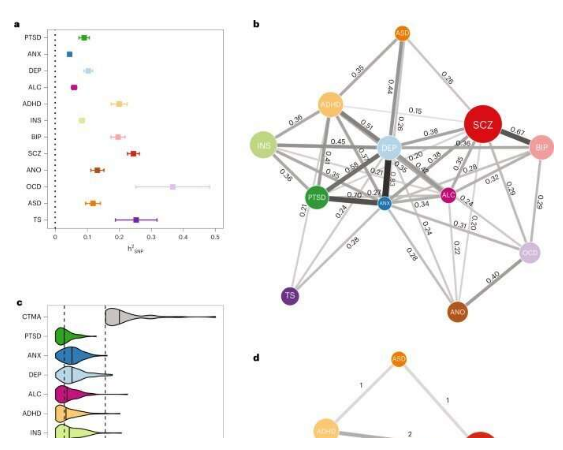
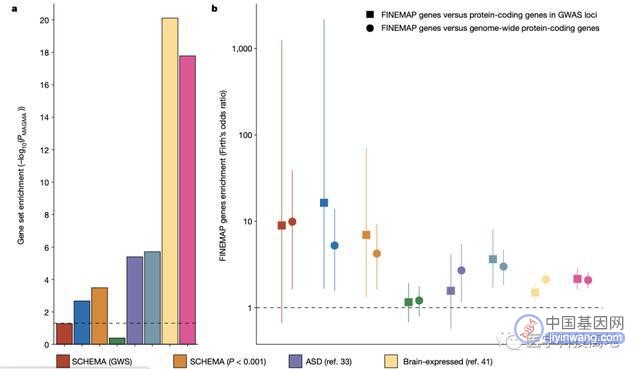
在全基因组水平上对包含FINEMAP可信SNPs的蛋白质编码基因进行基因集富集试验。测试的基因集从精神分裂症、ASD和发育障碍(DD)的测序研究中检索。代表不耐受功能丧失突变(lof不耐受)和脑表达基因的基因集也被显示出来。a、MAGMA基因集富集分析。虚线表示名义显著(P = 0.05)。b, 包含至少1个可信FINEMAP SNP (n = 418,排除无lof不耐受数据的基因)的蛋白编码基因与组内基因之间相关性的优势比(和95% CI)。优势比与GWAS K≤3.5位点内的蛋白编码基因(1,283个基因;或整个基因组,不包括扩展的MHC43(19547个基因;圈)。虚线表示没有浓缩。。
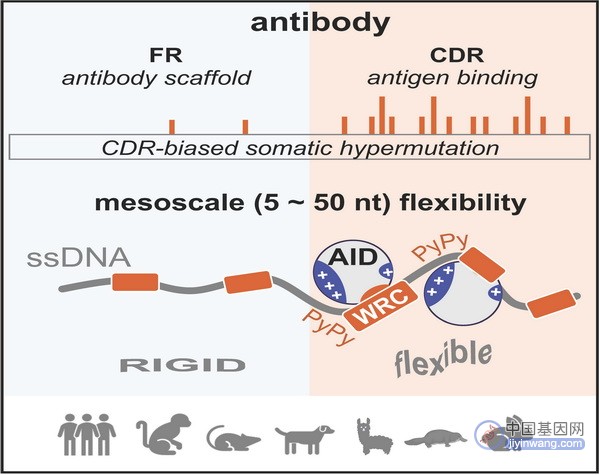
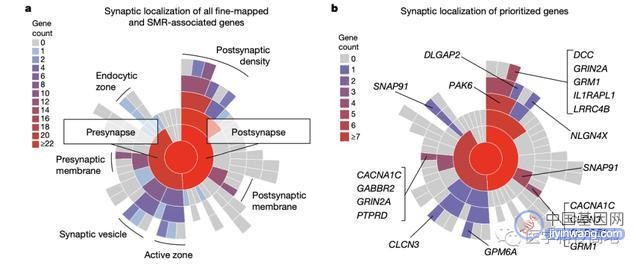
▉ 使用SynGO绘制所有精细映射和smr相关基因,以及优先级基因到突触位置
a,FINEMAP/SMR基因是由FINEMAP识别的至少一个可信SNP标记和/或SMR相关的蛋白编码基因(n = 470),其中n = 58是syngo注释的,51是细胞成分。b,优先排序基因(扩展数据表1;n = 106),其中15个是syngo标注的,14个是细胞成分。
详见 DOI: 10.1038/s41586-022-04434-5
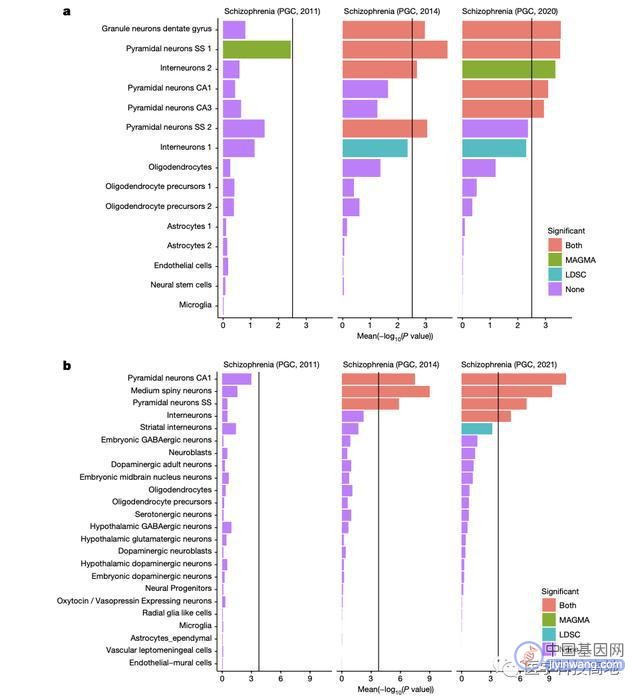
精神分裂症与人类和小鼠大脑多个区域细胞类型的关系。
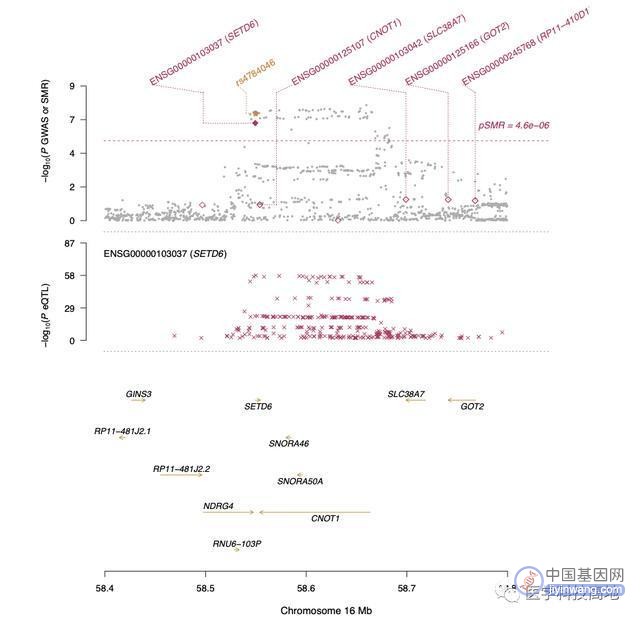
▉SMR+HEIDI分析结合GWAS和eQTL研究的数据
所有重要的SMR结果都在补充数据中提供。有强有力的证据表明,精神分裂症的关联可能是通过单个基因SETD6的表达来介导的。顶部的轨道显示了精神分裂症GWAS(扩展前数据)中SNPs的-log10(p值)(灰色点)。每个红色菱形表示SMR测试中与精神分裂症相关的基因表达的-log10(p值)。实菱形表示未被海蒂过滤拒绝的探针。黄色菱形表示与最高顺式eqtl (rs4784046)的SNP有关。
▉新颖之处
到目前为止,该项研究试对精神分裂症进行了最大的gwas研究,在此过程中,研究者发现了相关基因座数量的显著增加。通过精细定位,他们优先选择的相关基因位点对于那些在精神分裂症中罕见有害突变负担增加的人来说是丰富的,并识别了GRIN2A, SP4,STAG1和FAM120A作为特殊基因,其罕见和常见变异关联的聚合强烈支持其在疾病中的致病作用。值得注意的是,这种趋同也暗示了altere的致病相关性。
▉ 结语
精神分裂症通常在青春期晚期或成年早期表现出来,与预期寿命缩短、自杀风险增加、严重的身体疾病以及大量的健康和社会成本有关。对大多数人来说,治疗至少部分有效,但许多人有慢性症状,而且不良治疗效果很常见。科学家需要发现新的治疗靶点,但对病理生理学的了解有限,阻碍了这一过程。个体之间的风险变异大多是遗传的,包括大量的常见等位基因、罕见的拷贝数变异和罕见的编码变异。先前的全基因组关联研究(GWAS)报告了176个包含与精神分裂症相关的常见等位基因的基因组位点,但驱动这些关联的因果变异以及这些变异的生物学后果在很大程度上是未知的。为了增加对常见变异对精神分裂症的贡献的理解,该研究进行了迄今为止我们所知的最大的疾病GWAS,并分析了这些发现,优先考虑导致发病的变异、基因和生物过程。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。