创新的疾病控制技术:合成“隔间”阻止病原体共享抗生素抗性基因
杜克大学的生物医学工程师已经展示了一种控制细胞生化过程的新合成方法。与其通过传统的"锁和钥匙"机制创造直接与细胞机械相互作用的颗粒或结构,不如引导细胞建立物理上停止-或鼓励-生物分子功能的"隔间"。
杜克大学生物医学工程师开发了一种控制细胞过程的新合成方法。该方法涉及指导细胞建立调节生物分子功能的隔间,而不是直接与细胞机械互动。这种方法可以影响细菌之间的遗传指令传播和哺乳动物细胞中的蛋白质回路,有可能导致理解和对抗疾病和抗生素抗性病原体的新策略。
研究人员证明,他们的方法可以影响两个细胞过程,一个负责在细菌中传播遗传指令,另一个负责调节哺乳动物细胞中的蛋白质回路。这些结果可能被证明对开发新的战略以了解和对抗疾病或阻止抗生素抗性病原体的传播是非常宝贵的。该成果今天(2023年2月6日)在线发表于《自然-化学生物学》杂志。
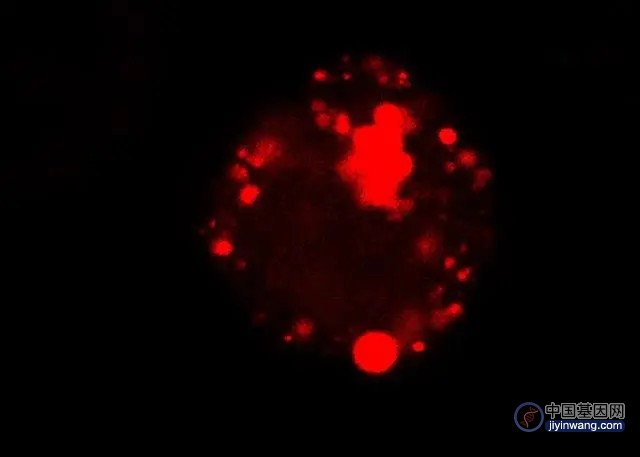
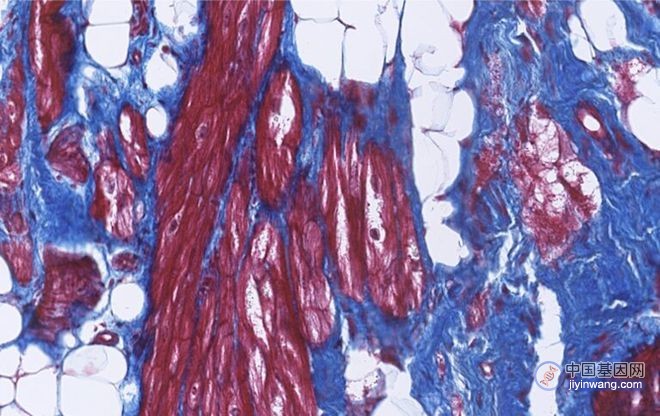
这些红色斑点是荧光的合成隔间,由活细胞自身的生物机器建造,以控制其生物分子行为。资料来源:戴一凡,杜克大学
戴一凡是一名博士后研究员,在杜克大学生物医学工程系Alan L. Kaganov特聘教授Ashutosh Chilkoti的实验室和生物医学工程系James L. Meriam特聘教授Lingchong You的实验室工作,他胡搜:"一个活细胞就像一碗浓稠的面汤,细胞中生物分子的密度有时被描述为把地球上的每个人都放入大盐湖。"
戴说:"琥珀的形成有时会将动物锁住并保存数千年,因为它与周围环境相比具有独特的材料特性。科学家们认为,也许细胞可以对信息做同样的事情。"
生物微机械通常依赖于所谓的"锁和钥匙"机制,其中一个蛋白质、基因链或其他生物大分子的形状和大小恰好可以与其目标结构相互作用。因为这些是最容易和最明显的研究和重现的过程,几乎所有的生物医学研究都集中在其庞大而复杂的机械网络。
但是,由于细胞中密布着这种生物分子机械,而且它们需要控制活动以应对整个生命过程中的不同需求,科学家们长期以来一直怀疑它们必须有方法来调控活动。但直到2009年,研究人员才发现了这样一种方法的机制,称为相分离介导的生物凝集物。
生物凝结物是细胞可以建立的小隔间,将某些蛋白质和分子分离或困在一起,阻碍或促进其活动。研究人员刚刚开始了解冷凝物是如何工作的,以及它们可以用来做什么。创建一个可以告诉细胞创建这些生物分子笼子的合成版本的平台是朝着这两个目标迈出的一大步。
本研究最值得关注的部分是过去研究中出现的规则在指导这些冷凝物的物理特性的合理工程方面的有效性,而这些冷凝物又在活细胞中有效地工作,尽管有许多与细胞内环境有关的干扰因素。
在这篇论文中,Dai、Chilkoti、You和他们来自圣路易斯华盛顿大学Gene K. Beare生物医学工程杰出教授和生物分子凝集物中心主任Rohit V. Pappu实验室的同事,展示了创建一套合成的遗传指令,使细胞创建不同类型的凝集物以捕获各种生物分子过程。在一个例子中,他们建立了凝结物,阻止被称为质粒的DNA小包在细菌之间传播,这个过程被称为水平基因转移。这个过程是病原体用来传播对抗生素的抗性的主要方法之一,阻止它的发生可能是打击"超级细菌"的产生和扩散的关键一步。
研究人员还表明,他们可以用这种方法来控制大肠杆菌中DNA转录成RNA的过程,通过将不同的因素聚集在一起,有效地放大特定基因的表达。他们进一步展示了这种方法在哺乳动物细胞中调控蛋白质电路。调控特定基因的活性和蛋白质的活动可能是对抗各种疾病,特别是遗传性疾病的一个有用方法。
"这篇论文表明,我们作为生物医学工程师,可以从头开始设计新的分子部件,说服细胞制造这些部件,并在细胞内组装这些部件以制造新机器,"Chilkoti说。"这些合成的凝结物然后可以在细胞内被打开,以控制细胞的功能方式。这篇论文是一个新兴领域的一部分,它将使我们能够以新的和令人兴奋的方式重新编程生命。"
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。